工业纯碱中含少量氯化钠。兴趣小组分别采用不同的方法测定工业纯碱样品中碳酸钠的质量分数。
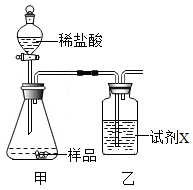
(1)方法一:差量法。称取W克样品与足量的稀盐酸充分反应,生成的二氧化碳通过装有试剂X的乙装置,并利用测量乙装置增加的质量,求得样品中碳酸钠的质量分数。该方法中试剂X可选用_________ 。
(2)方法二:沉淀法。称取15克样品完全溶解于水中配成60克样品溶液,取三个烧杯分三次进行实验,每次加入30克氯化钙溶液充分反应,过滤、洗涤、干燥所得的沉淀质量记录如表。计算样品中碳酸钠的质量分数。
(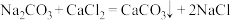 )
)
___________
(3)请写出提高方法一测量精确度的操作建议(写出2条)。____________

(1)方法一:差量法。称取W克样品与足量的稀盐酸充分反应,生成的二氧化碳通过装有试剂X的乙装置,并利用测量乙装置增加的质量,求得样品中碳酸钠的质量分数。该方法中试剂X可选用
(2)方法二:沉淀法。称取15克样品完全溶解于水中配成60克样品溶液,取三个烧杯分三次进行实验,每次加入30克氯化钙溶液充分反应,过滤、洗涤、干燥所得的沉淀质量记录如表。计算样品中碳酸钠的质量分数。
| 烧杯1 | 烧杯2 | 烧杯3 | |
| 样品溶液(克) | 10 | 20 | 30 |
| 氯化钙溶液(克) | 30 | 30 | 30 |
| 沉淀质量(克) | 2 | 4 | 5 |
(
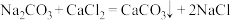 )
)(3)请写出提高方法一测量精确度的操作建议(写出2条)。
更新时间:2020-07-05 07:18:15
|
相似题推荐
解答题
|
适中
(0.65)
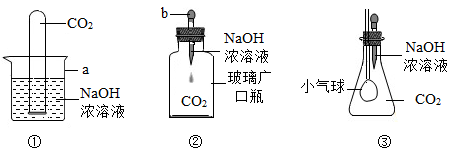
【推荐1】小明在探究CO2和NaOH是否发生反应时,设计出下列三种装置进行实验:
请回答以下几个问题:
(1)写出图中标有字母的仪器名称:a: ,b: 。
(2)以上三个实验中,①③有明显现象,请你帮小明记录他观察到的实验现象:
实验① ;实验③ 。
(3)实验②因选用仪器不当导致未能观察到明显现象,请你帮小明寻找一种物品替代该装置中的广口瓶,以使实验取得成功,你将选用的物品是 ,改进后能看到的实验现象是 。

请回答以下几个问题:
(1)写出图中标有字母的仪器名称:a: ,b: 。
(2)以上三个实验中,①③有明显现象,请你帮小明记录他观察到的实验现象:
实验① ;实验③ 。
(3)实验②因选用仪器不当导致未能观察到明显现象,请你帮小明寻找一种物品替代该装置中的广口瓶,以使实验取得成功,你将选用的物品是 ,改进后能看到的实验现象是 。
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】在化学实验中,有时药品的滴加顺序不同会导致实验现象不同。某同学使用图甲所示实验装置进行实验,广口瓶内气球的体积变化与滴加药品体积关系如图乙所示,其中A点表示开始滴加某种药品,B点表示开始滴加另一种药品(不考虑由于滴入液体的体积及反应导致的温度变化对集气瓶内气压的影响)。据图回答:

(1)实验中首先加入的试剂是_____________ 。
(2)试从加入药品的种类、顺序及发生的化学反应等角度来解释气体体积变化的情况。____________

(1)实验中首先加入的试剂是
(2)试从加入药品的种类、顺序及发生的化学反应等角度来解释气体体积变化的情况。
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】某次实验后,废液缸中残留物由稀硫酸、氢氧化钠、碳酸钠和氯化钡等试剂混合而成。同学们讨论后得到共识:上层溶液中一定含有Na+、Cl-,但对于其他离于还不能确认。为了确定该溶液中所含有的离子,同学们将残留物进行过滤,对滤渣和滤液所做的实验和现象如下:
①取少量滤渣于试管中,滴加足量稀盐酸,有气泡产生;
②取少量滤液于试管中,滴加几滴酚酞试液,滤液变红色;
③取少量滤液于试管中,滴加几滴稀硫酸,有白色沉淀产生;
④取少量滤液于试管中,滴加几滴氯化钡溶液,没有沉淀产生。
请回答下列问题:
(1)仅通过步骤①的实验现象,可以确定该废液缸的液体中一定没有的离子是_______ ;
(2)小组同学讨论后的共识上层溶液中一定含有Na+、Cl-,原因是_______ 。
①取少量滤渣于试管中,滴加足量稀盐酸,有气泡产生;
②取少量滤液于试管中,滴加几滴酚酞试液,滤液变红色;
③取少量滤液于试管中,滴加几滴稀硫酸,有白色沉淀产生;
④取少量滤液于试管中,滴加几滴氯化钡溶液,没有沉淀产生。
请回答下列问题:
(1)仅通过步骤①的实验现象,可以确定该废液缸的液体中一定没有的离子是
(2)小组同学讨论后的共识上层溶液中一定含有Na+、Cl-,原因是
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】图甲是目前流行的某品牌“自热火锅”,图乙是自热火锅结构示意图,图丙为使用说明。
某兴趣小组对这种不用火,不用电,只要加水就能食用的火锅的产生了兴趣。于是他们查阅了相关资料如下:
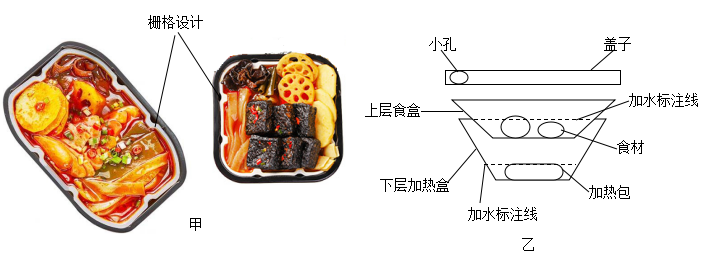
①材料:外盒是采用具有良好耐热性、保温性能的聚丙烯材料制成,餐盒为航空铝箔材料,无污染可再生。带有小孔的盒盖内扣设计,具有良好的密闭功能。
②栅格设计:内外盒之间采用栅格设计,有利于空气流动。
③加热包内含有铁粉、铝粉、焦碳粉、生石灰等物质,其中的金属粉末与碳粉在热水中能发生氧化并缓慢放热。
请结合上述材料和学过的科学知识解释:“自热火锅”能快速加热食材并保温的工作原理。
某兴趣小组对这种不用火,不用电,只要加水就能食用的火锅的产生了兴趣。于是他们查阅了相关资料如下:

| 自热火锅使用方法 1.下层底盒中倒入适量冷水,打开加热包塑料膜,将加热包放入凉水中。 2.放上上层食材盒,倒入一定食用冷水,盖上盖子,15分钟后,即可开盖食用。 丙 |
①材料:外盒是采用具有良好耐热性、保温性能的聚丙烯材料制成,餐盒为航空铝箔材料,无污染可再生。带有小孔的盒盖内扣设计,具有良好的密闭功能。
②栅格设计:内外盒之间采用栅格设计,有利于空气流动。
③加热包内含有铁粉、铝粉、焦碳粉、生石灰等物质,其中的金属粉末与碳粉在热水中能发生氧化并缓慢放热。
请结合上述材料和学过的科学知识解释:“自热火锅”能快速加热食材并保温的工作原理。
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】某同学向一定质量的石灰石中加入7.3%的稀盐酸来制取二氧化碳,测得反应过程中溶液的pH与加入的稀盐酸的关系如图所示。
(1)试求反应生成的二氧化碳质量(石灰石中的杂质不溶于也不溶于酸)_____ ;
(2)该同学把制取气体后的废液过滤,向滤液中加入Na2CO3溶液,测得加入的Na2CO3,溶液质量与产生沉淀质量的有关数据见表格。试分析与计算∶

①表格中m、n的数值分别为_____ 、_____ ;
②加入5gNa2CO3溶液充分反应后,滤液中的溶质有_____ (填化学式);
③加入Na2CO3溶液的溶质质量分数_____ 。
(1)试求反应生成的二氧化碳质量(石灰石中的杂质不溶于也不溶于酸)
(2)该同学把制取气体后的废液过滤,向滤液中加入Na2CO3溶液,测得加入的Na2CO3,溶液质量与产生沉淀质量的有关数据见表格。试分析与计算∶

| Na2CO3溶液质量/g | 5 | 20 | 30 | 40 | 50 | 60 | 70 |
| 沉淀质量/g | 0 | 1 | m | 3 | 4 | 5 | n |
①表格中m、n的数值分别为
②加入5gNa2CO3溶液充分反应后,滤液中的溶质有
③加入Na2CO3溶液的溶质质量分数
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】酸碱盐性质的实验课上,小丽在一支干净的试管内加入2毫升左右的稀盐酸,再滴入2滴Na2CO3溶液,很快产生大量气泡。而同桌的小明则先加入2毫升左右的Na2CO3溶液,再滴入2滴稀盐酸,结果没有看到所预想的气泡;再滴入几滴稀盐酸才产生大量气泡。这是为什么呢?
小丽上网查阅:
Na2CO3与盐酸的反应分两步:第一步:Na2CO3 + HCl = NaHCO3 + NaCl,这一步没有气体产生。第二步:NaHCO3 + HCl =" NaCl" +H2O +CO2↑,这一步才有气体产生。请回答:
(1)写出盐酸和Na2CO3溶液反应的化学方程式: 。
(2)请说出生活中酸碱灭火器的原料用NaHCO3而不用Na2CO3的理由: 。
小丽上网查阅:
Na2CO3与盐酸的反应分两步:第一步:Na2CO3 + HCl = NaHCO3 + NaCl,这一步没有气体产生。第二步:NaHCO3 + HCl =" NaCl" +H2O +CO2↑,这一步才有气体产生。请回答:
(1)写出盐酸和Na2CO3溶液反应的化学方程式: 。
(2)请说出生活中酸碱灭火器的原料用NaHCO3而不用Na2CO3的理由: 。
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐3】某兴趣小组为探究某品牌洁厕灵有效成分(有效成分是 O)的质量分数,进行以下实验:取已潮解且部分变质氢氧化钠固体
O)的质量分数,进行以下实验:取已潮解且部分变质氢氧化钠固体 放入烧杯中,然后又往烧杯中逐滴加入洁厕灵液体,实验过程中的数据记录在如下表中(不考虑反应过程中水分的蒸发和盐酸的挥发等因素)。
放入烧杯中,然后又往烧杯中逐滴加入洁厕灵液体,实验过程中的数据记录在如下表中(不考虑反应过程中水分的蒸发和盐酸的挥发等因素)。
请回答下列问题:
(1)表中m的值为______ 。
(2)该品牌洁厕灵的有效成分质量分数是多少______ ?
(3)未潮解变质前氢氧化钠固体的质量是多少______ ?
 O)的质量分数,进行以下实验:取已潮解且部分变质氢氧化钠固体
O)的质量分数,进行以下实验:取已潮解且部分变质氢氧化钠固体 放入烧杯中,然后又往烧杯中逐滴加入洁厕灵液体,实验过程中的数据记录在如下表中(不考虑反应过程中水分的蒸发和盐酸的挥发等因素)。
放入烧杯中,然后又往烧杯中逐滴加入洁厕灵液体,实验过程中的数据记录在如下表中(不考虑反应过程中水分的蒸发和盐酸的挥发等因素)。| 实验序号 | 1 | 2 | 3 | 4 | 5 |
加入洁厕灵液体的总质量/ | 20 | 40 | 60 | 80 | 100 |
溶液的总质量/ | 30 |  | 69.12 | 88.24 | 107.8 |
(1)表中m的值为
(2)该品牌洁厕灵的有效成分质量分数是多少
(3)未潮解变质前氢氧化钠固体的质量是多少
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】向100克含硫酸和硫酸铜的混合溶液中,分6次加入溶质质量分数为8%的氢氧化钠溶液,加入的氢氧化钠溶液质量与生成沉淀质量关系如下表:
(1)第1次反应后,所得溶液的溶质是______ 。(填化学式)
(2)求原混合溶液中硫酸的溶质质量分数______ ?
(3)分析实验数据,在图中画出产生沉淀质量和加入氢氧化钠溶液质量对应的关系图______ 。
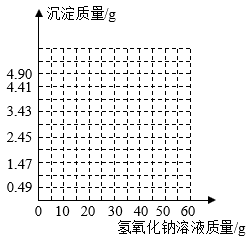
| 次数 | 1 | 2 | 3 | 4 | 5 | 6 |
| 氢氧化钠溶液质量/g | 10 | 20 | 30 | 40 | 50 | 60 |
| 产生沉淀质量/g | 0.49 | 1.47 | 2.45 | 3.43 | 4.41 | 4.90 |
(1)第1次反应后,所得溶液的溶质是
(2)求原混合溶液中硫酸的溶质质量分数
(3)分析实验数据,在图中画出产生沉淀质量和加入氢氧化钠溶液质量对应的关系图

您最近一年使用:0次
解答题
|
适中
(0.65)
名校
【推荐2】 为了测得工业纯碱中碳酸钠的质量分数(纯碱中常含有少量NaCl),小红同学设计了如图实验装置。她的实验步骤为;

(1)准确称取盛有碱石灰的干燥管的质量为158.0g,再准确称取11.0g纯碱样品并全部放入A中;
(2)组装全部反应装置并检查气密性,关闭d;由e逐滴加入稀硫酸至不再产生气泡为止;
(3)打开d,慢慢鼓入空气10min;
(4)再称干燥管的总质量为162.4g,请列式求出该产品中碳酸钠的质量分数。_______

(1)准确称取盛有碱石灰的干燥管的质量为158.0g,再准确称取11.0g纯碱样品并全部放入A中;
(2)组装全部反应装置并检查气密性,关闭d;由e逐滴加入稀硫酸至不再产生气泡为止;
(3)打开d,慢慢鼓入空气10min;
(4)再称干燥管的总质量为162.4g,请列式求出该产品中碳酸钠的质量分数。
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐3】在学习了金属的化学性质后,科学老师布置了一项课外学习任务:调查化工颜料店出售的涂料添加剂“银粉”是什么金属?某学习小组通过调查,分别获得了“银粉”是银粉、铝粉、锌粉这三种不同结果。为了确定究竟是哪一种金属,学习小组同学将一小包“银粉”带回实验室,进行了如下实验和分析。(相关反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑;2Al+3H2SO4=Al2(SO4)3+3H2↑)

(1)取少量“银粉”于试管中,滴加适量盐酸,观察到有________产生,说明“银粉”一定不是银。
(2)为了进一步确定“银粉”是铝还是锌,学习小组通过理论计算,获得两种金属分别与足量盐酸反应产生氢气的质量关系,并绘制成如图所示图像。在绘制锌的图像时,a点所对应的锌的质量m为多少?(通过计算回答)
(3)取1.8g“银粉”(杂质忽略不计)加入50g稀硫酸中,恰好完全反应,生成氢气0.2g。根据图可知,“银粉”是______________。计算实验中所用稀硫酸的溶质质量分数。
(4)上述稀硫酸若用密度为1.84g/cm3,浓度为98%的浓硫酸稀释,则需要多少毫升这样的浓硫酸?

(1)取少量“银粉”于试管中,滴加适量盐酸,观察到有________产生,说明“银粉”一定不是银。
(2)为了进一步确定“银粉”是铝还是锌,学习小组通过理论计算,获得两种金属分别与足量盐酸反应产生氢气的质量关系,并绘制成如图所示图像。在绘制锌的图像时,a点所对应的锌的质量m为多少?(通过计算回答)
(3)取1.8g“银粉”(杂质忽略不计)加入50g稀硫酸中,恰好完全反应,生成氢气0.2g。根据图可知,“银粉”是______________。计算实验中所用稀硫酸的溶质质量分数。
(4)上述稀硫酸若用密度为1.84g/cm3,浓度为98%的浓硫酸稀释,则需要多少毫升这样的浓硫酸?
您最近一年使用:0次




