某同学用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,他决定利用该废液,测定Na2CO3溶液中溶质的质量分数。他将废液过滤,然后向滤液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示。
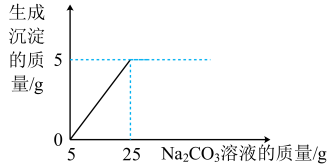
(1)在加入Na2CO3溶液的过程中,开始时没有发现沉淀生成,但却看到溶液有气泡产生,是因为废液中含有_________ (填化学式)。
(2)Na2CO3溶液从0加到5克的过程中,溶液pH________ (填“变大”、“变小”或“不变”)。
(3)计算Na2CO3溶液中溶质的质量分数。

(1)在加入Na2CO3溶液的过程中,开始时没有发现沉淀生成,但却看到溶液有气泡产生,是因为废液中含有
(2)Na2CO3溶液从0加到5克的过程中,溶液pH
(3)计算Na2CO3溶液中溶质的质量分数。
更新时间:2023-12-22 19:44:03
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】如图是配制50克溶质质量分数为8%的氯化钠(NaCl)溶液的有关操作示意图:
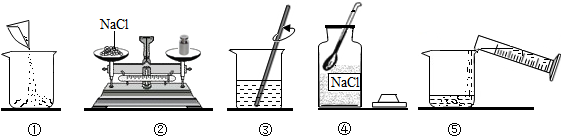
(1)称量时出现了右盘低的现象,接下来的操作应该是:继续向左盘中增加氯化钠,直至天平平衡;
(2)配制氯化钠溶液的正确顺序是____ (用上述图示的序号表示);
(3)③中玻璃棒的作用是____ ;
(4)经检测,所配制的溶液溶质质量分数偏小,其原因可能有____ 。
A.所用氯化钠药品不纯
B.称量时,砝码端忘垫质量相同的纸片
C.量取水时,仰视读数
D.装瓶时,有少量溶液洒出。
E.称量时使用了生锈的砝码

(1)称量时出现了右盘低的现象,接下来的操作应该是:继续向左盘中增加氯化钠,直至天平平衡;
(2)配制氯化钠溶液的正确顺序是
(3)③中玻璃棒的作用是
(4)经检测,所配制的溶液溶质质量分数偏小,其原因可能有
A.所用氯化钠药品不纯
B.称量时,砝码端忘垫质量相同的纸片
C.量取水时,仰视读数
D.装瓶时,有少量溶液洒出。
E.称量时使用了生锈的砝码
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】小明同学在实验室里配制100克溶质的质量分数为6%的氯化钠(NaCl)溶液,实验步骤如下:

(1)正确的实验操作顺序是____ (填序号)。
(2)称量和溶解:小明调节好的托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向右盘(如下图),小明接下来的操作应是____ 。
(3)操作⑤中量筒的量程是____ (选填“10毫升”、“50毫升”和“100毫升”)。
(4)若小明在操作过程中出现了下列情况,则会导致配制的氯化钠溶液的溶质质量分数小于 6%的是____ 。(填序号)
A.先用蒸馏水清洗烧杯,再把称得的氯化钠倒入烧杯中
B.用量筒量取水时,眼睛俯视刻度线
C.若操作①中有部分固体洒落桌面
D.当氯化钠固体全部消失后,继续用玻璃棒搅拌,此时有少量液体溅出

(1)正确的实验操作顺序是
(2)称量和溶解:小明调节好的托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向右盘(如下图),小明接下来的操作应是
(3)操作⑤中量筒的量程是
(4)若小明在操作过程中出现了下列情况,则会导致配制的氯化钠溶液的溶质质量分数
A.先用蒸馏水清洗烧杯,再把称得的氯化钠倒入烧杯中
B.用量筒量取水时,眼睛俯视刻度线
C.若操作①中有部分固体洒落桌面
D.当氯化钠固体全部消失后,继续用玻璃棒搅拌,此时有少量液体溅出
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某同学配制80g15%的NaCl溶液,整个操作过程如图所示。__________ 。
(2)下列操作会导致他所配制的溶液溶质质量分数偏大的有__________ (填字母)。
A.用量筒量取蒸馏水读数时,仰视凹液面的最低处
B.用托盘天平称量氯化钠时,使用的砝码生锈了
C.将量筒中的水倒入烧杯时,量筒中有少量水残余
(3)上述溶液取10g加水40g进行稀释,所得氯化钠溶液的溶质质量分数是__________ 。
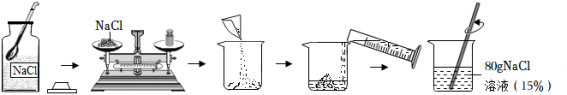
(2)下列操作会导致他所配制的溶液溶质质量分数偏大的有
A.用量筒量取蒸馏水读数时,仰视凹液面的最低处
B.用托盘天平称量氯化钠时,使用的砝码生锈了
C.将量筒中的水倒入烧杯时,量筒中有少量水残余
(3)上述溶液取10g加水40g进行稀释,所得氯化钠溶液的溶质质量分数是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】金属铜和浓硝酸、稀硝酸反应的方程式如下:
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
工业上用铜屑和浓硝酸为原料制取硝酸铜,在实际生产中,需把浓硝酸用等体积水稀释。试简答:
(1)用稀硝酸而不用浓硝酸的原因:________________________
(2)从经济效益和环保角度考虑、设计制取硝酸铜的最适宜方法,用化学方程式表示为:______________________________ ,________________ 。
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
工业上用铜屑和浓硝酸为原料制取硝酸铜,在实际生产中,需把浓硝酸用等体积水稀释。试简答:
(1)用稀硝酸而不用浓硝酸的原因:
(2)从经济效益和环保角度考虑、设计制取硝酸铜的最适宜方法,用化学方程式表示为:
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
【推荐2】小丽利用底部有一小孔的大试管,如图甲所示装配成一个制取CO2气体的装置。
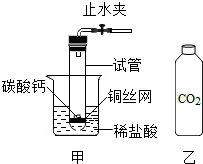
(1)实验前,关闭止水夹,先将试管底部稍浸没在水中,再用双手紧握试管,观察到 ,则说明装置气密性良好;
(2)小丽将CO2通入盛有NaOH溶液的试管中,观察不到明显现象。那么CO2与NaOH是否发生反应?为此又做了实验:在集满CO2的软塑料瓶(如图乙)中加入适量的NaOH溶液,盖紧瓶塞振荡,发现瓶变瘪,于是认为CO2与NaOH发生了反应。小衢提出质疑,认为导致软塑料瓶变瘪的原因还有可能是 ;
(3)小科从变瘪的软塑料瓶中取出少量试液置于试管中,滴入 溶液(填一种盐),观察到有白色沉淀产生,就证明了CO2与NaOH的反应确实已经发生。

(1)实验前,关闭止水夹,先将试管底部稍浸没在水中,再用双手紧握试管,观察到 ,则说明装置气密性良好;
(2)小丽将CO2通入盛有NaOH溶液的试管中,观察不到明显现象。那么CO2与NaOH是否发生反应?为此又做了实验:在集满CO2的软塑料瓶(如图乙)中加入适量的NaOH溶液,盖紧瓶塞振荡,发现瓶变瘪,于是认为CO2与NaOH发生了反应。小衢提出质疑,认为导致软塑料瓶变瘪的原因还有可能是 ;
(3)小科从变瘪的软塑料瓶中取出少量试液置于试管中,滴入 溶液(填一种盐),观察到有白色沉淀产生,就证明了CO2与NaOH的反应确实已经发生。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,称取石灰石样品若干,把200g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余成分不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下:
(1)从以上数据可推知,m=___________ 。
(2)石灰石样品中碳酸钙的质量分数是___________ 。
(3)求稀盐酸中溶质的质量分数___________ (写出计算过程,结果精确到0.1%)。
(1)从以上数据可推知,m=
(2)石灰石样品中碳酸钙的质量分数是
(3)求稀盐酸中溶质的质量分数
实验序号 | 稀盐酸的用量/g | 剩余固体的质量/g |
第一次 | 50 | 10 |
第二次 | 50 | 5 |
第三次 | 50 | 3 |
第四次 | 50 | m |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:
【查得资料】
该牙膏摩擦剂由碳酸钙、氢氧化铝组成:牙膏中其它成分遇到盐酸时无气体产生.
【设计实验】小组同学设计了如图所示装置(图中夹持仪器略去) 测定牙膏样品中碳酸钙的含量.

依据图示回答下列问题:
(1)该装置中氢氧化钠溶液的作用是________________________________ .
(2)实验过程中需持续缓缓通入空气,其作用有_______________________ .
(3)有人认为不必测定C中沉淀的质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数.实验证明按此方法测定的结果明显偏高,原因是_______________________________ .
【查得资料】
该牙膏摩擦剂由碳酸钙、氢氧化铝组成:牙膏中其它成分遇到盐酸时无气体产生.
【设计实验】小组同学设计了如图所示装置(图中夹持仪器略去) 测定牙膏样品中碳酸钙的含量.

依据图示回答下列问题:
(1)该装置中氢氧化钠溶液的作用是
(2)实验过程中需持续缓缓通入空气,其作用有
(3)有人认为不必测定C中沉淀的质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数.实验证明按此方法测定的结果明显偏高,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】金属单质A和非金属单质B可生成化合物A2B,反应的化学方程式为2A+B  A2B.某校一课外小组的甲、乙、丙三个学生分别在实验室内做该实验,充分反应时,所用A和B的质量a和b各不相同,但总质量相等,都是8.0g.有关实验数据记录如下.试求丙学生实验中a:b的值可能是多少?
A2B.某校一课外小组的甲、乙、丙三个学生分别在实验室内做该实验,充分反应时,所用A和B的质量a和b各不相同,但总质量相等,都是8.0g.有关实验数据记录如下.试求丙学生实验中a:b的值可能是多少?___________
 A2B.某校一课外小组的甲、乙、丙三个学生分别在实验室内做该实验,充分反应时,所用A和B的质量a和b各不相同,但总质量相等,都是8.0g.有关实验数据记录如下.试求丙学生实验中a:b的值可能是多少?
A2B.某校一课外小组的甲、乙、丙三个学生分别在实验室内做该实验,充分反应时,所用A和B的质量a和b各不相同,但总质量相等,都是8.0g.有关实验数据记录如下.试求丙学生实验中a:b的值可能是多少?| A的用量 | B的用量 | A2B的质量 | |
| 甲 | 7.0g | 1.0g | 5.0g |
| 乙 | 4.0g | 4.0g | 5.0g |
| 丙 | ag | bg | 3.0g |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】为比较碳酸氢钠片和铝碳酸镁片对治疗胃酸的效果.某兴趣小组同学进行了如下的实验.
(1)利用图一装置,取100毫升pH=1的稀盐酸分别和两种药片反应,化学方程式如下:
①:NaHCO3+HCl=NaCl+CO2↑+H2O
②:Al2Mg6(OH)16CO3·4H2O+18HCl=2_________+6MgCl2+CO2↑+21H2O
请写出化学方程式②中_________ 处物质的化学式.
(2)利用排水法测定产生二氧化碳的体积,则应选择图二中的装置_________ 与图一中的A相连.

(1)利用图一装置,取100毫升pH=1的稀盐酸分别和两种药片反应,化学方程式如下:
①:NaHCO3+HCl=NaCl+CO2↑+H2O
②:Al2Mg6(OH)16CO3·4H2O+18HCl=2_________+6MgCl2+CO2↑+21H2O
请写出化学方程式②中
(2)利用排水法测定产生二氧化碳的体积,则应选择图二中的装置

您最近一年使用:0次




