浙江省绍兴市上虞区2023-2024学年九年级上学期期中科学试卷
浙江
九年级
期中
2023-12-22
48次
整体难度:
容易
考查范围:
常见的物质、科学探究所需要的基本技能、物质的运动与相互作用
一、选择题 添加题型下试题
A. 粮食酿酒 粮食酿酒 | B. 纺纱织布 纺纱织布 |
C. 在甲骨上刻文字 在甲骨上刻文字 | D. 用石块修筑长城 用石块修筑长城 |
【知识点】 化学变化和物理变化的判别
2. 规范的操作是实验成功的基本保证,下列实验操作规范的是( )
A. 过滤 过滤 | B.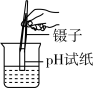 测试溶液pH 测试溶液pH |
C.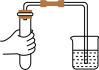 气密性检查 气密性检查 | D.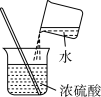 稀释浓硫酸 稀释浓硫酸 |
【知识点】 常见实验操作 浓硫酸的性质及浓硫酸的稀释
| A.Na2CO3(烧碱) | B.NaOH(纯碱) |
| C. Ca(OH)2(石灰石) | D.CaO(生石灰) |
【知识点】 常见物质的俗称
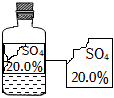
A.其 一定为7 一定为7 | B.不可能是硫酸铜溶液 |
| C.这瓶液体可能是碱 | D.其中一定含有金属元素 |

| A.金属的硬度 | B.金属的耐腐蚀性 |
| C.金属的导电性 | D.金属的延展性 |
【知识点】 金属的物理性质及用途
| A.伽利略的斜面实验中,小球从斜面滚下后能滚上另一个斜面是因为小球具有“能” |
| B.挂在树枝上的苹果没有运动,所以苹果不具有“能” |
| C.人在跑步时要消耗体内的“能” |
| D.向日葵在太阳下不断生长时将太阳光中的“能”储存到体内 |
【知识点】 能量及其存在的不同形式 能量的转化与守恒定律
 )来提高洗涤衣物的效果。下列物质与
)来提高洗涤衣物的效果。下列物质与 溶液一样呈碱性的是( )
溶液一样呈碱性的是( )
| A.稀硫酸 | B.食醋 | C.蒸馏水 | D.碳酸钠溶液 |
【知识点】 溶液的酸碱性与pH值的关系
选项 | 劳动项目 | 科学知识 |
A | 烹饪服务:用小苏打发面,做包子 | 利用碳酸钠分解产生二氧化碳,使面团松软 |
B | 学农活动:用厨余垃圾制肥料 | 厨余垃圾中含有N、P、K等植物所需的元素 |
C | 家务劳动:用白醋去除水壶中的水垢 | 醋酸能与水垢中的CaCO3、MgCO3等物质反应 |
D | 生活妙招:用紫甘蓝制作酸碱指示剂 | 紫甘蓝中的花青素在不同pH环境中显色不同 |
| A.A | B.B | C.C | D.D |
| A.澄清石灰水与碳酸钠溶液 |
| B.澄清石灰水与稀盐酸溶液 |
| C.澄清石灰水与氯化铜溶液 |
| D.澄清石灰水与二氧化碳 |
【知识点】 碱的化学性质
选项 | 物质 | 操作方法 |
A | Fe(Fe2O3) | 加入过量稀盐酸,充分反应后过滤 |
B | CaO 粉末(CaCO3粉末) | 加足量的水,充分搅拌后过滤 |
C | NaOH 溶液(Na2CO3) | 加入氯化钙至恰好不再产生白色沉淀 |
D | CuSO4溶液(硫酸) | 加入过量CuO粉末,充分反应后过滤 |
| A.A | B.B | C.C | D.D |
| A.NaNO3、NaCl、KNO3、CuSO4 |
| B.H2SO4、HCl、AgNO3、Na2SO4 |
| C.KMnO4、CuCl2、Fe2(SO4)3、NaNO3 |
| D.K2SO4、NaCl、K2CO3、NaOH |
【知识点】 盐的性质及用途 离子或物质的共存问题
①C→CO→CO2 ②Al→Al2O3→AlCl3
③Na2CO3→NaCl→NaNO3 ④CaCO3→CaO→Ca(OH)2
| A.①②③ | B.①③④ | C.①②④ | D.①②③④ |
【知识点】 盐的性质及用途 化合物之间的相互转化 金属、金属氧化物、碱之间的转化
| A.因为碱溶液呈碱性,所以呈碱性的溶液一定是碱溶液 |
| B.金属铝与盐酸反应生产AlCl3和H2,所以金属铁与盐酸反应生产FeCl3和H2 |
| C.因为燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件 |
| D.因为蜡烛燃烧生成二氧化碳和水,所以蜡烛中一定含有碳元素和氢元素 |
【知识点】 金属活动性顺序及其应用 碱的化学性质 燃烧的条件 质量守恒定律及其应用
| A.氢氧化钠 | B.浓硫酸 | C.氯化钠 | D.浓盐酸 |
【知识点】 酸的物理性质及用途 碱的化学性质 盐的性质及用途 浓硫酸的性质及浓硫酸的稀释

| A.置换反应 | B.分解反应 |
| C.化合反应 | D.复分解反应 |
| A.向NaOH溶液中滴入酚酞,观察溶液是否变红色 |
| B.向K2CO3的溶液中滴入酚酞,观察溶液是否变红色 |
| C.向Na2CO3的溶液中滴入酚酞后,再加入适量的盐酸,观察红色是否消失 |
| D.向Na2CO3的溶液中滴入酚酞,再加入适量的氢氧化钙,观察红色是否消失 |
【知识点】 盐的性质及用途
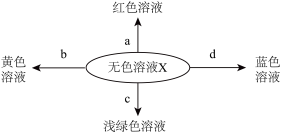
| A.若d是CuO,蓝色溶液中可能有硫酸铜 |
| B.若X是稀硫酸,a可能是紫色石蕊试液 |
| C.若X是稀硫酸,c可能是单质 |
| D.若b是Fe2O3,X一定是稀硫酸 |
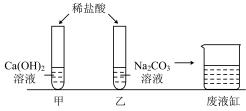
| A.甲实验结束后,试管中的溶液可能含有稀盐酸 |
B.乙实验结束后,试管中的废液一定含有 |
C.最终,废液缸中一定含NaCl、 两种溶质 两种溶质 |
D.最终,废液缸中可能含NaCl、HCl、 三种溶质 三种溶质 |
20. 在溶质为Cu(NO3)2、AgNO3和Al(NO3)3的溶液中加入一定量的锌粉,充分反应后过滤,得到滤渣和蓝色滤液。下列判断正确的是( )
| A.向滤渣中加入稀盐酸可能有气泡产生 |
| B.滤渣中一定有Ag,可能有Cu和Zn |
| C.滤液中一定无AgNO3 |
| D.滤液中可能有四种金属离子 |
【知识点】 金属活动性顺序及其应用 金属的化学性质
二、填空题 添加题型下试题
| 试剂 | 稀盐酸 | 食醋 | 蔗糖水 | 蒸馏水 | 肥皂水 | 石灰水 | 烧碱溶液 |
| 颜色 | 红 | 红 | 黄 | 黄 | 绿 | 绿 | 绿 |
请分析表格,并回答下列问题:
(1)该花汁
(2)蚊子叮咬人时注入蚁酸(具有酸的性质),会使皮肤红肿、痛痒。要缓解这种症状,简易可行的办法是在叮咬处涂抹上述试剂中的
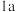 溶液呈蓝色………………………硫酸铜溶液 溶液呈蓝色………………………硫酸铜溶液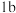 溶液呈无色………………………2 溶液呈无色………………………2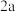 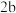 滴加紫色石蕊试液呈蓝色………3 滴加紫色石蕊试液呈蓝色………3 滴加氯化钡溶液有沉淀产生…… 滴加氯化钡溶液有沉淀产生……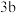 滴加氯化钡溶液无沉淀产生…… 滴加氯化钡溶液无沉淀产生…… |
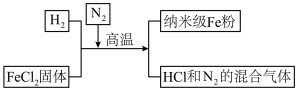
(1)纳米级铁粉在氧气中能自燃并生成一种红色固体,此红色固体的化学式为
(2)上述纳米级铁粉制备工艺的化学方程式为H2+FeCl2
 Fe+2HCl。在制备纳米级铁粉工艺流程中,N2 的作用是
Fe+2HCl。在制备纳米级铁粉工艺流程中,N2 的作用是 (3)研究人员发现最后制得的纳米级铁粉样品中混有少量的FeCl2杂质。为除去样品中的杂质,在无氧环境下,先溶解
(1)性质3是酸溶液与
(2)根据性质5,硫酸可以与下列哪些物质发生反应
A.烧碱溶液
B.纯碱溶液
C.氯化钡溶液
D.食盐溶液
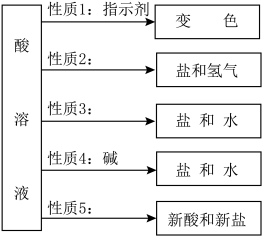
【知识点】 酸的化学性质
(1)铜锌合金的外观与黄金极为相似,市场上有一些不法分子以假乱真,祸害百姓。利用简单的化学知识,将其放入稀盐酸中,观察是否有
(2)铝、铁、银是日常生活中经常接触到的三种金属。对Al、Fe、Ag三种金属的活动性顺序进行探究,能达到目的的一组试剂是
①Ag、FeCl2溶液、AlCl3溶液② Fe、AlCl3溶液、AgNO3溶液 ③ Ag、Fe、AlCl3溶液
【知识点】 金属活动性顺序及其应用

(1)在酸碱反应的实验中,操作如图甲所示,当他观察到红色刚好消失时,写出反应的化学方程式
(2)小黄对一瓶敞口放置的氢氧化钠溶液产生兴趣,他想探究该溶液是否完全变质。于是他做了如图乙所示的一系列实验,其中第一步中就先加入足量未知试液为
【知识点】 碱的化学性质 盐的性质及用途 书写化学方程式、文字表达式
三、探究题 添加题型下试题
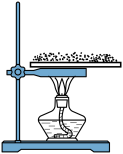
【实验步骤】取一条长为15cm,宽4cm的铁片用砂纸将其打磨干净,水平固定在铁架台上,在铁片上铺成细条状,然后用酒精灯在铁片的一端加热
【实验现象】观察到铁片上残留有黑色固体,并闻到一股刺激性气味。
(1)小组同学选用铁片代替试管,是想利用铁良好的
(2)小组同学取下铁片上的黑色固体,进一步探究该反应是否有新物质生成。小温认为可以用磁铁靠近的方法进行检验,小钟认为小温的方案有缺陷
(3)结合实验现象,请你指出该改进实验中仍存在的不足:
【知识点】 金属的物理性质及用途 金属的化学性质 磁性、磁体、磁极
四、解答题 添加题型下试题
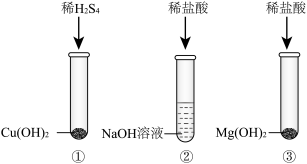
观察到试管①③中共同的明显现象是
【提出问题】试管②中没有明显现象,是否发生了反应?
【实验探究】化学兴趣小组取少量实验后试管②中的溶液,分别放入a、b两支试管中,向a试管中滴入酚酞溶液,观察到了
A.Zn B.Fe(OH)3 C.FeCl3 D.AgNO3
【知识点】 中和反应及其应用
五、探究题 添加题型下试题
实验次数 | 钢球质量m/g | 钢球下摆高度h/cm | 木块滑行距离s/cm |
1 | 20 | 30 | 35 |
2 | 40 | 30 | 65 |
3 | 60 | 30 |
(2)第3次实验时,木块被撞后滑出木板无法记录数据,需要重做第三次实验,甲同学建议换用同样较长的木板,乙同学建议换一个较大的木块,丙同学建议降低钢球下摆的高度,你认为应该采用
(3)由上述实验数据和现象可得出结论
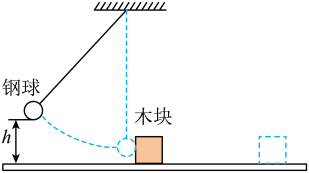
【知识点】 动能的影响因素
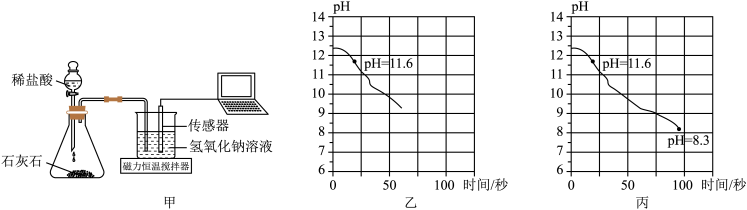
①碳酸钠能与二氧化碳、水反应生成碳酸氢钠
(
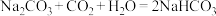 )
)②该温度下,饱和碳酸钠溶液的pH为11.6,饱和碳酸氢钠溶液的pH为8.3;
③该温度下碳酸钠的溶解度大于碳酸氢钠的溶解度。
根据以上现象和信息,小组同学展开进一步探究:
【建立假设】假设1:只有碳酸钠;假设2:碳酸钠、碳酸氢钠:假设3:只有碳酸氢钠;假设4:…
小敏根据图乙曲线判断假设1不成立,理由是
【实验过程】继续通入二氧化碳,溶液的pH随时间变化情况如图丙。
【实验结论】小敏根据图丙曲线认为二氧化碳持续通入氢氧化钠溶液后的最终产物是
【交流评价】
(1)小金认为该曲线还不能确定最终产物。因为pH可能还未呈稳定状态,接下去的操作是
(2)小兴受小金的启发,猜测最后溶液可能呈酸性,他猜想的依据是
【知识点】 二氧化碳的化学性质 碱的化学性质 溶液的酸碱性与pH值的关系
【实验步骤】
①在规格相同的A、B试管中分别放入大小相近、数量相同的锌粒,胶头滴管吸入等量的溶液,如图甲所示。塞紧橡胶塞。
②将两个胶头滴管中的溶液同时挤入试管后,立即开启数据采集器。
③约
 后,停止采集数据。电脑显示气压p随时间t变化的关系如图乙。
后,停止采集数据。电脑显示气压p随时间t变化的关系如图乙。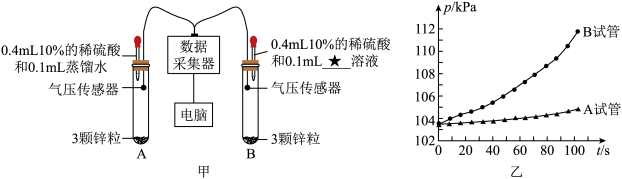
【实验分析】
(1)图甲中“★”处应填
(2)要确保实验成功,实验前应检查反应装置的
(3)实验中,锌和稀硫酸反应的快慢通过采集到的试管内
【实验结论】
在锌和稀硫酸的反应中,加入硫酸铜溶液可以
六、解答题 添加题型下试题

(1)以下四种物品中属于垃圾分类中可回收物的是
A.破碗瓷片
B.过期药物
C.废旧报纸
D.枯枝落叶
(2)易腐垃圾经过处理会产生沼气,沼气可以燃烧发电。沼气的主要成分是甲烷(CH4),请写出甲烷燃烧的化学方程式
(3)废电池属于“有害垃圾”,主要是因为废电池里含有大量的汞、镉、锰、铅等重金属
(4)“可回收物”中包含铝制易拉罐和废弃铁制品,铝的金属活动性比铁强,但为什么铝制品比铁制品更耐腐蚀?
【知识点】 金属的化学性质 书写化学方程式、文字表达式
(1)根据现有的条件,你认为能测出______合金中铜的质量分数。
| A.Cu——Zn合金 | B.Cu—Ag合金 | C.Cu——Zn合金和Cu—Ag合金 |
第一次 | 第二次 | 第三次 | |
连续加入盐酸的体积(ml) | 10 | 10 | 10 |
生成氢气的质量(g) | 0.08 | 0.08 | 0.04 |
【知识点】 金属的化学性质 根据化学反应方程式的计算
七、填空题 添加题型下试题
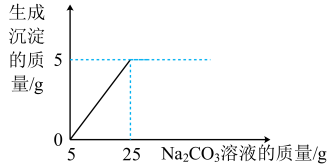
(1)在加入Na2CO3溶液的过程中,开始时没有发现沉淀生成,但却看到溶液有气泡产生,是因为废液中含有
(2)Na2CO3溶液从0加到5克的过程中,溶液pH
(3)计算Na2CO3溶液中溶质的质量分数。
【知识点】 溶质质量分数的简单计算 酸的化学性质 盐的性质及用途 根据化学反应方程式的计算
八、解答题 添加题型下试题
实验次数 | 1 | 2 | 3 | 4 | 5 | 6 |
加入稀盐酸的质量(克) | 20 | 20 | 20 | 20 | 20 | 20 |
电子天平的示数(克) | 120 | 140 | 160 | 179.1 | m | 218.9 |
(1)小科认为:滴加稀盐酸,若氢氧化钠溶液不变质,不会产生二氧化碳,生成的碳酸钠越多,产生的二氧化碳越多;氢氧化钠完全变质,完全反应所需的稀盐酸的质量越大。请判断小科的推测是否正确:
(2)分析表格数据和图像,判断表中m的值为
(3)列式计算该份氢氧化钠样品变质前的质量。

【知识点】 碱的化学性质 盐的性质及用途 根据化学反应方程式的计算
试卷分析
试卷题型(共 36题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 化学变化和物理变化的判别 | |
| 2 | 0.94 | 常见实验操作 浓硫酸的性质及浓硫酸的稀释 | |
| 3 | 0.94 | 合成塑料 合成橡胶 合成纤维 | |
| 4 | 0.94 | 常见物质的俗称 | |
| 5 | 0.85 | 酸的化学性质 盐的性质及用途 | |
| 6 | 0.85 | 金属的物理性质及用途 | |
| 7 | 0.65 | 能量及其存在的不同形式 能量的转化与守恒定律 | |
| 8 | 0.94 | 溶液的酸碱性与pH值的关系 | |
| 9 | 0.85 | 酸的化学性质 盐的性质及用途 盐与化肥 酸碱指示剂及其性质 | |
| 10 | 0.85 | 碱的化学性质 | |
| 11 | 0.65 | 酸的化学性质 盐的性质及用途 物质除杂或净化 | |
| 12 | 0.85 | 盐的性质及用途 离子或物质的共存问题 | |
| 13 | 0.85 | 盐的性质及用途 化合物之间的相互转化 金属、金属氧化物、碱之间的转化 | |
| 14 | 0.85 | 金属活动性顺序及其应用 碱的化学性质 燃烧的条件 质量守恒定律及其应用 | |
| 15 | 0.65 | 酸的物理性质及用途 碱的化学性质 盐的性质及用途 浓硫酸的性质及浓硫酸的稀释 | |
| 16 | 0.85 | 置换反应及其应用 复分解反应及其应用 | |
| 17 | 0.65 | 盐的性质及用途 | |
| 18 | 0.85 | 酸的化学性质 碱的化学性质 | |
| 19 | 0.65 | 酸的化学性质 盐的性质及用途 | |
| 20 | 0.65 | 金属活动性顺序及其应用 金属的化学性质 | |
| 二、填空题 | |||
| 21 | 0.65 | 动能和势能的概念 动能大小的比较 | |
| 22 | 0.85 | 中和反应及其应用 酸碱指示剂及其性质 | |
| 23 | 0.85 | 盐的性质及用途 常见物质的鉴定 | |
| 24 | 0.65 | 金属的化学性质 物质除杂或净化 | |
| 25 | 0.85 | 酸的化学性质 | |
| 26 | 0.65 | 金属活动性顺序及其应用 | |
| 27 | 0.65 | 碱的化学性质 盐的性质及用途 书写化学方程式、文字表达式 | |
| 35 | 0.65 | 溶质质量分数的简单计算 酸的化学性质 盐的性质及用途 根据化学反应方程式的计算 | |
| 三、探究题 | |||
| 28 | 0.4 | 金属的物理性质及用途 金属的化学性质 磁性、磁体、磁极 | |
| 30 | 0.65 | 动能的影响因素 | |
| 31 | 0.65 | 二氧化碳的化学性质 碱的化学性质 溶液的酸碱性与pH值的关系 | |
| 32 | 0.65 | 等效法 控制变量法 金属的化学性质 | |
| 四、解答题 | |||
| 29 | 0.85 | 中和反应及其应用 | |
| 33 | 0.85 | 金属的化学性质 书写化学方程式、文字表达式 | |
| 34 | 0.65 | 金属的化学性质 根据化学反应方程式的计算 | |
| 36 | 0.65 | 碱的化学性质 盐的性质及用途 根据化学反应方程式的计算 | |



