浙江省杭州市弘益中学2023-2024学年九年级上学期10月月考科学试题
浙江
九年级
阶段练习
2023-12-20
52次
整体难度:
适中
考查范围:
常见的物质、科学探究所需要的基本技能、物质的结构、物质的运动与相互作用
一、选择题 添加题型下试题
A. 熄灭酒精灯 熄灭酒精灯 | B.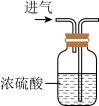 干燥氧气 干燥氧气 |
C.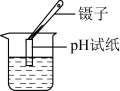 测定某溶液的 测定某溶液的 | D.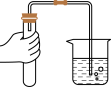 检查气密性 检查气密性 |
【知识点】 常见实验操作 溶液的酸碱性与pH值的关系
| A.氢氧化钙;石灰石;Ca(OH)2 |
| B.碳酸钠;火碱;Na2CO3 |
| C.氧化钙;熟石灰;CaO |
| D.氯化钠;食盐;NaCl |
| A.碱性溶液能使石蕊试液变蓝,所以能使石蕊试液变蓝的溶液呈碱性 |
| B.纯净物是由一种物质组成的,盐酸是一种纯净物 |
| C.酸与碱反应生成盐和水,所以生成盐和水的反应一定是酸与碱的反应 |
| D.铝比铁活泼,所以通常情况下铁的抗腐蚀性能比铝强 |

| A.若X是稀硫酸,则a可能是紫色石蕊试液 |
| B.若X是稀硫酸,则d一定是CuO固体 |
| C.若X是稀盐酸,则c一定是单质 |
| D.若b是Fe2O3,则黄色溶液一定是氯化铁 |
【知识点】 酸的化学性质


| A.①中盛放NaOH溶液的试剂瓶瓶塞甲是玻璃塞 |
| B.③中反应的实质是H+和OH-结合生成水 |
| C.⑤中稀释浓硫酸时,倒入的乙物质是水 |
| D.⑥中酚酞试液用完后,滴管及时清洗 |
【知识点】 中和反应及其应用
| A.Cu、FeCl2溶液、MgCl2溶液 |
| B.Fe、Cu、MgCl2溶液 |
| C.Mg、FeSO4溶液、CuCl2溶液 |
| D.Fe、CuSO4溶液、MgCl2溶液 |
【知识点】 金属活动性顺序及其应用 金属的化学性质
| 选项 | 性质 | 用途 |
| A | 浓硫酸具有脱水性 | 干燥氧气 |
| B | 氢氧化钠呈碱性 | 改良酸性土壤 |
| C | 稀盐酸能与某些金属氧化物反应 | 除铁锈 |
| D | 氢氧化钠能与某些非金属氧化物反应 | 吸收一氧化碳 |
| A.A | B.B | C.C | D.D |


| A.密闭容器反应前后总质量减少 |
B. 时,溶液中溶质为 时,溶液中溶质为 |
C. ,发生的化学反应是: ,发生的化学反应是: |
D. ,温度降低说明反应停止并逐渐冷却,导致压强减小 ,温度降低说明反应停止并逐渐冷却,导致压强减小 |
【知识点】 金属的化学性质
选项 | 实验目的 | 实验方案 |
A | 证明溶液中存在Na2CO3 | 取样,滴加无色酚酞溶液 |
B | 除去溶液中的杂质Na2CO3 | 加入一定量的CaCl2溶液,然后过滤 |
C | 证明溶液部分变质 | 取样,加入过量呈中性的BaCl2溶液,振荡后滴加无色酚酞溶液 |
D | 测溶液的pH | 用玻璃棒蘸取少量溶液滴在湿润的pH试纸上,与标准比色卡对比 |
| A.A | B.B | C.C | D.D |
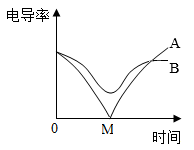
| A.A曲线对应的是乙烧杯溶液导电性 |
| B.A曲线对应的溶液中离子浓度一直在减小 |
| C.B曲线对应的烧杯中溶液始终为红色 |
| D.B曲线对应溶液导电性始终比A曲线对应溶液导电性强 |
| A.NaOH 、NaCl 、 CuSO4 、 HCl |
| B.KNO3 、 Na2SO4 、NaOH 、KCl |
| C.KCl 、Ba(NO3)2 、 HCl 、 CaCl2 |
| D.Na2CO3 、 Ba(OH)2 、KNO3 、Na2SO4 |
【知识点】 盐的性质及用途
| A.镁粉、氧化铜粉、木炭粉 |
| B.NaOH溶液、Ba(OH)2溶液、KOH溶液 |
| C.Na2CO3溶液、NaCl溶液、BaCl2溶液 |
| D.铝片、铁片、银片 |
【知识点】 盐的性质及用途 离子或物质的共存问题 酸、碱、盐的鉴别
| A.同铜片和稀硫酸制取氢气 |
| B.用铁和盐酸制备氯化铁 |
| C.用块状石灰石和硫酸制取二氧化碳 |
| D.用硫酸铜溶液和氢氧化钠溶液制备氢氧化铜 |
| A.CuCl2;AlCl3 | B.ZnCl2;MgCl2 |
| C.Fe2(SO4)3;FeSO4 | D.Na2SO3;K2SO4 |
【知识点】 金属的化学性质
| A.氯化钡 | B.氧化铁 | C.二氧化碳 | D.硫酸铜 |
(1)取该固体粉末少量,加足量水,搅拌,静置,得到沉淀,上层为无色溶液;
(2)过滤,在沉淀中加入少量稀硝酸,沉淀有一部分溶解,且有无色气体产生。依据上述实验对原固体粉末的判断正确的是( )
| A.一定含有碳酸钠,可能含有硫酸钠、硝酸钡、氯化钾,氯化铜 |
| B.一定含有碳酸钠、硫酸钠、硝酸钡,一定不含氯化铜,可能含有氯化钾 |
| C.一定含有碳酸钠、硫酸钠、硝酸钡,可能含有氯化铜,氯化钾 |
| D.一定含有碳酸钠、硝酸钡,一定不含硫酸钠、氯化铜,可能含有氯化钾 |

| A.加入试剂a的顺序可以是过量的NaOH溶液、Na2CO3溶液、BaCl2溶液 |
| B.加入试剂a后,将混合物过滤,得到的沉淀中除泥沙外还含有3种不溶物 |
| C.精盐的质量要比粗盐中NaCl的质量大 |
| D.操作b的名称为过滤 |
【知识点】 粗盐提纯实验
二、填空题 添加题型下试题
【知识点】 常见物质的分类 氧化物、酸、碱和盐的概念
(1)下列物质属于有机物的是
①CO2 ②H2CO3 ③Na2CO3 ④C4H8O2 ⑤C2H5OH ⑥CCl4
(2)天然气的主要用途是作燃料,写出它在空气中充分燃烧的化学方程式
【知识点】 有机物与无机物的区别 书写化学方程式、文字表达式
(1)金属和金属材料在生产生活中有广泛的用途。请回答下列问题:我国自主研制的C919大型客机试飞成功,标志着我国飞机制造技术又有了新的突破。飞机外壳的主要材料是铝合金,“铝合金”属于
(2)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的的是
A.稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉
B.ZnCl2溶液中加入足量铁粉后,再加入CuCl2溶液
C.ZnCl2溶液中加入足量铜粉后,再加入铁粉
(2)根据上述实验结论,下列措施中能有效防止金属锈蚀的是
①金属表面涂抹油漆 ②改变金属的内部结构 ③用湿布擦拭,保持金属表面清洁④在金属表面进行电镀 ⑤使金属表面形成致密的氧化物薄膜
三、探究题 添加题型下试题

(1)仪器A中溶液中的微粒(分子或离子)是
(2)下列说法正确的是
A.图2中b点所示溶液中的溶质是K2SO4和KOH;
B.图2中d点所示溶液中的微粒(分子或离子)是K+、
 、H+;
、H+;C.图2中c→d所示溶液中K2SO4的质量不断增加;
D.图3中e→f变化趋势可说明该反应是放热反应。
(3)丙同学认为氢氧化钾溶液与稀硫酸混合没有明显现象。于是他想借助下列溶液来验证反应是否真的发生,你觉得肯定不可行的是
A.无色酚酞试液 B.氯化钾溶液KCl
C.氯化钡溶液 D.氢氧化镁固体
【知识点】 中和反应及其应用
四、填空题 添加题型下试题

(1)写出向上层清液中滴加NaOH溶液,生成沉淀的化学方程式
(2)图乙中A点对应溶液中一定有的溶质是
五、解答题 添加题型下试题
①取少量滤渣于试管中,滴加足量稀盐酸,有气泡产生;
②取少量滤液于试管中,滴加几滴酚酞试液,滤液变红色;
③取少量滤液于试管中,滴加几滴稀硫酸,有白色沉淀产生;
④取少量滤液于试管中,滴加几滴氯化钡溶液,没有沉淀产生。
请回答下列问题:
(1)仅通过步骤①的实验现象,可以确定该废液缸的液体中一定没有的离子是
(2)小组同学讨论后的共识上层溶液中一定含有Na+、Cl-,原因是
六、探究题 添加题型下试题

(1)首先称取8克该样品放入图装置甲中,然后进行下列实验操作:
①打开弹簧夹,通入足量的氮气,关闭弹簧夹;
②称量装置丙的质量m1;
③打开分液漏斗的活塞,注入足量的稀硫酸,关闭活塞;
④打开弹簧夹,通入足量的氮气,关闭弹簧夹;
⑤称量装置丙的质量m2。
(2)装置丁在这里的作用是
【知识点】 碱的化学性质 盐的性质及用途 浓硫酸的性质及浓硫酸的稀释

反应时间(秒) | 20 | 40 | 60 | 80 | 100 | 120 | 140 | |
收集到的气体体积(毫升) | 甲金属 | 25 | 60 | 95 | 130 | 160 | 170 | 170 |
乙金属 | 30 | 75 | 120 | 150 | 150 | 150 | 150 | |
(2)为使得到的实验数据准确,小吴开始收集气体的时间点应该是
A.导管口一有气泡冒出时 B.冒出气泡连续且均匀时 C.检验产生的气体纯净时
(3)根据已有实验数据,要比较甲、乙两种金属的相对原子质量大小,需要计算气体的质量还要查找的物理量是
【知识点】 金属的化学性质
七、解答题 添加题型下试题
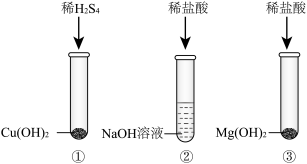
观察到试管①③中共同的明显现象是
【提出问题】试管②中没有明显现象,是否发生了反应?
【实验探究】化学兴趣小组取少量实验后试管②中的溶液,分别放入a、b两支试管中,向a试管中滴入酚酞溶液,观察到了
A.Zn B.Fe(OH)3 C.FeCl3 D.AgNO3
【知识点】 中和反应及其应用
八、探究题 添加题型下试题
 Na2SO4+2HCl↑,随着反应的持续进行,浓硫酸的浓度不断下降。已知氯化氢气体极易溶于水,密度比空气大。如图是实验制取气体的两种常见发生装置。
Na2SO4+2HCl↑,随着反应的持续进行,浓硫酸的浓度不断下降。已知氯化氢气体极易溶于水,密度比空气大。如图是实验制取气体的两种常见发生装置。
(1)写出标注的仪器名称,c为
(2)根据提供的信息,实验室制取HCl气体应选择的发生装置为
(3)将反应剩余物加适量水稀释,得到反应物稀释液。
①假设在现有“强热”条件下,生成的HCl以气体形式全部逸出,则在反应物稀释液中滴加石蕊试液,试液
②为了证明反应剩余物中是否含有Cl-,现取少量反应物稀释液于试管,滴加
九、解答题 添加题型下试题

(1)由图1、2实验可知,硫酸铵与氢氧化钙、氢氧化钠混合研磨或加热,都能放出刺激性气味的气体,图2中湿润的红色石蕊试纸变为
(2)图2中硫酸铵与氢氧化钠反应的化学方程式为
(3)图3中无水硫酸铜变蓝,说明碳酸氢铵分解有
【知识点】 盐的性质及用途
十、探究题 添加题型下试题
①将250ml,碳酸饮料放入冰箱冷藏。在较低温下操作,能避免CO2逸出;
②从冰箱内取出,迅速加入NaOH溶液5mL,倒转瓶轻轻振荡,然后放置恢复至室温,作待测液;
③如图连接装置。取40mL待测液置于装置B的锥形瓶中,关闭开关K,打开漏斗活塞,向锥形瓶中注入稀硫酸,至不再产生气泡,关闭漏斗活塞;

④打开______,向装置中鼓入空气,一段时间后,将C装置中的物质过滤,洗涤,烘干称量质量为0.197g。
结合资料,根据以上实验过程完成下列问题:
| 资料: ①CO2与足量Ba(OH)2反应生成BaCO3沉淀 ②碱石灰是CaO与NaOH的固体混合物 ③实验中各种溶液的密度都视为1g/mL |
(2)根据题中提供的数据计算此品牌碳酸饮料中CO2的含量为
(3)根据实验数据计算发现:CO2含量的测量结果较国家标准低。造成这一实验结果的原因可能是
A.碳酸饮料放入冰箱冷藏时间过短 B.装置气密性不好 C.步骤④中洗涤不干净
【知识点】 二氧化碳的化学性质 碱的化学性质 根据化学反应方程式的计算
十一、解答题 添加题型下试题
(1)根据现有的条件,你认为能测出______合金中铜的质量分数。
| A.Cu——Zn合金 | B.Cu—Ag合金 | C.Cu——Zn合金和Cu—Ag合金 |
第一次 | 第二次 | 第三次 | |
连续加入盐酸的体积(ml) | 10 | 10 | 10 |
生成氢气的质量(g) | 0.08 | 0.08 | 0.04 |
【知识点】 金属的化学性质 根据化学反应方程式的计算
(1)工作时,“反应锅”内不断搅拌的目的是
(2)现有100吨含盐酸质量分数为1.46%的废水,理论上最多可生产氯化钙多少吨

【知识点】 溶质质量分数的简单计算
(1)图中ab段所对应的反应的化学方程式
(2)图中d点对应溶液中的溶质是
(3)计算图中bc段溶液增加的质量为多少克

【知识点】 盐的性质及用途 根据化学反应方程式的计算
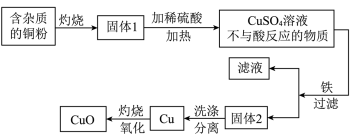
(1)铜粉灼烧后可能有氧化铜和氧化亚铜两种物质。氧化亚铜(Cu2O)中铜元素的化合价是
(2)已知氧化亚铜和稀硫酸反应可生成硫酸铜和铜,假如固体1中只含有铜的氧化物,下列推理合理的是
①固体1中加入稀硫酸,若溶液呈蓝色,说明该固体中一定有氧化铜
②固体1中加入稀硫酸,若有红色沉淀物,说明该固体中一定有氧化亚铜
(3)将得到的1.6吨氧化铜全部转化为硫酸铜;可得硫酸铜多少吨?
【知识点】 酸的化学性质 有关元素化合价的计算 根据化学反应方程式的计算
十二、填空题 添加题型下试题
(1)合金材料的研发:
①合金的很多性能与组成它们的纯金属不同。图1能表示锡铅合金的是
②镁合金被誉为“21世纪绿色金属结构材料”Mg17Al12是一种特殊的镁合金。该合金是一种储氢材料,完全吸氢后得到MgH2和Al,“储氢过程”属于
(2)CO2的绿色利用:
①目前空间站处理CO2的一种方法是在催化剂作用下,利用H2使CO2转化为甲烷并得到生活用水。该反应的化学方程式为
②以“铁氧化物”为催化剂,利用太阳能将CO2热解为碳和氧气,这一转化过程(如图2)中化合价升高的非金属元素是

【知识点】 合金与合金的性质 书写化学方程式、文字表达式
试卷分析
试卷题型(共 37题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 盐与化肥 | |
| 2 | 0.94 | 常见实验操作 溶液的酸碱性与pH值的关系 | |
| 3 | 0.94 | 碱的化学性质 盐的性质及用途 | |
| 4 | 0.85 | 模型与符号 置换反应及其应用 | |
| 5 | 0.85 | 金属的化学性质 碱的化学性质 中和反应及其应用 | |
| 6 | 0.85 | 酸的化学性质 | |
| 7 | 0.65 | 中和反应及其应用 | |
| 8 | 0.85 | 金属活动性顺序及其应用 金属的化学性质 | |
| 9 | 0.65 | 酸的化学性质 碱的化学性质 | |
| 10 | 0.65 | 金属的化学性质 | |
| 11 | 0.85 | 盐的性质及用途 常见物质的鉴定 | |
| 12 | 0.65 | 碱的化学性质 盐的性质及用途 | |
| 13 | 0.85 | 盐的性质及用途 | |
| 14 | 0.65 | 盐的性质及用途 离子或物质的共存问题 酸、碱、盐的鉴别 | |
| 15 | 0.65 | 物质除杂或净化 | |
| 16 | 0.94 | 金属的化学性质 盐的性质及用途 | |
| 17 | 0.94 | 金属的化学性质 | |
| 18 | 0.85 | 碱的化学性质 盐的性质及用途 | |
| 19 | 0.85 | 盐的性质及用途 物质的推断 | |
| 20 | 0.65 | 粗盐提纯实验 | |
| 二、填空题 | |||
| 21 | 0.85 | 常见物质的分类 氧化物、酸、碱和盐的概念 | |
| 22 | 0.94 | 有机物与无机物的区别 书写化学方程式、文字表达式 | |
| 23 | 0.65 | 金属锈蚀的条件及其防护 金属活动性顺序及其应用 金属的化学性质 合金与合金的性质 | |
| 25 | 0.65 | 酸的化学性质 碱的化学性质 盐的性质及用途 | |
| 37 | 0.85 | 合金与合金的性质 书写化学方程式、文字表达式 | |
| 三、探究题 | |||
| 24 | 0.85 | 中和反应及其应用 | |
| 27 | 0.85 | 碱的化学性质 盐的性质及用途 浓硫酸的性质及浓硫酸的稀释 | |
| 28 | 0.85 | 金属的化学性质 | |
| 30 | 0.65 | 常用气体的发生装置和收集装置与选取方法 酸的化学性质 盐的性质及用途 常见物质的鉴定 | |
| 32 | 0.85 | 二氧化碳的化学性质 碱的化学性质 根据化学反应方程式的计算 | |
| 四、解答题 | |||
| 26 | 0.65 | 碱的化学性质 盐的性质及用途 常见物质的鉴定 | |
| 29 | 0.85 | 中和反应及其应用 | |
| 31 | 0.85 | 盐的性质及用途 | |
| 33 | 0.65 | 金属的化学性质 根据化学反应方程式的计算 | |
| 34 | 0.85 | 溶质质量分数的简单计算 | |
| 35 | 0.65 | 盐的性质及用途 根据化学反应方程式的计算 | |
| 36 | 0.65 | 酸的化学性质 有关元素化合价的计算 根据化学反应方程式的计算 | |








