如图,某固体氧化物X,经过如图①②两步反应后,得到红色固体单质C,溶液B只含一种溶质,且是盐,试回答:
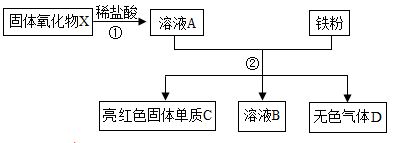
(1)固体氧化物X的化学式是___________
(2)第①步加的盐酸是否过量?________ (填“是”或“否”)
(3)图示过程中,总共发生了几个化学反应__________

(1)固体氧化物X的化学式是
(2)第①步加的盐酸是否过量?
(3)图示过程中,总共发生了几个化学反应
更新时间:2018-11-11 00:40:18
|
相似题推荐
解答题
|
较难
(0.4)
【推荐1】某学习小组用如图所示装置测定锌铜合金中锌、铜的质量分数。

(1)实验前,先将锌铜合金在稀酸中浸泡片刻,其目的是:___________;
(2)实验操作步骤有:检查气密性,将药品和水装入各仪器中,连接好装置后,再进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥、称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B滴加足量试剂;⑤检查气密性。上述再进行的操作的顺序是 (填序号);记录C的液面位置使D和C的液面相平
(3)B中发生反应的化学方程式为: ↑
(4)若实验用锌铜合金的质量为ag,与酸充分反应后,测得氢气体积为VL,为求出合金中锌、铜的质量分数,还缺少的一个数据是 。
(5)若实验用锌铜合金的质量为ag,与酸充分反应后,B中剩余固体的质量为bg,则锌的质量分数为 ;
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得锌的质量分数将 (填“偏大”“偏小”或“不受影响”)。

(1)实验前,先将锌铜合金在稀酸中浸泡片刻,其目的是:___________;
(2)实验操作步骤有:检查气密性,将药品和水装入各仪器中,连接好装置后,再进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥、称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B滴加足量试剂;⑤检查气密性。上述再进行的操作的顺序是 (填序号);记录C的液面位置使D和C的液面相平
(3)B中发生反应的化学方程式为: ↑
(4)若实验用锌铜合金的质量为ag,与酸充分反应后,测得氢气体积为VL,为求出合金中锌、铜的质量分数,还缺少的一个数据是 。
| A.反应前加入稀酸的体积 |
| B.反应前加入稀酸的质量分数 |
| C.实验前反应装置中空气的体积 |
| D.实验条件下氢气的密度 |
(5)若实验用锌铜合金的质量为ag,与酸充分反应后,B中剩余固体的质量为bg,则锌的质量分数为 ;
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得锌的质量分数将 (填“偏大”“偏小”或“不受影响”)。
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】某化学小组同学按下图所示装置和表中所给试剂进行实验(图中铁架台等夹持仪器均已略去):

(1)在试管I中加入试剂后,塞紧橡皮塞,关闭止水夹a,打开止水夹b,试管II中液面上升,溶液变浑浊。符合以上实验现象的试剂是_____ 组,此时II中发生反应的化学方程式为_____ 。
(2)在试管I中加入试剂后,塞紧橡皮塞,立即打开止水夹a,关闭止水夹b,II中有气泡冒出,溶液变浑浊。符合以上实验现象的试剂是_____ 组。

| 组别 | A组 | B组 | C组 | D组 |
| 试管I |  稀  |  稀  |  稀  |  稀  |
| 试管Ⅱ |  溶液 溶液 |  溶液 溶液 |  溶液 溶液 |  溶液 溶液 |
(1)在试管I中加入试剂后,塞紧橡皮塞,关闭止水夹a,打开止水夹b,试管II中液面上升,溶液变浑浊。符合以上实验现象的试剂是
(2)在试管I中加入试剂后,塞紧橡皮塞,立即打开止水夹a,关闭止水夹b,II中有气泡冒出,溶液变浑浊。符合以上实验现象的试剂是
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐3】某校化学实验室废油桶中收集了溶有大量FeSO4、CuSO4的废液,此外还有一些不溶性杂质。若废液直接排放到下水道不仅造成重金属污染,而且造成浪费。该校化学兴趣小组同学设计了如下图处理方案,请回答有关问题。

(1)废液在加入金属X前需进行过滤,目的是将其中的不溶性杂质除去。进行过滤操作所需的玻璃仪器有_______ (3种);
(2)金属X是铁(或Fe),其加入废液后发生反应的化学方程式为_______ ;溶液Y是稀硫酸(或稀H2SO4),利用其除去铜中杂质,有关反应的化学方程式为_______ 。

(1)废液在加入金属X前需进行过滤,目的是将其中的不溶性杂质除去。进行过滤操作所需的玻璃仪器有
(2)金属X是铁(或Fe),其加入废液后发生反应的化学方程式为
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】为了测定某陨石中铁的含量,某化学兴趣小组的同学进行了以下实验:取四份相同质量的样品分别放入等质量的烧杯中,然后分别加入稀硫酸,充分反应后用天平称量杂质不与稀硫酸反应产生气体)几次试验数据如下,请回答下列问题并计算
(1)在第1次实验结束后,反应物_____ 完全反应完了
(2)50.0g样品与足量稀硫酸反应最多能生成气体_______ g
(3)计算陨石中铁的质量分数(写出具体计算过程)。______________
试验次序 | 第1次 | 第2次 | 第3次 | 第4次 |
所取样品的质量/g | 50.0 | 50.0 | 50.0 | 50.0 |
加入稀硫酸的质量/g | 20.0 | 40.0 | 60.0 | 80.0 |
生成气体的质量/g | 0.2 | 0.4 | 0.5 | 0.5 |
(1)在第1次实验结束后,反应物
(2)50.0g样品与足量稀硫酸反应最多能生成气体
(3)计算陨石中铁的质量分数(写出具体计算过程)。
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】电导率传感器,是在实验室、工业生产和探测领域里被用来测量超纯水、纯水、饮用水、污水等各种溶液的电导性或水标本整体离子的浓度的传感器,电导率的数值越大,溶液的导电性越强;电导率的数值越小,溶液的导电性越弱. (电导率的单位是us/cm)老师利用电导率传感仪在实验室完成了两个实验.
实验一:稀氢氧化钡溶液中逐滴滴加稀硫酸,测定溶液电导率的变化,所得图象如图1所示;
实验二:稀氢氧化钠溶液中逐滴滴加稀盐酸,测定溶液电导率的变化,所得图象如图2所示.
观察图象回答下列问题

(1)2组实验开始前的空白对照实验中测得水的电导率为0.82us/cm,说明水________ (填“有”或“无”)微弱的导电性。
(2)写出实验1中反应的化学方程式________ 。请观察图1中的A点,此时烧杯内物质的电导率________ (填写“>”、“<”或“=”)水的电导率,该现象说明了________ 。
(3)观察图2,0~100s时间内,溶液中自由移动的离子数目________ (填“增加”、“减少”或“不变”),溶液的电导率________ (填“增加”、“减少”或“不变”)减少,据此说明溶液的电导率与________ 有关。
实验一:稀氢氧化钡溶液中逐滴滴加稀硫酸,测定溶液电导率的变化,所得图象如图1所示;
实验二:稀氢氧化钠溶液中逐滴滴加稀盐酸,测定溶液电导率的变化,所得图象如图2所示.
观察图象回答下列问题

(1)2组实验开始前的空白对照实验中测得水的电导率为0.82us/cm,说明水
(2)写出实验1中反应的化学方程式
(3)观察图2,0~100s时间内,溶液中自由移动的离子数目
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】A、B、C、D、E、F、G七种物质都是日常生活和生产中常见的物质,各物质间存在如下转化关系(反应的条件已省略):
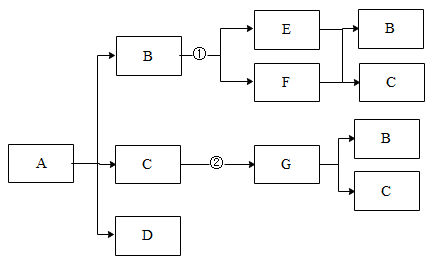
已知:B、C两种物质在不同情况下可分别发生①和②两个反应;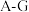 七种物质都是由非金属元素组成的,其中只有一种物质是盐,一种物质是单质;且B的相对分子质量大于C。
七种物质都是由非金属元素组成的,其中只有一种物质是盐,一种物质是单质;且B的相对分子质量大于C。
(1)请写出下列物质的化学式:A________ ;G________ 。
(2)请写出 的化学方程式:
的化学方程式:________________________ 。
(3)D是一种刺激性气味的气体,将其通入B、C的混合物中可以转化为A,写出反应的化学方程式________________________ 。

已知:B、C两种物质在不同情况下可分别发生①和②两个反应;
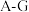 七种物质都是由非金属元素组成的,其中只有一种物质是盐,一种物质是单质;且B的相对分子质量大于C。
七种物质都是由非金属元素组成的,其中只有一种物质是盐,一种物质是单质;且B的相对分子质量大于C。(1)请写出下列物质的化学式:A
(2)请写出
 的化学方程式:
的化学方程式:(3)D是一种刺激性气味的气体,将其通入B、C的混合物中可以转化为A,写出反应的化学方程式
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】图甲中A是一种常见的酸,它能与黑色固体B反应,B质量为8克,将NaOH溶液渐渐加入C中,生成蓝色沉淀E的质量与加入NaOH溶液的质量关系如图乙所示,在D中加入Ba(NO3)2溶液能生成一种不溶于稀硝酸的白色沉淀。
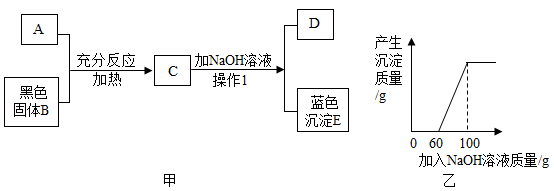
(1)A溶液中溶质的化学式为_________ ;
(2)操作1的名称是_____ ;
(3)NaOH溶液中溶质的质量分数是多少?____________________

(1)A溶液中溶质的化学式为
(2)操作1的名称是
(3)NaOH溶液中溶质的质量分数是多少?
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】小金以化合价为纵坐标、以物质类别为横坐标绘制了如图所示的图像,每种物质中都有一种元素的化合价与纵坐标的数值对应,图中字母均表示初中科学中的常见物质, 其中“→”表示物质间的转化关系。已知 A 中氧元素的质量分数为 60%,C、D、E、F 均含有铜元素。请回答:

(1)“A+H2O=B”的反应属于基本反应类型中的____ ;
(2)写出C与一种物质反应得到D的化学方程式为________ ;

(1)“A+H2O=B”的反应属于基本反应类型中的
(2)写出C与一种物质反应得到D的化学方程式为
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】有一包白色粉末,可能是由Na2CO3、Na2SO4、CuSO4、BaCl2 、NaCl中的一种或几种组成,现做如下实验。
Ⅰ:将少量粉末放在烧杯中加足量水,搅拌、静置、过滤,得无色溶液及白色沉淀;
Ⅱ:向Ⅰ过滤得到的白色沉淀中加足量稀盐酸,沉淀部分溶解并有气体产生;
Ⅲ:向Ⅱ过滤得到的滤液中滴加硝酸银溶液,立即有较多的白色沉淀生成,再加稀硝酸,沉淀不溶解。根据以上实验现象推断白色粉末中:
(1)一定存在的物质是________ ;
(2)可能存在的物质是________ ;若步骤(Ⅱ)改用稀硝酸,________ (选填“可以”、“还是不能”)确定该物质的存在。
Ⅰ:将少量粉末放在烧杯中加足量水,搅拌、静置、过滤,得无色溶液及白色沉淀;
Ⅱ:向Ⅰ过滤得到的白色沉淀中加足量稀盐酸,沉淀部分溶解并有气体产生;
Ⅲ:向Ⅱ过滤得到的滤液中滴加硝酸银溶液,立即有较多的白色沉淀生成,再加稀硝酸,沉淀不溶解。根据以上实验现象推断白色粉末中:
(1)一定存在的物质是
(2)可能存在的物质是
您最近一年使用:0次




