如图是实验室用“W”形玻璃管进行的微型实验。
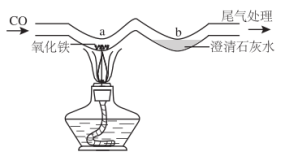
(1)“a”处发生的化学反应中,氧化铁是_____ 。(选填“氧化剂”或“还原剂”)
(2)“b”处发生化学反应的化学方程式:_____ 。
(3)该实验中尾气处理的方法是_____ 。

(1)“a”处发生的化学反应中,氧化铁是
(2)“b”处发生化学反应的化学方程式:
(3)该实验中尾气处理的方法是
更新时间:2019/11/19 17:25:01
|
相似题推荐
填空题
|
较易
(0.85)
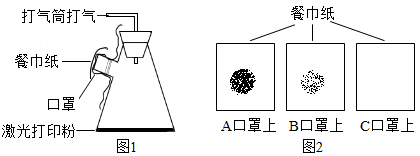
【推荐1】戴口罩是防止雾霾颗粒物进入人体的一种有效措施,市场上口罩品种繁多。为探究口罩防护功能,小敏在三只如左图所示瓶内装少量激光打印粉,将A,B,C三种口罩分别在瓶口系紧,外面覆盖一张餐中纸,通过打气筒打气,使粉末飞扬,实验结果如右图,则防护功能最好的口罩为________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某气体由氢气、一氧化碳、水蒸气中的一种或几种组成.把该气体依次通过下列装置后,测得装有浓硫酸的装置质量增加,装有氢氧化钠溶液的装置质量不变.

(1)该气体一定不存在_____ 。
(2)若实验中观察到_____ 现象,就可证明原气体中存在氢气。

(1)该气体一定不存在
(2)若实验中观察到
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】鸡蛋腐败时会产生一种无色、有臭鸡蛋味的硫化氢(H2S)气体,它是一种大气污染物,在空气中点燃完全燃烧时,生成SO2和水,把H2S通入浓硫酸中,发生的反应为:H2S+H2SO4(浓)=SO2↑+X +2H2O
(1)上述内容中,属于H2S物理性质的是_________________________________ 。
(2)写出H2S在空气中完全燃烧的化学方程式_____________________________ 。
(3)H2S与H2SO4(浓)反应时,生成物中X的化学式是___________________ 。
(4)若尾气中含有H2S,为什么不能用浓H2SO4来吸收?___________________ 。
(1)上述内容中,属于H2S物理性质的是
(2)写出H2S在空气中完全燃烧的化学方程式
(3)H2S与H2SO4(浓)反应时,生成物中X的化学式是
(4)若尾气中含有H2S,为什么不能用浓H2SO4来吸收?
您最近一年使用:0次
填空题
|
较易
(0.85)
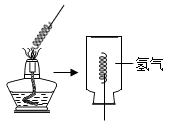
【推荐1】小明利用如图的实验装置开展氢气还原氧化铜的实验。________ 。
(2)氢气还原氧化铜的本质是氢气夺取氧化铜中的氧生成水。如果与氢气反应前、后铜丝的质量分别为m1和m2,则参加反应的氢气质量为________ 。
(2)氢气还原氧化铜的本质是氢气夺取氧化铜中的氧生成水。如果与氢气反应前、后铜丝的质量分别为m1和m2,则参加反应的氢气质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】九年级在进行《从自然界中的铜到纪念币中的铜》项目化学习。探究课上,同学们进行了湿法炼铜和火法炼铜两种方案,如下:
方案一:湿法炼铜。____________ 。
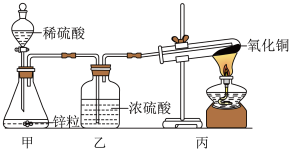
如图所示为氢气还原氧化铜的装置,甲中锥形瓶内装有锌粒,分液漏斗里装有稀硫酸,丙中试管底部黑色固体为氧化铜。____________ 。
A.先打开甲处分液漏斗活塞
B.先点燃丙处的酒精灯
(4)不能用丙图的装置进行CO还原氧化铜的实验,理由是____________ 。
方案一:湿法炼铜。
原理: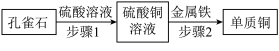
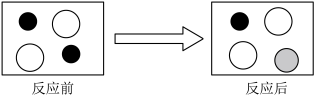
(2)若步骤2前后溶液中存在的离子种类如图所示,其中“ ”“
”“ ”“
”“ ”表示不同种类的离子,则“
”表示不同种类的离子,则“ ”表示
”表示
如图所示为氢气还原氧化铜的装置,甲中锥形瓶内装有锌粒,分液漏斗里装有稀硫酸,丙中试管底部黑色固体为氧化铜。
A.先打开甲处分液漏斗活塞
B.先点燃丙处的酒精灯
(4)不能用丙图的装置进行CO还原氧化铜的实验,理由是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】在工业上,精炼铜、镀铜以及制取各种铜的化合物时,常用到硫酸铜。某工厂用硫化铜(CuS)生产硫酸铜,提出了以下两个生产方案:
方案Ⅰ:硫化铜在硫杆菌的作用下跟空气中的氧气发生反应生成硫酸铜,反应方程式为:CuS+2O2 CuSO4;
CuSO4;
方案Ⅱ:高温煅烧硫化铜,生成氧化铜,反应方程式为:2CuS+3O2 2CuO+2SO2 , 氧化铜跟硫酸反应生成硫酸铜。根据上述信息,请你回答:
2CuO+2SO2 , 氧化铜跟硫酸反应生成硫酸铜。根据上述信息,请你回答:
(1)在方案I所发生的化学反应中,硫杆菌起________ 作用;
(2)上述两个方案中,哪个更合理?________ ,理由是(写出两点)________ 。
方案Ⅰ:硫化铜在硫杆菌的作用下跟空气中的氧气发生反应生成硫酸铜,反应方程式为:CuS+2O2
 CuSO4;
CuSO4;方案Ⅱ:高温煅烧硫化铜,生成氧化铜,反应方程式为:2CuS+3O2
 2CuO+2SO2 , 氧化铜跟硫酸反应生成硫酸铜。根据上述信息,请你回答:
2CuO+2SO2 , 氧化铜跟硫酸反应生成硫酸铜。根据上述信息,请你回答:(1)在方案I所发生的化学反应中,硫杆菌起
(2)上述两个方案中,哪个更合理?
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】金属钛( )的硬度大、熔点高、常温下耐酸碱腐蚀,是航海、医疗等不可缺少的材料。钛铁矿(主要成分
)的硬度大、熔点高、常温下耐酸碱腐蚀,是航海、医疗等不可缺少的材料。钛铁矿(主要成分 )是工业冶炼金属钛的主要原料,制备金属钛的工艺流程如图所示。
)是工业冶炼金属钛的主要原料,制备金属钛的工艺流程如图所示。
(1) 的物理性质有
的物理性质有___________ (任意写一点)
(2)②的反应方程式为 从氧化还原角度,这个反应体现了
从氧化还原角度,这个反应体现了 的
的___________ 性
(3)③中制取金属钛的化学反应的基本类型是___________ 。
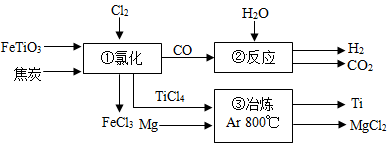
 )的硬度大、熔点高、常温下耐酸碱腐蚀,是航海、医疗等不可缺少的材料。钛铁矿(主要成分
)的硬度大、熔点高、常温下耐酸碱腐蚀,是航海、医疗等不可缺少的材料。钛铁矿(主要成分 )是工业冶炼金属钛的主要原料,制备金属钛的工艺流程如图所示。
)是工业冶炼金属钛的主要原料,制备金属钛的工艺流程如图所示。(1)
 的物理性质有
的物理性质有(2)②的反应方程式为
 从氧化还原角度,这个反应体现了
从氧化还原角度,这个反应体现了 的
的(3)③中制取金属钛的化学反应的基本类型是

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】水煤气厂生产煤气,将水加热成蒸气,通过炽热的炭,得到氢气和一氧化碳。沈老师为了说明其化学原理,画出了卡通图片,其中B表示________ ;A作________ 剂。

您最近一年使用:0次