2021年福建省福州市中考三模(专题突破篇)化学试题
福建
九年级
模拟预测
2021-10-14
289次
整体难度:
适中
考查范围:
身边的化学物质、物质的化学变化、化学实验、物质构成的奥秘
2021年福建省福州市中考三模(专题突破篇)化学试题
福建
九年级
模拟预测
2021-10-14
289次
整体难度:
适中
考查范围:
身边的化学物质、物质的化学变化、化学实验、物质构成的奥秘
一、选择题 添加题型下试题
选择题-单选题
|
适中(0.65)
名校
1. 向一定量的铁粉中逐滴加入稀硫酸至过量,该图是反应过程中某种物质的质量Y随加入稀硫酸的质量变化的关系,则Y不可能表示( )。
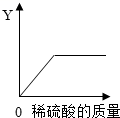

| A.消耗铁粉的质量 |
| B.生成硫酸亚铁的质量 |
| C.溶液的总质量 |
| D.生成氢气的质量 |
您最近一年使用:0次
2016-11-28更新
|
378次组卷
|
16卷引用:2011-2012学年广西南宁三中中考模拟测试化学试卷(十)
(已下线)2011-2012学年广西南宁三中中考模拟测试化学试卷(十)2016届重庆市南开中学九年级下学期段考化学试卷2016届江西省崇仁县九年级下第一次模拟测试化学试卷沪科版(遵义专版)2018届九年级化学:第5章测试卷黑龙江省肇源县第四中学2018届九年级上学期期末化学试题【全国市级联考】山东省枣庄市2018年中考化学二模化学试题四川省成都外国语学校2019届九年级下学期中考一诊化学试题湖北恩施白果初中2018年-2019年上学期九年级4月月考化学试题河南省洛阳市偃师市2018-2019学年九年级上学期期末化学试题(已下线)【万唯原创】2015年山西省中考化学黑白卷-白卷河北省唐山市滦南县宋道口初中2020-2021学年九年级上学期第二次月考化学试题福建省厦门市思明区湖滨中学2020-2021学年九年级下学期期中化学试题四川省成都市金牛区成都外国语学校2018-2019学年九年级下学期入学考试化学试题2021年福建省福州市中考三模(专题突破篇)化学试题2022年广西南宁地区初中第一次学业水平模拟考试化学试题重庆市黔江区2020-2021学年九年级下学期期末化学试题
选择题-单选题
|
适中(0.65)
解题方法
2. 为探究过氧化氢分解反应快慢的影响因素,某学习小组设计了下列实验,下列说法不正确的是
| 实验① | 实验② | 实验③ |
 | 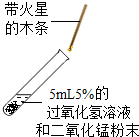 | 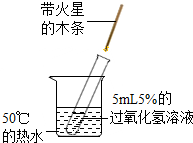 |
| A.对比实验①和②,可研究常温下,MnO2对反应快慢的影响 |
| B.对比实验①和③,可研究常温和50℃对反应快慢的影响是否相同 |
| C.对比实验②和③,可研究MnO2和50℃的温度对反应快慢的影响是否相同 |
| D.综合实验①、②和③可知,5%过氧化氢溶液最适合用于实验室制取氧气 |
【知识点】 催化作用解读 过氧化氢制取氧气实验解读 控制变量
您最近一年使用:0次
2021-01-23更新
|
350次组卷
|
6卷引用:广东省广州市天河区明珠教育集团2020-2021学年九年级上学期第二次月考化学试题
广东省广州市天河区明珠教育集团2020-2021学年九年级上学期第二次月考化学试题2021年福建省福州市中考三模(专题突破篇)化学试题江苏省扬州市江都区八校2021-2022学年九年级12月测试化学试题(已下线)第07讲 制取氧气-【暑假自学课】2022年新九年级化学暑假精品课(人教版)(已下线)2-03 制取氧气(下)(word讲义)-【帮课堂】2022-2023学年九年级上册化学同步精品讲义(人教版)2023分层教学_人教版_第二单元 课题3制取氧气 课时1_能力题(已审)
选择题-单选题
|
适中(0.65)
名校
3. 质量相等的两份药品 a 和 b,a 是混有少量二氧化锰的氯酸钾,b 是纯净的氯酸钾, 将药品分别加热,则收集到氧气的质量随加热时间变化的图象如图,正确的是( )
A. | B.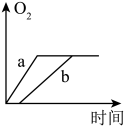 |
C.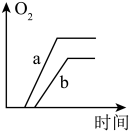 | D.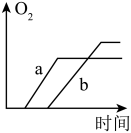 |
【知识点】 制取氧气实验的图像问题解读
您最近一年使用:0次
2020-10-04更新
|
500次组卷
|
29卷引用:四川省眉山龙正学区2018届九年级期中考试化学试题
四川省眉山龙正学区2018届九年级期中考试化学试题广东省虎门外语学校2019届九年级上学期11月月考化学试题【校级联考】黑龙江省齐齐哈尔市克东县2019届九年级上学期期末考试化学试题广东省东莞市虎门外国语学校2019届九年级上学期期中化学试卷四川省内江市西林中学2019届九年级下学期中考三模化学试题安徽省宿州市黄湾中学2019-2020学年九年级上学期期中化学试题安徽省合肥市包河区2019-2020学年九年级上学期期中化学试题黑龙江省大庆市肇源县第四中学2019-2020学年九年级上学期期中化学试题云南省曲靖市罗平县第四教研联合体2019—2020学年九年级上学期期中化学试题广东省汕头市潮南区两英镇2019-2020学年九年级上学期期末化学试题山西省晋中市灵石县2019-2020学年九年级上学期期末化学试题山西省2019-2020学年九年级上学期期末化学试题1广东省梅州市梅县区丙雁松片2019-2020学年九年级上学期期中联考化学试题广西南宁市青秀区天桃中学2019-2020学年八年级下学期开学考试化学试题天津市南开区翔宇学校2020-2021学年九年级上学期第一次月考化学试题山东省临沂市临沭县2020-2021学年九年级上学期期中化学试题山东省临沂市费县2020-2021学年九年级化学上学期期中试题江西省抚州市2020-2021学年九年级上学期期末化学试题云南省曲靖市麒麟区第七中学2019-2020学年九年级上学期第一次月考化学试题2021年福建省福州市中考三模(专题突破篇)化学试题黑龙江省齐齐哈尔市拜泉县第三中学2021-2022学年九年级上学期第一次质量测查化学试题广东省深圳市福田区深圳市实验中学初中部2021-2022学年九年级上学期10月月考化学试题湖南省常德市桃源县中路片区四校联考2021-2022学年九年级上学期期末化学试题黑龙江省大庆市肇源县第五中学2021-2022学年八年级上学期期中化学试题吉林省长春市公主岭市范家屯镇第二中学2021-2022学年九年级上学期第一次月考化学试题实验活动1 氧气的实验室制取与性质同步练习卷— 2022-2023学年化学九年级人教版上册(已下线)实验活动1 氧气的实验室制取与性质(练习)-【名课题精选】2023-2024学年九年级化学上册同步精品课件(人教版)江苏省盐城市亭湖新区初级中学2023-2024学年九年级上学期10月月考化学试题2019-2020学年广东省梅州市梅县区宪梓中学九年级(上)期末化学试卷(B)(解析版)
选择题-单选题
|
适中(0.65)
4. 称取21.6 g过氧化钙晶体(化学式为CaO2·yH2O),用热分析仪对其进行热分解实验,并绘制成固体质量与温度关系图(过氧化钙晶体受热时会先失去结晶水,350℃后会分解生成CaO和O2),下列说法不正确的是


| A.y值为8 |
| B.0~150 ℃未达到反应所需的温度 |
C.350 ℃后发生反应的化学方程式为2CaO2 2CaO+O2↑ 2CaO+O2↑ |
| D.CaO2中氧元素的化合价为-2价 |
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
5. 下列图像能正确反映对应变化关系的是
A. 常温下,稀释KOH溶液 常温下,稀释KOH溶液 |
B.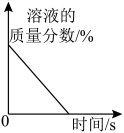 将浓硫酸露置在空气中 将浓硫酸露置在空气中 |
C. 足量粉末状金属分别与等质量、相同浓度的稀盐酸反应 足量粉末状金属分别与等质量、相同浓度的稀盐酸反应 |
D. 一定质量的饱和石灰水中加入生石灰 一定质量的饱和石灰水中加入生石灰 |
您最近一年使用:0次
2021-10-13更新
|
140次组卷
|
2卷引用:2021年福建省福州市中考三模(专题突破篇)化学试题
选择题-单选题
|
适中(0.65)
名校
解题方法
6. “价一类”二维图可以表示元素化合价与物质类别之间的关系,下图中的a、b、c、d、e代表常见的含碳物质,下列说法错误的是


| A.b和氧气反应生成c | B.c和水反应生成d |
| C.e可能难溶于水 | D.由a得到e至少要经过三步反应 |
您最近一年使用:0次
2021-08-09更新
|
145次组卷
|
8卷引用:2021年四川省成都市锦江区四川成都七中育才学校中考一诊化学试题
选择题-单选题
|
较难(0.4)
真题
7. 甲、乙、丙、丁四种物质的相互反应关系如图所示(“—”表示相连的物质间能发生反应)下列符合对应反应关系的选项是
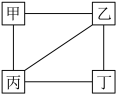

| 选项 | A | B | C | D | |
| 物质 | 甲 | Ca(OH)2 | CO2 | H2 | Fe |
| 乙 | Na2CO3 | NaOH | O2 | HCl | |
| 丙 | H2SO4 | CaCl2 | CuO | CuSO4 | |
| 丁 | BaCl2 | AgNO3 | HCl | NaOH | |
| A.A | B.B | C.C | D.D |
【知识点】 复分解反应发生的条件解读 各类物质间反应的总结解读
您最近一年使用:0次
2015-07-08更新
|
696次组卷
|
12卷引用:2015年初中毕业升学考试(湖北孝感卷)化学
2015年初中毕业升学考试(湖北孝感卷)化学【校级联考】江苏省南京市溧水区孔镇中学等八校2019届九年级下学期第一次联考化学试题江苏省南京市溧水区柘塘中学2019届九年级下学期中考一模化学试题(已下线)2019年4月28日 《每日一题》—— 每周一测2017年天津市红桥区中考三模化学试题2018年天津市西青区中考二模化学试题2018年江苏省南京市六合区中考二模化学试题2020年天津市滨海新区中考一模化学试题(已下线)天津市2020年一、二模汇编-物质间的转化、推断2021年天津市西青区九年级结课考试化学试题2021年云南省丽江市中考一模化学试题2021年福建省福州市中考三模(专题突破篇)化学试题
选择题-单选题
|
较难(0.4)
名校
8. 科学就是发现问题和解决问题,化学兴趣小组发现向碳酸钠溶液中滴加相同浓度的盐酸溶液并不是立即有气体生成,据此小组首先查阅资料:原来向碳酸钠溶液中加入盐酸时反应分两步完成。第一步,当加入盐酸的体积在0~V1ml时无气泡产生,此时发生的反应是Na2CO3+HCl=NaHCO3+NaCl;第二步,当加入盐酸的体积大于V1ml后,NaHCO3与盐酸反应产生气体,反应的化学方程式为NaHCO3+HCl=NaCl+CO2↑+H2O。然后在老师指导下使用数字化传感器测定反应过程中pH及CO2浓度的变化值如图所示,请同学们根据所学化学知识和资料及实验数据判断下列有关实验分析正确的是( )


| A.曲线①表示溶液pH的变化 |
| B.滴加0~40mL盐酸溶液时CO2浓度几乎不变,说明此时盐酸与碳酸钠没有发生反应 |
| C.A点溶液pH大于7,是因为碳酸钠的水溶液呈碱性 |
| D.B点所得溶液所含微粒有:Na+、Cl-、H+ |
您最近一年使用:0次
2020-06-13更新
|
216次组卷
|
4卷引用:2020年安徽省合肥市瑶海区中考二模化学试题
2020年安徽省合肥市瑶海区中考二模化学试题2021年福建省福州市中考三模(专题突破篇)化学试题2022年福建省厦门市同安第一中学中考热身作业化学试题(已下线)化学(深圳卷)-【试题猜想】2023年中考考前最后一卷
二、填空与简答 添加题型下试题
填空与简答-推断题
|
适中(0.65)
解题方法
9. 你玩过搭积木的游戏吗?小明用六块积木A~F,分别对应碳酸钠、铁、硫酸、二氧化碳、氢氧化钙、氯化钡。按照“物质间能反应,积木就能叠靠在一起,不反应积木就不接触”的原则搭成如图所示形状。

已知E的物质类别与其他五种不同。请回答下列问题:
(1)写出物质的化学式:A____ ;E____ 。
(2)①B与D反应的化学方程式为:____ 。②C与F反应的化学方程式为:____ 。
(3)B~F的叠放组合中,能发生的复分解反应共有____ 个。
(4)小美认为加一块积木X可以更稳定,X的名称是____ (不能重复A~F中的物质)。

已知E的物质类别与其他五种不同。请回答下列问题:
(1)写出物质的化学式:A
(2)①B与D反应的化学方程式为:
(3)B~F的叠放组合中,能发生的复分解反应共有
(4)小美认为加一块积木X可以更稳定,X的名称是
您最近一年使用:0次
2019-04-20更新
|
169次组卷
|
2卷引用:广东省佛山市顺德区2019届中考化学一模试卷
填空与简答-填空题
|
适中(0.65)
真题
解题方法
10. 黄铜矿(主要成分CuFeS2)经初步处理后,所得溶液甲中的溶质为Fe2(SO4)3、CuSO4及H2SO4。某同学通过废铁屑与溶液甲反应,制取补血剂原料碳酸亚铁并回收铜。主要步骤如图所示:
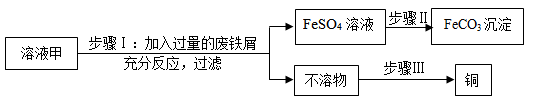
(1)Fe2(SO4)3与铁反应的化学方程式:x Fe2(SO4)3+ y Fe= z FeSO4,其中x、y、z为化学计量数,z的值为_____________ 。
(2)步骤Ⅰ中,生成铜的化学方程式:__________________________ 。
(3)步骤Ⅰ中,废铁屑含有少量铁锈,对产物的成分没有影响,原因是______________________ 。
(4)步骤Ⅱ中加入一种可溶性可实现其转化,从复分解反应发生的条件分析,该试剂可以是________ 。
(5)步骤Ⅲ回收铜的方法为___________________ 。

(1)Fe2(SO4)3与铁反应的化学方程式:x Fe2(SO4)3+ y Fe= z FeSO4,其中x、y、z为化学计量数,z的值为
(2)步骤Ⅰ中,生成铜的化学方程式:
(3)步骤Ⅰ中,废铁屑含有少量铁锈,对产物的成分没有影响,原因是
(4)步骤Ⅱ中加入一种可溶性可实现其转化,从复分解反应发生的条件分析,该试剂可以是
(5)步骤Ⅲ回收铜的方法为
您最近一年使用:0次
2016-11-28更新
|
232次组卷
|
3卷引用:2015年初中毕业升学考试(福建厦门卷)化学
三、科学探究题 添加题型下试题
科学探究题
|
较难(0.4)
11. 茶垢清洁剂能快速清除茶具上附着的茶垢,某小组同学对茶垢清洁剂进行了探究。
〖查阅资料〗如图所示是某品牌茶垢清洁剂说明书中的部分内容。说明书中碳酸钠的俗称有误,应改为_____ 。

〖提出问题Ⅰ〗茶垢清洁剂溶于水时生成过氧化氢,是否生成氧气?
〖实验1〗在盛有茶垢清洁剂固体的小烧杯中,加适量常温水,完全溶解后得到无色溶液,观察到有小气泡缓慢冒出,伸入带火星的木条,木条不复燃。
〖实验 2〗取三份等量的实验1中的溶液,分别加入甲、乙、丙三支试管中,按图所示进行实验。观察到都较快产生气泡,且温度越高产生气泡越快;伸入带火星的木条,木条都复燃。
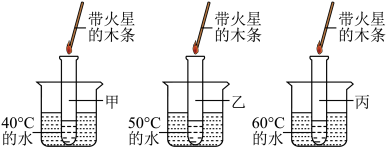
〖表达交流Ⅰ〗通过实验证明,茶垢清洁剂溶于水时生成氧气。
(1)实验1中“木条不复燃”的原因是_______ 。
(2)实验2中丙试管内不再产生气泡后,其中溶液所含溶质与加热前溶液的不同是_______ 。
〖提出问题Ⅱ〗茶垢清洁剂溶于水时生成碳酸钠,是否生成氢氧化钠?
〖实验 3〗取实验2丙试管内溶液,按如图流程进行实验。
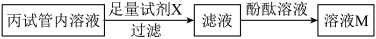
〖表达交流Ⅱ〗
(1)加入试剂X的目的是_______ (用化学方程式表示)。
(2)不新增试剂,检验加入的试剂X已足量的方法是_______ 。
(3)溶液M呈_______ 色,说明茶垢清洁剂溶于水时没有生成氢氧化钠。
〖反思总结〗
(1)茶垢清洁剂溶于水生成了碳酸钠和过氧化氢。碳酸钠溶液有较好的去污效果,过氧化氢分解生成活性氧,可深层带走污垢。
(2)使用茶垢清洁剂时应选择_______ 的水进行溶解,去垢效果更好。
〖查阅资料〗如图所示是某品牌茶垢清洁剂说明书中的部分内容。说明书中碳酸钠的俗称有误,应改为

〖提出问题Ⅰ〗茶垢清洁剂溶于水时生成过氧化氢,是否生成氧气?
〖实验1〗在盛有茶垢清洁剂固体的小烧杯中,加适量常温水,完全溶解后得到无色溶液,观察到有小气泡缓慢冒出,伸入带火星的木条,木条不复燃。
〖实验 2〗取三份等量的实验1中的溶液,分别加入甲、乙、丙三支试管中,按图所示进行实验。观察到都较快产生气泡,且温度越高产生气泡越快;伸入带火星的木条,木条都复燃。

〖表达交流Ⅰ〗通过实验证明,茶垢清洁剂溶于水时生成氧气。
(1)实验1中“木条不复燃”的原因是
(2)实验2中丙试管内不再产生气泡后,其中溶液所含溶质与加热前溶液的不同是
〖提出问题Ⅱ〗茶垢清洁剂溶于水时生成碳酸钠,是否生成氢氧化钠?
〖实验 3〗取实验2丙试管内溶液,按如图流程进行实验。

〖表达交流Ⅱ〗
(1)加入试剂X的目的是
(2)不新增试剂,检验加入的试剂X已足量的方法是
(3)溶液M呈
〖反思总结〗
(1)茶垢清洁剂溶于水生成了碳酸钠和过氧化氢。碳酸钠溶液有较好的去污效果,过氧化氢分解生成活性氧,可深层带走污垢。
(2)使用茶垢清洁剂时应选择
您最近一年使用:0次
2021-06-22更新
|
2441次组卷
|
23卷引用:河北省2021年中考化学试题
河北省2021年中考化学试题(已下线)专题23 科学探究-2021年中考化学真题分项汇编(全国通用)(第02期)2021年福建省福州市中考三模(专题突破篇)化学试题(已下线)2021年河北省中考化学真题变式汇编2021年河南省邓州市龙堰乡第一初级中学中考二模化学试题2021年河南省洛阳市孟津县第二初级中学中考一模化学试题2022年山西省吕梁市交城县中考一模化学试题江西省赣州市石城县第二中学2021-2022学年九年级下学期周考四化学试题2022年山东省滨州市滨城区中考一模化学试题(已下线)高分突破15 有关生产生活问题的探究-备战2022年中考化学实验探究题高分突破(已下线)高分突破01 关于实验传感器图像的探究-备战2022年中考化学实验探究题高分突破(已下线)高分突破05 有关燃烧与灭火的探究-备战2022年中考化学实验探究题高分突破(已下线)卷1-备战2022年中考化学【名校地市好题必刷】全真模拟卷(通用版)·第二辑2022年山东省滨州市博兴县中考一模化学试题2022年新疆乌鲁木齐市第八中学中考二模化学试题(已下线)2023中考风向标-山西-科学探究题(已下线)2023中考风向标-山西-科学探究题(已下线)2023年中考风向标-河北-科学探究题新疆克孜勒苏柯尔克孜自治州阿克陶县2023-2024学年学业水平第二次模拟化学试题江苏省宿迁市2023-2024学年九年级上学期期末化学试题(已下线)黄金卷03(深圳专用)-【赢在中考·黄金8卷】备战2024年中考化学模拟卷(广东专用)(已下线)2024年中考风向标-河北-科学探究题2024年河北省唐山市丰润区一模物理·化学试题-初中化学
四、计算题 添加题型下试题
计算题
|
适中(0.65)
解题方法
12. 利用下图甲所示的方法可粗略测定氢氧化钠溶液的浓度。反应的化学方程式为NaOH+HCl=NaCl+H2O。

(1)实验中,如何判断氢氧化钠溶液和稀盐酸恰好完全反应?_____________ 。
(2)若实验测得在持续滴加稀盐酸的过程中,该烧杯内物质溶液的pH变化如图乙所示。请计算该氢氧化钠溶液中溶质的质量分数。

(1)实验中,如何判断氢氧化钠溶液和稀盐酸恰好完全反应?
(2)若实验测得在持续滴加稀盐酸的过程中,该烧杯内物质溶液的pH变化如图乙所示。请计算该氢氧化钠溶液中溶质的质量分数。
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:身边的化学物质、物质的化学变化、化学实验、物质构成的奥秘
试卷题型(共 12题)
题型
数量
选择题
8
填空与简答
2
科学探究题
1
计算题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.65 | 金属与酸反应的图像 | 单选题 |
| 2 | 0.65 | 催化作用 过氧化氢制取氧气实验 控制变量 | 单选题 |
| 3 | 0.65 | 制取氧气实验的图像问题 | 单选题 |
| 4 | 0.65 | 用质量守恒定律解释现象 化学方程式的书写 不含杂质的化学方程式计算 化合价代数和的计算与应用 | 单选题 |
| 5 | 0.65 | 金属与酸反应的图像 浓酸敞口放置的变化和现象 生石灰的性质及用途 溶液酸碱性及pH相关关系 | 单选题 |
| 6 | 0.65 | 常用化合价规律 碳及其化合物间相互转化 盐类参与的反应 | 单选题 |
| 7 | 0.4 | 复分解反应发生的条件 各类物质间反应的总结 | 单选题 |
| 8 | 0.4 | 溶液酸碱性及pH相关关系 正盐、酸式盐及结晶水合物 实验的设计与操作 | 单选题 |
| 二、填空与简答 | |||
| 9 | 0.65 | 根据酸的通性推断物质的性质 根据碱的性质推断其他物质的性质 盐类参与的反应 各类物质间反应的总结 | 推断题 |
| 10 | 0.65 | 金属与酸反应原理 盐类参与的反应 | 填空题 |
| 三、科学探究题 | |||
| 11 | 0.4 | 过氧化氢制取氧气实验 常见盐的俗名、用途 盐类参与的反应 设计实验探究物质的成分 | |
| 四、计算题 | |||
| 12 | 0.65 | 不含杂质的化学方程式计算 溶质质量分数结合化学方程式的计算 无明显现象的中和反应的判断 | |



