江西省景德镇市2020-2021学年九年级下学期第二次质检(期中)化学试题
江西
九年级
期中
2022-05-20
240次
整体难度:
适中
考查范围:
物质的化学变化、物质构成的奥秘、化学实验、化学与社会发展、身边的化学物质
江西省景德镇市2020-2021学年九年级下学期第二次质检(期中)化学试题
江西
九年级
期中
2022-05-20
240次
整体难度:
适中
考查范围:
物质的化学变化、物质构成的奥秘、化学实验、化学与社会发展、身边的化学物质
一、选择题 添加题型下试题
选择题-单选题
|
容易(0.94)
解题方法
1. 凉拌冷粉是我市的特色早餐。下列冷粉的制作流程中,一定包含化学变化的是
| A.淘米 | B.磨米浆 | C.洗锅 | D.点燃煤炉 |
【知识点】 化学变化与物理变化判断解读
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
名校
解题方法
2. 臭氧(O3)能够吸收紫外线保护地球生命,打雷放电时,空气中有极少量氧气会转化成臭氧(O3),即O2→O3。下列有关说法中正确的是
①O2和O3都是单质;②O2和O3是不同的物质;③该变化属于物理变;④相同质量的O2和O3,所含分子的数目相同;⑤相同质量的O2和O3,所含原子的数目相同。
①O2和O3都是单质;②O2和O3是不同的物质;③该变化属于物理变;④相同质量的O2和O3,所含分子的数目相同;⑤相同质量的O2和O3,所含原子的数目相同。
| A.①②④ | B.①②⑤ | C.②③⑤ | D.②③④ |
您最近一年使用:0次
2021-03-05更新
|
101次组卷
|
2卷引用:江苏省苏州市苏州新区实验中学2020-2021学年九年级上学期期中化学试题
选择题-单选题
|
适中(0.65)
名校
3. 下列实验操作正确的是( )
A.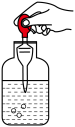 取液体药品 取液体药品 | B.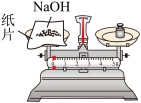 称量NaOH 固体 称量NaOH 固体 |
C. 配制溶液 配制溶液 | D.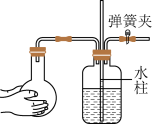 检查装置的气密性 检查装置的气密性 |
您最近一年使用:0次
2020-03-31更新
|
211次组卷
|
5卷引用:2020年福建省泉州市鲤城区泉州五中中考模拟化学试题
选择题-单选题
|
适中(0.65)
名校
解题方法
4. 原子簇是若干原子的聚集体,有望开发成新材料,某铝原子簇由13个铝原子构成其最外层电子数的总和为40时相对稳定,下图为铝原子的结构示意图,则该稳定铝原子簇的微粒符号是
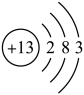

| A.Al3+ | B.13Al3+ | C.13Al- | D.Al13- |
您最近一年使用:0次
2021-03-05更新
|
180次组卷
|
3卷引用:江苏省苏州市苏州东沙湖、金鸡湖、星洋学校2020-2021学年九年级上学期期中联考化学试题
选择题-单选题
|
较易(0.85)
5. 景德镇的高岭土【主要成分:Al2(Si2O5)(OH)n】是制造陶瓷器的优良原料。经分析,其中铝、氧元素质量比为3∶8,则
| A.n=1 |
| B.n=2 |
| C.n=3 |
| D.n=4 |
【知识点】 根据化学式计算元素质量比解读
您最近一年使用:0次
2020-07-31更新
|
1189次组卷
|
27卷引用:江苏省常州市2020年中考化学试题
江苏省常州市2020年中考化学试题(已下线)《单元测试定心卷》第三单元 物质构成的奥秘(能力提升)-2020-2021学年九年级化学上册单元测试定心卷(沪教版)(已下线)《同步精品课堂》4.4 化学式与化合价(第二课时)(练习)-2020-2021学年人教版九年级化学上册同步精品课堂(已下线)《十分钟同步课堂专练》第四单元第5课 化学式计算(基础练)-2020-2021学年九年级化学上册十分钟同步课堂专练(人教版)江苏省无锡市梁溪区大桥实验学校2020-2021学年九年级上学期期中化学试题湖北省武汉市青山区2020-2021学年九年级上学期期中化学试题江苏省扬州市宝应县2020-2021学年九年级上学期期末化学试题江苏省苏州市工业园区金鸡湖中学2020-2021学年九年级上学期12月月考化学试题(已下线)【万唯原创】2021年河北省中考化学面对面卷练习册九年级第5单元2021年江苏省扬州市广陵区中考二模化学试题江苏省苏州市星海实验中学2020-2021学年九年级第一学期期中考试化学试题江西省南昌市西湖区百树学校2021-2022学年九年级上学期12月月考化学试题四川省乐山市市中区2020-2021学年九年级上学期期末化学试题江苏省无锡市2021-2022学年九年级上学期期末化学试题(已下线)单元04 自然界的水 【过关测试】-2022年中考一轮化学单元复习过过过(人教版)江西省景德镇市2020-2021学年九年级下学期第二次质检(期中)化学试题2022年江苏省扬州市中考化学模拟试题2022年河南省中考综合模拟训练化学试题(已下线)第11课 化学式计算-【预新知】2022年新九年级化学暑假自学精品讲义(人教版)(已下线)第15课 课题4化学式与化合价计算-2022-2023学年九年级化学上学期课后培优分级练(人教版)(已下线)3.3.2化学式相关计算-【帮课堂】2022-2023学年九年化学上册同步精品讲义(沪教版 )湖北省黄石市两镇一区2022-2023学年九年级上学期期末联考模拟化学试题(已下线)第16课 纯净物中元素间的质量关系(化学式计算)-【帮课堂】2023-2024学年九年化学上册同步学与练(沪教版·全国)(已下线)第四单元 课题4 化学式与化合价 4(有关相对分子质量的计算)-2023-2024学年九年级化学上册当堂清作业设计(人教版)(已下线)第18课 有关相对分子质量的计算(化学式计算)-【帮课堂】2023-2024学年九年级化学上册同步学与练(人教版)(已下线)专题04 自然界的水(专题检测)-2023-2024学年九年级化学上册期中期末考点归纳满分攻略讲练(人教版)(已下线)第3章 物质构成的奥秘-【好题汇编】备战2023-2024学年九年化学上学期期末真题分类汇编(沪教版,江苏专用)
选择题-单选题
|
较易(0.85)
名校
您最近一年使用:0次
2019-01-30更新
|
558次组卷
|
9卷引用:2016届河南省渑池县直中学九年级上学期精英对抗赛化学试卷
7. 下列说法正确的是
| A.pH试纸使用前用水润湿,不一定会产生实验误差 |
| B.吹胀气球,是由于气体分子间隔增大 |
| C.酸能使紫色石蕊溶液变红。通入CO2后的紫色石蕊溶液变红,所以CO2是酸 |
| D.溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小 |
您最近一年使用:0次
2022-05-17更新
|
42次组卷
|
2卷引用:江西省景德镇市2020-2021学年九年级下学期第二次质检(期中)化学试题
选择题-单选题
|
适中(0.65)
8. “化学棋”游戏规则:①每粒棋子代表一种物质;②吃子:所选棋子能与棋盘(如图)中的某棋子发生反应,则棋盘中的该棋子被吃掉;③连吃:前一次反应的生成物能与另一棋子发生反应时,则该棋子也被吃掉。若一次就可连续吃掉棋盘上的所有棋子,应选择的棋子是
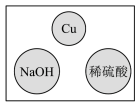

A. | B.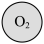 | C.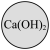 | D. |
您最近一年使用:0次
2019-06-26更新
|
1481次组卷
|
41卷引用:江苏省常州市2019年中考化学真题
江苏省常州市2019年中考化学真题(已下线)专题07 酸与碱 盐和复分解反应 化肥《备战2020年中考化学真题分类汇编》(江苏省)备战2020中考化学考题专项训练——酸和碱聚焦2020九年级化学基础演练——专题三十二 :常见的酸和碱2020年陕西省渭南市临渭区前进路中学中考模拟化学试题江苏省苏州市吴江区2020年九年级线上学习诊断性评价化学试题2020年河北省唐山市遵化市中考一模化学试题甘肃省兰州市城关区兰州外国语2019-2020学年九年级下学期开学考试化学试题(已下线)【万唯原创】2020年河北省中考化学面对面卷练习册九年级第十单元(已下线)第十单元、酸和碱·满分特训12020年山东省枣庄市台儿庄区中考一模化学试题2020年山东省德州市庆云县中考第二次练兵(二模)化学试题(已下线)盐 化肥·满分特训12020年山东省淄博市沂源县中考二模化学试题2020年江苏省苏州市昆山市三校联合调研化学试题2020年江苏省苏州市昆山市中考模拟化学试题(5月份)2020年山东省潍坊安丘市中考三模化学试题2020年山东省潍坊市诸城市中考二模化学试题(已下线)【万唯原创】2020年陕西省中考化学面对面卷题组训练5-62020年山东省潍坊市昌邑县中考二模化学试题2020年陕西省中考模拟化学试题2(已下线)主题 常见的酸和碱·满分特训2山东省枣庄市薛城区2019-2020学年九年级上学期期末化学试题山东省枣庄市2020-2021学年九年级上学期期末化学试题2021年山东省潍坊市诸城市中考二模化学试题(已下线)【万唯原创】2021年河北省中考化学面对面卷练习册九年级第10单元河南省商丘市柘城县实验中学2020-2021学年九年级下学期第一次月考化学试题(已下线)【万唯原创】2021年河南省中考化学试题研究卷练习册九年级第十单元(已下线)【万唯原创】2021年河南省中考化学面对面卷练习册九年级第10单元2021年广西贵港市桂平市中考三模化学试题(已下线)必刷卷02-2021年中考化学考前信息必刷卷(深圳专用)2021年山东省潍坊市青州市、临朐县、昌邑县、诸城市、昌乐县、寿光市中考二模化学试题2020年广东省广州市越秀区执信中学中考二模化学试题2021年山东省潍坊市寿光市古城初级中学中考二模化学试题2022年山东省中考总复习综合模拟化学试题(二)2022年福建省龙岩市上杭四中九年级下学期质量检测化学试题2022年广东省广州市华南师范大学附属中学中考二模化学试题江西省景德镇市2020-2021学年九年级下学期第二次质检(期中)化学试题江苏省泰州市兴化市2022-2023学年九年级下学期3月月考化学试题(已下线)专题02 常见的酸和碱-【学以致用】备战2023年中考化学易错题型讲练(广东专用)2024年陕西省榆林市佳县中考二模化学试题
选择题-单选题
|
适中(0.65)
名校
9. 实验创新是化学素养之一,如图是小峰设计的有关盐的性质的创新实验装置,下列是他对实验现象的描述及结论的分析,其中不正确的是
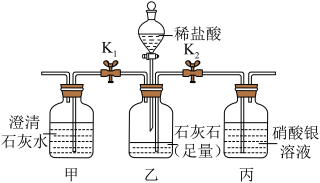

| A.关闭K2,打开K1,加入稀盐酸后,观察到乙中有气泡产生,甲中澄清石灰水变浑浊 |
| B.关闭K1、K2,加入稀盐酸,观察到乙中有气泡产生,一段时间后打开K2,丙中无明显现象 |
| C.该实验说明可以利用稀盐酸和澄清石灰水检验盐中是否有CO32- |
| D.由该实验可知盐可以与某些酸和某些盐反应 |
您最近一年使用:0次
2020-04-05更新
|
331次组卷
|
11卷引用:万唯联考2020山西线上大模考化学试题
万唯联考2020山西线上大模考化学试题2020年山西省中考模拟(线上)化学试题2020年山西省临汾市洪洞县中考模拟化学试题2020年6月广西柳州市中考模拟化学试题(已下线)考点38 盐的化学性质-备战2022年中考化学一轮复习考点帮江西省景德镇市2020-2021学年九年级下学期第二次质检(期中)化学试题2022年山西省汾阳市中考模拟化学试题(已下线)第十一单元 盐 化肥【过习题】 -2022-2023学年九年级化学下册单元复习过过过(人教版)2023年陕西省西安市高新唐南中学中考二模化学试题2023年陕西省西安市高新第一中学中考二模化学试题(已下线)专题02 气体的制取和净化(题型专练)-备战2024年中考化学一轮复习考点帮(沪教版·全国)
选择题-单选题
|
适中(0.65)
名校
10. 图像中的化学,下列图象能正确反映对应变化关系的是( )


| A.图像①可以表示向稀盐酸中滴加氢氧化钠溶液的 pH 变化 |
| B.图像②向一定量露置的熟石灰溶液中不断滴入稀盐酸至过量 |
| C.图像③表示加热高锰酸钾制取氧气过程中钾元素含量变化 |
| D.图像④表示向 KNO3 的饱和溶液中加入 KNO3 |
您最近一年使用:0次
2019-09-30更新
|
725次组卷
|
5卷引用:广东省深圳市龙岗区2018届初三年级调研测试题
二、选择填充题 添加题型下试题
选择填充题
|
容易(0.94)
名校
解题方法
11. 下列各组物质按单质、混合物的顺序排列的是________ 。
A.白酒、空气 B.氮气、生石灰 C.铁粉、焦炭 D._________
A.白酒、空气 B.氮气、生石灰 C.铁粉、焦炭 D.
您最近一年使用:0次
2022-05-17更新
|
44次组卷
|
2卷引用:江西省景德镇市2020-2021学年九年级下学期第二次质检(期中)化学试题
选择填充题
|
适中(0.65)
名校
解题方法
12. 如图所示是某化学反应的微观示意图,下列说法正确的是________ 。

A.该反应属于置换反应
B.该反应放热
C.生成物丁中碳和氧元素的质量比为1:2
D.参加反应的甲和乙的分子个数比为______

A.该反应属于置换反应
B.该反应放热
C.生成物丁中碳和氧元素的质量比为1:2
D.参加反应的甲和乙的分子个数比为
您最近一年使用:0次
2022-05-17更新
|
47次组卷
|
2卷引用:江西省景德镇市2020-2021学年九年级下学期第二次质检(期中)化学试题
选择填充题
|
适中(0.65)
解题方法
13. 为除去下列物质中的少量杂质(括号内为杂质),下列操作方法能达到目的的是________ 。
| 选项 | 物质(杂质) | 操作方法 |
| A | CuO (Cu) | 在空气中充分灼烧 |
| B | CO2 (H2O) | 将气体通过装生石灰的干燥管 |
| C. | CaO (CaCO3) | 加入足量水,充分溶解后过滤 |
| D | NaCl (Na2SO4) |
您最近一年使用:0次
三、填空与简答 添加题型下试题
14. 2019年年底新型冠状病毒的爆发,一场公共卫生紧急事件让我们更加明白健康的重要和生命的可贵。
(1)预防新型冠状病毒,首先要注意个人卫生,保持均衡饮食,提高自身的免疫力。小宇的妈妈准备了一份午餐:米饭、清蒸鲈鱼、红烧排骨、豆腐汤,其中富含蛋白质的是_______ (填一种即可)。从营养均衡的角度考虑,还应补充的营养素是________ 。
(2)做好居家环境的卫生,必要时使用消毒液对室内进行消毒。84消毒液是常用的消毒液,其主要有效成分为次氯酸钠(NaClO),次氯酸钠中氯元素的化合价为________ 价。消毒液喷洒后,室内充满刺激性气味,这说明_______ 。
(3)活性炭口罩能有效阻隔空气中的氨、苯、甲醛等有害气体,其功能比普通口罩强大,原因是活性炭具有________ 性。
(1)预防新型冠状病毒,首先要注意个人卫生,保持均衡饮食,提高自身的免疫力。小宇的妈妈准备了一份午餐:米饭、清蒸鲈鱼、红烧排骨、豆腐汤,其中富含蛋白质的是
(2)做好居家环境的卫生,必要时使用消毒液对室内进行消毒。84消毒液是常用的消毒液,其主要有效成分为次氯酸钠(NaClO),次氯酸钠中氯元素的化合价为
(3)活性炭口罩能有效阻隔空气中的氨、苯、甲醛等有害气体,其功能比普通口罩强大,原因是活性炭具有
您最近一年使用:0次
填空与简答-填空题
|
较易(0.85)
15. 归纳是学习的重要方法。学完盐的性质后,小郑归纳出酸的 A、B、C、D、E 五条化学性质,并用“五角星”呈现出来,见下图:
(1)图中酸的 D 性质中,即“五角星”右下角里面对应物质的类别是____________ ;

(2)紫色石蕊试液滴入酸中,溶液显_____________ 色;
(3)若酸是硫酸,请写出用稀硫酸清除铁锈的主要反 应化学方程式:________________ ;
(4)若酸是盐酸,请你选择一种常见的物质来检验酸 的 D 性质___________________ (填化学式);
(5)小郑探究 Mg 和 Fe 与酸液反应的快慢,需要控制的变量是______________________ (填代号)。
①金属的聚集形态(形状);②酸液起始温度;③酸液种类;④酸液的浓度;⑤反应容器的大小
(1)图中酸的 D 性质中,即“五角星”右下角里面对应物质的类别是

(2)紫色石蕊试液滴入酸中,溶液显
(3)若酸是硫酸,请写出用稀硫酸清除铁锈的主要反 应化学方程式:
(4)若酸是盐酸,请你选择一种常见的物质来检验酸 的 D 性质
(5)小郑探究 Mg 和 Fe 与酸液反应的快慢,需要控制的变量是
①金属的聚集形态(形状);②酸液起始温度;③酸液种类;④酸液的浓度;⑤反应容器的大小
【知识点】 酸的通性解读 控制变量法在实验设计中的应用解读
您最近一年使用:0次
2019-04-26更新
|
142次组卷
|
3卷引用:广东省揭阳市空港区2019届九年级下学期一模考试化学试题
填空与简答-简答题
|
较难(0.4)
名校
16. 将 60 g 某固体物质放入盛有 50 g 水的烧杯中充分溶解,测得溶液质量随温度变化的曲线如图。则 t1 ℃时该物质的溶解度为_____ g;A、B、C 三点所对应的溶液中,一定属于饱和溶液的是_____ 点处的溶液;将 t3 ℃时的 110 g 溶液稀释成20%,需加水的质量为_____ g。


【知识点】 饱和溶液和不饱和溶液判断解读 固体溶解度概念解读
您最近一年使用:0次
2020-03-01更新
|
348次组卷
|
5卷引用:2019年河南省中考化学试题(B卷)
填空与简答-推断题
|
较难(0.4)
解题方法
17. A~D是初中化学常见的四种不同的物质,C是一种酸。它们相互之间的关系如图所示,“———”表示两种物质之间可以相互反应,“→”表示一种物质可转化为另一种物质。分析辨识,解决问题:

(1)A的化学式是________ 。
(2)若B是氧化物,则B与C反应的化学方程式为________ 。
(3)D与CO2反应的化学方程式为________ 。
(4)C与D反应的微观实质是________________ 。

(1)A的化学式是
(2)若B是氧化物,则B与C反应的化学方程式为
(3)D与CO2反应的化学方程式为
(4)C与D反应的微观实质是
您最近一年使用:0次
2020-04-05更新
|
274次组卷
|
5卷引用:万唯联考2020山西线上大模考化学试题
四、实验题 添加题型下试题
实验题
|
较难(0.4)
解题方法
18. 某同学欲探究市售的某种品牌的牙膏和牙粉的主要成分,设计如下探究实验。
查阅资料。
(1)牙膏和牙粉均是由摩擦剂、活性剂、香料等成分组成的。
(2)常用的摩擦剂有极细颗粒的碳酸钙(CaCO3)水合硅酸(mSiO2.nH2O)等。
(3)牙膏和牙粉中除了碳酸钙以外,其他物质均不与稀盐酸反应产生气体。
【实验一】比较等质量牙膏和牙粉中碳酸钙的含量。
取如图1所示的两套相同装置,分别加入等质量的牙膏和牙粉于锥形瓶中,并在分液漏斗中加入等质量、等浓度的稀盐酸。
(1)打开分液漏斗活塞注入一定量的稀盐酸,然后关闭活塞,观察到有气泡产生,发生反应的化学方程式为________ 。
(2)待反应结束后,再打开活塞,继续注入一定量的稀盐酸,关闭活塞,未观察到明显现象,继续加入稀盐酸的目的是_________ 。
(3)称量反应后装置及药品的总质量,发现加入牙膏的装置及药品的总质量大于加入牙粉的装置及药品的总质量,说明_______ 。
(4)小丽在实验前检查该装置的气密性,但小华认为该实验不需要检查装置的气密性,其原因是_________ 。

【实验二】取一定量的牙粉做如图2所示实验(牙粉完全反应)。实验记录如下表(表中数据在相同温度、相同压强下测定)。
(5)根据以上实验过程和数据综合分析,最终生成CO2的体积是______ mL,理由是______ 。
(6)若在该条件下CO2的密度为2.2g/L,根据数据求该牙粉中钙元素的质量_________ g。
查阅资料。
(1)牙膏和牙粉均是由摩擦剂、活性剂、香料等成分组成的。
(2)常用的摩擦剂有极细颗粒的碳酸钙(CaCO3)水合硅酸(mSiO2.nH2O)等。
(3)牙膏和牙粉中除了碳酸钙以外,其他物质均不与稀盐酸反应产生气体。
【实验一】比较等质量牙膏和牙粉中碳酸钙的含量。
取如图1所示的两套相同装置,分别加入等质量的牙膏和牙粉于锥形瓶中,并在分液漏斗中加入等质量、等浓度的稀盐酸。
(1)打开分液漏斗活塞注入一定量的稀盐酸,然后关闭活塞,观察到有气泡产生,发生反应的化学方程式为
(2)待反应结束后,再打开活塞,继续注入一定量的稀盐酸,关闭活塞,未观察到明显现象,继续加入稀盐酸的目的是
(3)称量反应后装置及药品的总质量,发现加入牙膏的装置及药品的总质量大于加入牙粉的装置及药品的总质量,说明
(4)小丽在实验前检查该装置的气密性,但小华认为该实验不需要检查装置的气密性,其原因是

【实验二】取一定量的牙粉做如图2所示实验(牙粉完全反应)。实验记录如下表(表中数据在相同温度、相同压强下测定)。
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/mL | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
(6)若在该条件下CO2的密度为2.2g/L,根据数据求该牙粉中钙元素的质量
您最近一年使用:0次
实验题
|
适中(0.65)
解题方法
19. 某化学兴趣小组在探究“复分解反应发生的条件”时,选做了如图所示的三个实验。
(提示:BaCl2溶液呈中性)

祺祺:向试管I中慢慢滴入MgCl2溶液,并不断振荡,至溶液颜色恰好变为无色为止。
雯雯:分别完成试管Ⅱ和Ⅲ中的两个实验后,接着进行如下探究(如图)。请分析后作答。

(1)雯雯经过分析推断,试管Ⅲ反应后所得溶液中一定含有的溶质是________ (填化学式);步骤①中一定发生的反应的化学方程式是______ ;滤液C的溶质一定有______ (填化学式)。
(2)祺祺把沉淀M、N混合后加入AgNO3溶液和过量的稀硝酸,观察到的实验现象是______ 。实验结束,祺祺把反应后的混合物与滤液C全部倒入废液缸中,则废液缸内上层清液中,除酚酞和HNO3外一定含有的溶质有_____ (填化学式)。
(提示:BaCl2溶液呈中性)

祺祺:向试管I中慢慢滴入MgCl2溶液,并不断振荡,至溶液颜色恰好变为无色为止。
雯雯:分别完成试管Ⅱ和Ⅲ中的两个实验后,接着进行如下探究(如图)。请分析后作答。

(1)雯雯经过分析推断,试管Ⅲ反应后所得溶液中一定含有的溶质是
(2)祺祺把沉淀M、N混合后加入AgNO3溶液和过量的稀硝酸,观察到的实验现象是
您最近一年使用:0次
五、计算题 添加题型下试题
计算题
|
较难(0.4)
20. 为测定铜锌合金中锌的质量分数,进行了以下实验;取40g铜锌合金放入烧杯中,称得烧杯及所盛铜锌合金的总质量为140g,再把120g盐酸平均分成四份依次加入烧杯中,每次充分反应后进行称量,实验数据如下:
请你据此分析计算:
(1)第一次实验生成氢气的质量是 ________ g.
(2)利用第一次实验的数据,计算30g盐酸中溶质的质量分数________ (写出计算过程,精确到0.1%)
(3)实验最终结束后,同学们求出了合金中锌的质量分数=__________。
(4)下图表示所加盐酸的质量与反应后所得溶液质量的关系曲线,请写出A点(X=______ ,Y=______)的坐标。

| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质的总质量/g | 169.7 | 199.4 | 229.2 | 259.2 |
(1)第一次实验生成氢气的质量是 ________ g.
(2)利用第一次实验的数据,计算30g盐酸中溶质的质量分数________ (写出计算过程,精确到0.1%)
(3)实验最终结束后,同学们求出了合金中锌的质量分数=__________。
(4)下图表示所加盐酸的质量与反应后所得溶液质量的关系曲线,请写出A点(X=______ ,Y=______)的坐标。

您最近一年使用:0次
2018-05-11更新
|
294次组卷
|
2卷引用:广东省揭阳市揭西县2018届九年级下学期期中考试化学试题
试卷分析
整体难度:适中
考查范围:物质的化学变化、物质构成的奥秘、化学实验、化学与社会发展、身边的化学物质
试卷题型(共 20题)
题型
数量
选择题
10
选择填充题
3
填空与简答
4
实验题
2
计算题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 化学变化与物理变化判断 | 单选题 |
| 2 | 0.65 | 化学变化与物理变化判断 单质和化合物的判断 化学式、分子式及涵义 | 单选题 |
| 3 | 0.65 | 量筒的正确使用方法和注意事项 托盘天平的正确使用方法和注意事项 胶头滴管的正确使用方法和注意事项 | 单选题 |
| 4 | 0.65 | 原子核外电子的分层排布认识 原子结构示意图含义及应用 核外电子排布规律的理解及应用 最外层电子在化学变化中的作用 | 单选题 |
| 5 | 0.85 | 根据化学式计算元素质量比 | 单选题 |
| 6 | 0.85 | 燃烧的定义及条件 | 单选题 |
| 7 | 0.65 | 微粒的观点解释现象 二氧化碳与水的反应及实验 晶体与非晶体 溶液的酸碱性的判断与pH的测定 | 单选题 |
| 8 | 0.65 | 金属与酸反应原理 金属活动顺序理解和判断 酸的通性 氯化钠 | 单选题 |
| 9 | 0.65 | 制取二氧化碳原理的拓展 二氧化碳与碱的反应及实验 碳酸根离子的验证 | 单选题 |
| 10 | 0.65 | 高锰酸钾制取氧气实验 图像分析溶质质量分数的变化 溶液酸碱性及pH相关关系 计算混合物中物质或元素的质量分数 | 单选题 |
| 二、选择填充题 | |||
| 11 | 0.94 | 纯净物和混合物的判断 单质和化合物的判断 生石灰的性质及用途 | |
| 12 | 0.65 | 置换反应 化学方程式含义 根据化学式计算元素质量比 常见吸热反应及放热反应 | |
| 13 | 0.65 | 盐类参与的反应 灼烧(在空气中) 干燥 转化为沉淀 | |
| 三、填空与简答 | |||
| 14 | 0.85 | 微粒的观点解释现象 化合价代数和的计算与应用 活性炭的吸附性 蛋白质 | 填空题 |
| 15 | 0.85 | 酸的通性 控制变量法在实验设计中的应用 | 填空题 |
| 16 | 0.4 | 饱和溶液和不饱和溶液判断 固体溶解度概念 | 简答题 |
| 17 | 0.4 | 根据酸的通性推断物质的性质 根据碱的性质推断其他物质的性质 中和反应的概念及微观本质 | 推断题 |
| 四、实验题 | |||
| 18 | 0.4 | 用质量守恒定律解释现象 不含杂质的化学方程式计算 盐类参与的反应 | |
| 19 | 0.65 | 常见的酸碱指示剂及其变色情况 盐类参与的反应 几种常见阴、阳离子的鉴别 设计实验探究物质的成分 | |
| 五、计算题 | |||
| 20 | 0.4 | 含杂质的化学方程式计算 金属与酸反应 溶质质量分数结合化学方程式的计算 | |



