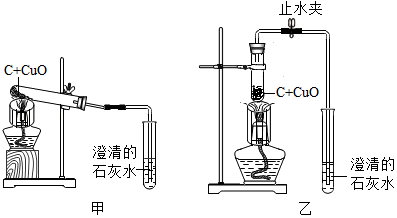
16. 某中学化学兴趣小组按照课本实验方法(如图甲),做木炭与氧化铜反应实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现。他们决定对这个实验进行探究和改进。请写出木炭还原氧化铜的方程式:
___________。
【提出问题】暗红色的固体是什么?如何选择合适的条件,使这个实验的现象更明显?
【查阅资料】铜有+1和+2两种化合价,通常情况下,氧的化合价为-2。
【进行猜想】同学们认为这种暗红色固体可能是一种氧化物,并猜测它的化学式为
___________。
【交流讨论】同学们还认为,通过改变反应物的状态、质量比,以及反应装置,可以使该实验现象更加明显,减少出现暗红色固体的情况。
小吴建议用超细炭粉与氧化铜粉末进行实验。你认为这样建议的原理是
___________。
小周建议用图乙装置替代甲装置。与甲相比较,乙装置中将试管直立放置的作用是
___________。
【实验过程】同学们决定按改进后的方案进行实验,往试管中加入已干燥的药品并开始加热,当看到澄清的石灰水刚出现浑浊时,
___________(填“能”或“不能”)确定氧化铜和炭粉已经开始反应。不久,即可看到试管底部变红热,停止加热后,仍能看到红热现象,并沿试管底部自下而上蔓延,这个现象说明该反应是
___________(填“吸”或“放”)热反应。
【拓展延伸】兴趣小组同学在实验过程中发现在木炭和氧化铜的混合物中加入一定量的某种添加剂后,此实验只利用酒精灯加热也能快速完成,他们利用同样的酒精灯做了如下实验:
| 1 | 2 | 3 | 4 | 5 | 6 |
| 木炭0.3g,氧化铜3.4g | 木炭0.3g,氧化铜3.4g | 木炭0.3g,氧化铜3.4g | 木炭0.25g,氧化铜3.4g | 木炭0.3g,氧化铜3.4g | 木炭0.3g,氧化铜3.4g |
| 不加添加剂 | 0.1gCaCl2 | 0.1gKCl | 0.1gMgCl2 | 0.1gK2SO4 | 0.1gNa2CO3 |
| 加热时间长,几乎没有红色物质析出 | 加热约1分钟后,剧烈反应,产物红亮美观,有金色铜粒生成 | 加热约2分钟后,剧烈反应,产物红色,有金色铜粒生成 | 加热约1分钟后,剧烈反应,产物红亮美观 | 加热时间长,产生红色物质不明显 | 加热时间长,产生红色物质不明显 |
(1)请你推测主要是哪一种离子对木炭和氧化铜的反应有促进作用?
___________,说出你的判断理由
___________。
(2)除了上述离子对木炭和氧化铜反应的促进作用以外,产生金色铜粒的还需要什么条件?
___________。