废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下。
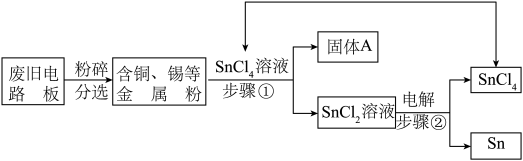
已知:Sn+SnCl4=2SnCl2
(1)SnCl4中锡元素的化合价是_____________________ 。
(2)铜的金属活动性比锡的________ (填“强”或“弱”),固体A中一定含有的金属元素是_______ 。
(3)写出步骤②发生反应的化学方程式________________________________________ 。
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是__________________ (回答一点即可)。

已知:Sn+SnCl4=2SnCl2
(1)SnCl4中锡元素的化合价是
(2)铜的金属活动性比锡的
(3)写出步骤②发生反应的化学方程式
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是
2018·安徽·中考真题 查看更多[17]
2022年安徽省学业水平考试猜题卷化学试题安徽省阜阳市颍州区城南中学2021-2022学年九年级下学期开学化学作业检测试题(已下线)第16讲 金属的活动性-2022年中考化学一轮总复习基础通关安徽省芜湖市南陵县十校联考2020-2021学年九年级下学期化学试题湖北省黄石市大冶市还地桥镇五校2020~2021学年九年级下学期开学联考化学试题(已下线)专题18 工艺流程图题(考点专练)-备战2021年中考化学考点微专题(已下线)主题 金属的化学性质·满分特训1(已下线)主题 金属的化学性质·基础必练1(已下线)主题 金属与金属矿物·基础必练2广西柳州市城中区龙城中学2019-2020学年九年级下学期开学测试化学试题广西南宁市青秀区南宁二中2019-2020学年九年级下学期2月开学考试化学试题2019年广西来宾市象州县中考一模化学试题安徽省宿州市埇桥区教育集团2019-2020学年九年级上学期期末化学试题【市级联考】辽宁省葫芦岛市兴城市2019届九年级下学期中考一模化学试题福建省泉州第十六中学2019届九年级下学期(3月)第一次模拟考试化学试题(已下线)2018年中考试题分项版解析汇编【第一期】专题8—1 金属材料、金属资源的利用、保护安徽省2018年中考化学
更新时间:2018-06-21 12:00:19
|
相似题推荐
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】有一包粉末,已知其由BaCO3、Cu(NO3)2、Na2SO4、NaCl、NaOH中的几种组成,现对其做以下实验,各步骤均已经充分反应,请回答问题:
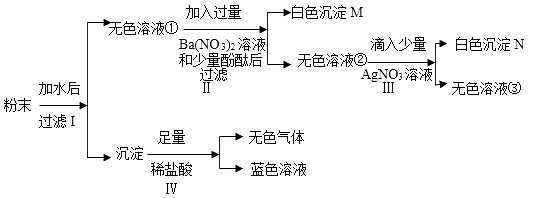
(1)请写出沉淀N的化学式:___________ 。
(2)步骤Ⅱ所发生反应的化学方程式为_________ ,其基本反应类型为____ 。
(3)无色溶液②中一定存在的溶质(酚酞除外)的化学式为___________ 。
(4)这包粉末中共含有___________ 种物质。

(1)请写出沉淀N的化学式:
(2)步骤Ⅱ所发生反应的化学方程式为
(3)无色溶液②中一定存在的溶质(酚酞除外)的化学式为
(4)这包粉末中共含有
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐2】已知某固体混合物 中可能含有
中可能含有 、
、 、
、 、
、 、
、 五种物质中的两种或多种。按下述步骤进行实验探究,观察实验现象,并加以分析推理。(设过程中所有发生的反应都恰好完全反应)
五种物质中的两种或多种。按下述步骤进行实验探究,观察实验现象,并加以分析推理。(设过程中所有发生的反应都恰好完全反应)
Ⅰ.取一定质量的该固体混合物放入一洁净烧杯中,向其中加入适量稀硝酸,搅拌,有气体生成,待烧杯中物质充分反应后,过滤,得滤液 和沉淀
和沉淀 。
。
Ⅱ.取滤液 ,向其中加入适量
,向其中加入适量 溶液,搅拌,待烧杯中物质充分反应后,过滤,得滤液
溶液,搅拌,待烧杯中物质充分反应后,过滤,得滤液 和蓝色沉淀
和蓝色沉淀 。
。
根据上述实验过程和发生的现象做出相应推理,填写以下空白:
(1)蓝色沉淀 的化学式是
的化学式是_____ 。
(2)在固体混合物 中,上述五种物质中肯定存在的物质是
中,上述五种物质中肯定存在的物质是_____ (写化学式)。
(3)写出步骤Ⅰ中生成沉淀 的化学方程式
的化学方程式_____ 。
(4)在滤液 中,含有的金属阳离子最多有
中,含有的金属阳离子最多有______ 种,该滤液中肯定存在的酸根离子______ 。
(5)在混合物 中,上述五种物质中还不能确定存在的物质是
中,上述五种物质中还不能确定存在的物质是______ (写化学式),得出此结论的理由是_____ 。
 中可能含有
中可能含有 、
、 、
、 、
、 、
、 五种物质中的两种或多种。按下述步骤进行实验探究,观察实验现象,并加以分析推理。(设过程中所有发生的反应都恰好完全反应)
五种物质中的两种或多种。按下述步骤进行实验探究,观察实验现象,并加以分析推理。(设过程中所有发生的反应都恰好完全反应)Ⅰ.取一定质量的该固体混合物放入一洁净烧杯中,向其中加入适量稀硝酸,搅拌,有气体生成,待烧杯中物质充分反应后,过滤,得滤液
 和沉淀
和沉淀 。
。Ⅱ.取滤液
 ,向其中加入适量
,向其中加入适量 溶液,搅拌,待烧杯中物质充分反应后,过滤,得滤液
溶液,搅拌,待烧杯中物质充分反应后,过滤,得滤液 和蓝色沉淀
和蓝色沉淀 。
。根据上述实验过程和发生的现象做出相应推理,填写以下空白:
(1)蓝色沉淀
 的化学式是
的化学式是(2)在固体混合物
 中,上述五种物质中肯定存在的物质是
中,上述五种物质中肯定存在的物质是(3)写出步骤Ⅰ中生成沉淀
 的化学方程式
的化学方程式(4)在滤液
 中,含有的金属阳离子最多有
中,含有的金属阳离子最多有(5)在混合物
 中,上述五种物质中还不能确定存在的物质是
中,上述五种物质中还不能确定存在的物质是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
解题方法
【推荐3】物质除杂是化学实验中经常遇到的问题。
【方法探究】为除去二氧化碳气体中混有的少量一氧化碳,小明设计了三种方案。
上述方案中有两个是合理的,写出合理方案中任意一个反应的化学方程式_______ ;
【方法提炼】上述两种合理方案体现了物质除杂的不同思路:
思路一:将杂质直接转化为所需物质;
思路二:将所需物质转化为中间物质,再将中间物质转化为所需物质。
【方法运用】
运用思路一:除去氯化镁粉末中混有的少量氯化钡,先加足量的水溶解,再向溶液中加入适量的_______ 溶液,过滤、蒸发,即得氯化镁固体。
运用思路二:除去氯化镁粉末中混有的少量氯化钡、氯化钠和硫酸钾。
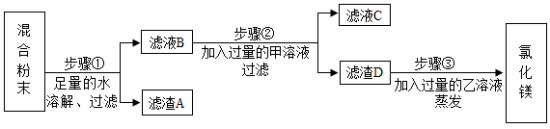
步骤①中反应的化学方程式是_________ ,滤液B中一定含有的溶质是 ________ ;
步骤②中反应的化学方程式是_________ ,滤液C中一定含有的阴离子是________ ;
步骤③中乙溶液是________ (填化学式)溶液。
【方法探究】为除去二氧化碳气体中混有的少量一氧化碳,小明设计了三种方案。
| 实验方案 | |
| 方案A |  |
| 方案B | 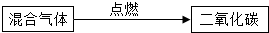 |
| 方案C | 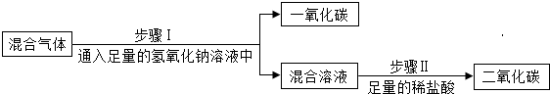 |
【方法提炼】上述两种合理方案体现了物质除杂的不同思路:
思路一:将杂质直接转化为所需物质;
思路二:将所需物质转化为中间物质,再将中间物质转化为所需物质。
【方法运用】
运用思路一:除去氯化镁粉末中混有的少量氯化钡,先加足量的水溶解,再向溶液中加入适量的
运用思路二:除去氯化镁粉末中混有的少量氯化钡、氯化钠和硫酸钾。

步骤①中反应的化学方程式是
步骤②中反应的化学方程式是
步骤③中乙溶液是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐1】下图是采用“联合脱硫脱氮技术”处理含SO2、NO的烟气,获得含CaSO4、Ca(NO2)2副产品的流程。
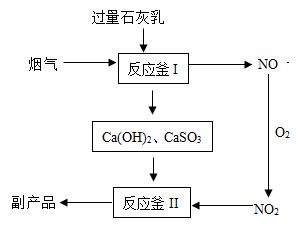
(1)CaSO3中硫元素的化合价为____________ 。
(2)反应釜Ⅱ中发生反应的化学方程式为____________ 。(反应中Ca(OH)2、CaSO3的化学计量系数之比为1:1)。

(1)CaSO3中硫元素的化合价为
(2)反应釜Ⅱ中发生反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐2】我国某科研团队以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料,制取高纯碳酸锰,工艺流程如下图:

已知:①SiO2不溶于水,不与稀H2SO4、SO2反应;②MnO2能将Fe2+氧化成Fe3+;③溶液中的Fe3+在 pH 大于或等于 3.2 时将完全转化为Fe(OH)3沉淀。
请回答:(1)滤渣Ⅰ、Ⅱ分别为_____ 、_____ (写化学式) ;
(2)浸锰过程中发生了 2 个化学反应,其中一个为Fe2O3与SO2反应,该反应的化学方 程式为Fe2O3+ SO2+H2SO4=2FeSO4+ H2O,另一个为MnO2和SO2按化学计量数为 1:1 发生化合反应,请写出该反应的化学方程式:_____ , 该反应中共有_____ 种元素的化合价发生了改变。
(3)“沉锰”:加入NH4HCO3溶液后,生成了 4 种产物,其中含有MnCO3沉淀和某种气 体,写出该反应的化学方程式:_____ 。
(4)取所得的高纯MnCO311.7g溶于足量的盐酸中,将产生的气体用足量的Ba(OH)2浓 溶液吸收,得到白色沉淀 19.7g,则所得产品的纯度为_____ %(保留一位小数)
(5)某研究小组用稀H2SO4与菱锰矿(含有MnCO3)反应来浸出Mn2+,该研究小组选 定两个因素作为研究条件进行对比实验,数据如下:
表中 X 最有可能的数值为_____ 。
a.79.7 b.80.8 c.87.6 d.92.8

已知:①SiO2不溶于水,不与稀H2SO4、SO2反应;②MnO2能将Fe2+氧化成Fe3+;③溶液中的Fe3+在 pH 大于或等于 3.2 时将完全转化为Fe(OH)3沉淀。
请回答:(1)滤渣Ⅰ、Ⅱ分别为
(2)浸锰过程中发生了 2 个化学反应,其中一个为Fe2O3与SO2反应,该反应的化学方 程式为Fe2O3+ SO2+H2SO4=2FeSO4+ H2O,另一个为MnO2和SO2按化学计量数为 1:1 发生化合反应,请写出该反应的化学方程式:
(3)“沉锰”:加入NH4HCO3溶液后,生成了 4 种产物,其中含有MnCO3沉淀和某种气 体,写出该反应的化学方程式:
(4)取所得的高纯MnCO311.7g溶于足量的盐酸中,将产生的气体用足量的Ba(OH)2浓 溶液吸收,得到白色沉淀 19.7g,则所得产品的纯度为
(5)某研究小组用稀H2SO4与菱锰矿(含有MnCO3)反应来浸出Mn2+,该研究小组选 定两个因素作为研究条件进行对比实验,数据如下:
矿酸比 | 温度/(℃) | 浸出率/(%) | |
1 | 1:0.5 | 60 | 80.2 |
2 | 1:0.5 | 80 | 83.8 |
3 | 1:0.6 | 60 | X |
4 | 1:0.6 | 80 | 91.8 |
a.79.7 b.80.8 c.87.6 d.92.8
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】向Cu(NO3)2、AgNO3的混合溶液中加入一定量的锌粉、铁粉的混合物,并充分反应,过滤得滤渣和滤液。若往滤渣中加入盐酸有气体放出,则滤液中一定有的溶质是_____ 。
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】金属及金属材料在生产、生活中有广泛的应用。
(1)生活中用铁锅做炊具,利用了铁的______ 性。铁锅易生锈,结合生活实际,写出一种防止铁锅生锈的具体方法______ 。铝的化学性质比铁活泼,但通常铝制品比铁制品更耐腐蚀的原因是______ ;
(2)我国古代曾用“湿法炼铜”“火法炼铜”。“湿法炼铜”的原理是“曾青(硫酸铜溶液)得铁则化为铜”;“火法炼铜”中用辉铜矿(主要成分Cu2S)炼铜的原理是:Cu2S与氧气在高温条件下反应生成铜和一种会导致酸雨的气体(其相对分子质量为64)。从减少空气污染的角度分析,相对环保的炼铜方法是______ ,写出其化学反应方程式______ ;
(3)已知Fe、R、Cr三种金属存在如下反应:Fe+ RCl2=R + FeCl2,Cr+FeSO4= Fe+CrSO4,则Fe、R、Cr三种金属的活动性由强到弱的顺序是______ ;
(4)含有锌粉6.5g,铁粉5.6g,铜粉3.2g,铝粉1.8g的混合物,与一定质量的稀硫酸反应,反应停止后,有6g固体剩余,则剩余固体是______ 。
(1)生活中用铁锅做炊具,利用了铁的
(2)我国古代曾用“湿法炼铜”“火法炼铜”。“湿法炼铜”的原理是“曾青(硫酸铜溶液)得铁则化为铜”;“火法炼铜”中用辉铜矿(主要成分Cu2S)炼铜的原理是:Cu2S与氧气在高温条件下反应生成铜和一种会导致酸雨的气体(其相对分子质量为64)。从减少空气污染的角度分析,相对环保的炼铜方法是
(3)已知Fe、R、Cr三种金属存在如下反应:Fe+ RCl2=R + FeCl2,Cr+FeSO4= Fe+CrSO4,则Fe、R、Cr三种金属的活动性由强到弱的顺序是
(4)含有锌粉6.5g,铁粉5.6g,铜粉3.2g,铝粉1.8g的混合物,与一定质量的稀硫酸反应,反应停止后,有6g固体剩余,则剩余固体是
您最近一年使用:0次
【推荐3】I、小亮学完合金后,知道了不锈钢的主要成分是铁,白铜中含有铜和镍(Ni)。
(1)【查阅资料】镍能与稀硫酸反应生成能溶于水的NiSO4,并放出氢气。写出镍与稀硫酸反应的化学方程式:_____________ 。
(2)向AgNO3、Cu(NO3)2的混合溶液中加入一定量的锌粉,充分反应,过滤。若反应后溶液为无色,滤渣中一定含有___________ 。
II、如图是硝酸钾(KNO3)和氯化钾(KCl)的溶解度曲线,请回答下列问题。
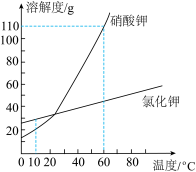
(3)10 ℃时,KNO3和KCl溶解度大小关系是___________ 。
(4)60℃时,将60 g KNO3固体放50g水中,充分溶解后,所得溶液的质量为_______ g。
(5)60 ℃时,从KNO3和KCl两种饱和溶液中获得等质量晶体,蒸发水较多的是________ 溶液。
(1)【查阅资料】镍能与稀硫酸反应生成能溶于水的NiSO4,并放出氢气。写出镍与稀硫酸反应的化学方程式:
(2)向AgNO3、Cu(NO3)2的混合溶液中加入一定量的锌粉,充分反应,过滤。若反应后溶液为无色,滤渣中一定含有
II、如图是硝酸钾(KNO3)和氯化钾(KCl)的溶解度曲线,请回答下列问题。

(3)10 ℃时,KNO3和KCl溶解度大小关系是
(4)60℃时,将60 g KNO3固体放50g水中,充分溶解后,所得溶液的质量为
(5)60 ℃时,从KNO3和KCl两种饱和溶液中获得等质量晶体,蒸发水较多的是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐1】某工厂排放的废液中含有Zn(NO3)2和AgNO3,为回收金属Ag,设计了下列方案:
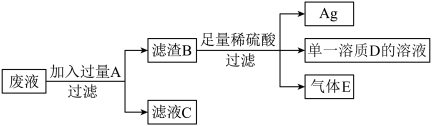
(1)B中含有________ ,滤液C中含有的溶质是________ ,气体E是________ .
(2)写出A与废液中的物质发生反应的化学方程式_______________________ .

(1)B中含有
(2)写出A与废液中的物质发生反应的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】据统计,我国每年报废的手机超过 1 亿部,若不进行有效回收利用,会造成巨大的浪费和污染。某种手机电路板中含有以下金属:Sn(锡)、Fe、Cu、Au、Ag、Pd(钯,银白色)。如图是某工厂回收其中部分金属的流程示意图。(假设流程示意图中各步反应均恰好完全反应。)
已知:①2Cu+O2+2H2SO4 2CuSO4+2H2O ②Sn常见化合价为+2价
2CuSO4+2H2O ②Sn常见化合价为+2价
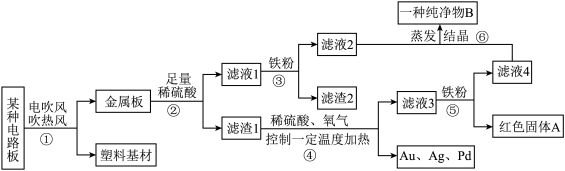
(1)滤渣2中含有的金属是______ 。
(2)写出反应③的化学方程式______ 。
(3)写出反应⑤的化学方程式为______ 。
(4)纯净物B中所含铁元素与金属板中所含铁元素的质量是否相等______ (填“是”或“否”)。
(5)金属 Fe、Sn、Pd 在溶液中的活动性由强到弱的顺序依次是______ 。
(6)上述①~⑥中涉及置换反应的有______ 。
已知:①2Cu+O2+2H2SO4
 2CuSO4+2H2O ②Sn常见化合价为+2价
2CuSO4+2H2O ②Sn常见化合价为+2价
(1)滤渣2中含有的金属是
(2)写出反应③的化学方程式
(3)写出反应⑤的化学方程式为
(4)纯净物B中所含铁元素与金属板中所含铁元素的质量是否相等
(5)金属 Fe、Sn、Pd 在溶液中的活动性由强到弱的顺序依次是
(6)上述①~⑥中涉及置换反应的有
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
【推荐3】金属镍可用于制造货币、不锈钢等。粗制氧化镍主要含氧化镍(NiO),以及少量氧化钴(CoO)和氧化铁,以粗制氧化镍为原料制备纯镍的流程如下:
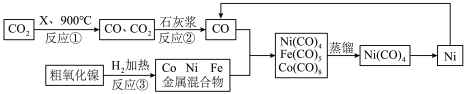
(1)反应①中,反应物X可能是_____ 。
(2)石灰浆是氢氧化钙的悬浊液,试写出反应②中发生的主要反应的化学方程式:_____ 。
(3)操作安全说明中要求反应③开始前“用氮气充分吹扫设备内部”的目的是_____ 。
(4)由下表推知:从Ni(CO)4、Fe(CO)5和Co2(CO)8的混合物中用蒸馏的方法提取Ni(CO)4应选择的温度(T)范围是_____ 。
(5)在以上生产流程中循环使用CO的目的是_____ 。

(1)反应①中,反应物X可能是
(2)石灰浆是氢氧化钙的悬浊液,试写出反应②中发生的主要反应的化学方程式:
(3)操作安全说明中要求反应③开始前“用氮气充分吹扫设备内部”的目的是
(4)由下表推知:从Ni(CO)4、Fe(CO)5和Co2(CO)8的混合物中用蒸馏的方法提取Ni(CO)4应选择的温度(T)范围是
| 物质 | Ni(CO)4 | Fe(CO)5 | Co2(CO)8 |
| 沸点/℃ | 43 | 106 | 52 |
您最近一年使用:0次



