某工厂排放的废液中含有Zn(NO3)2和AgNO3,为回收金属Ag,设计了下列方案:
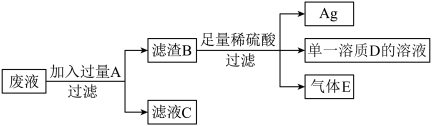
(1)B中含有________ ,滤液C中含有的溶质是________ ,气体E是________ .
(2)写出A与废液中的物质发生反应的化学方程式_______________________ .

(1)B中含有
(2)写出A与废液中的物质发生反应的化学方程式
2020九年级下·全国·专题练习 查看更多[1]
(已下线)拉分练18 工艺流程类推断题(基础)-2020年中考化学拉分题专练—实验探究及推断题
更新时间:2020-04-03 10:14:46
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】铝、铁、铜是生产生活中常见的金属。
(1)下列不属于铝、铁、铜三种金属都具有的性质是___________(填字母)。
(2)为验证铝、铁、铜的金属活动性顺序,化学兴趣小组的同学分别进行了如下实验:(金属片已打磨)

①甲组同学利用图1所示实验得出了金属活动性顺序Al>Fe>Cu,实验中发生反应的化学方程式为___________ 。
②乙组同学按照铁片、铜片、铝片的顺序插入盛有Y溶液的试管中(如图2),充分反应后(能与Y溶液反应的要一次将Y溶液消耗完),也可得出相同的结论,则Y溶液不可能是___________ (填字母)。
A.稀盐酸 B.硝酸铜 C.硫酸亚铁 D.氯化铝
(1)下列不属于铝、铁、铜三种金属都具有的性质是___________(填字母)。
| A.导热性 | B.导电性 | C.有银白色金属光泽 | D.与稀盐酸反应生成氢气 |
(2)为验证铝、铁、铜的金属活动性顺序,化学兴趣小组的同学分别进行了如下实验:(金属片已打磨)

①甲组同学利用图1所示实验得出了金属活动性顺序Al>Fe>Cu,实验中发生反应的化学方程式为
②乙组同学按照铁片、铜片、铝片的顺序插入盛有Y溶液的试管中(如图2),充分反应后(能与Y溶液反应的要一次将Y溶液消耗完),也可得出相同的结论,则Y溶液不可能是
A.稀盐酸 B.硝酸铜 C.硫酸亚铁 D.氯化铝
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐2】A、B、C、D、E、F、G表示初中常见的物质,其中A、B、C、D都是氧化物,E、F、G都是金属单质,A和G均为红色,它们之间的转化关系如图所示(反应条件、部分反应物及生成物已略去)。请回答下列问题:
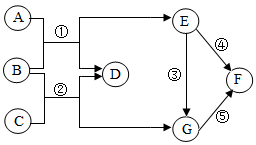
(1)A的化学式为_____ 。
(2)D的一种用途为_____ 。
(3)反应③的微观实质是____________ 。
(4)E、F、G三种金属活动性由强到弱的顺序为___________ ;写出④的化学方程式________ 。

(1)A的化学式为
(2)D的一种用途为
(3)反应③的微观实质是
(4)E、F、G三种金属活动性由强到弱的顺序为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】高纯氧化铁可作为现代电子工业的材料,以下是硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2)为原料制备高纯氧化铁(Fe2O3)的生产流程示意图:

查阅资料:(NH4)2CO3溶液呈碱性,40℃以上时(NH4)2CO3分解。
(1)操作I、操作II的名称________ ,用到的玻璃仪器:玻璃棒、__________ 、烧杯等。
(2)滤液I中的溶质_______________________ 。
(3)在该生产流程中当加入(NH4)2CO3后,应该控制的条件是_________ 。
(4)写出在空气中煅烧FeCO3的化学方程式_______________ 。

查阅资料:(NH4)2CO3溶液呈碱性,40℃以上时(NH4)2CO3分解。
(1)操作I、操作II的名称
(2)滤液I中的溶质
(3)在该生产流程中当加入(NH4)2CO3后,应该控制的条件是
(4)写出在空气中煅烧FeCO3的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】有限的元素可组成种类繁多的物质。依据表中的元素回答下列问题。
(1)能产生温室效应的单质的化学式___________ 。
(2)在我们目前所学知识范围内,若两种非金属氧化物能发生化合反应,则这两种氧化物的化学式可以是___________ 。
(3)写出一种能产生红褐色沉淀的化学方程式____________ 。
(4)A、B、C、D都是上述元素组成的常见物质,它们之间的关系如图所示(图中“一”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系)。
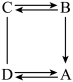
①若A、B都是盐且A不溶于水,则C的化学式为___________ 。
②下列说法不正确的是_____________ 。
A.若A、B都是氧化物,则C、D常温可能为气体
B.若A、B都是氧化物,则C和D反应时可能产生白色沉淀
C.若A、B都是金属单质,则B→A、B→C的反应基本类型相同
D.若A、B都是碱,则C在生活中可用作溶剂
| 元素名称 | 氢 | 碳 | 氧 | 氯 | 钙 | 铁 | 钠 | 铜 |
| 元素符号 | H | C | O | Cl | Ca | Fe | Na | Cu |
(2)在我们目前所学知识范围内,若两种非金属氧化物能发生化合反应,则这两种氧化物的化学式可以是
(3)写出一种能产生红褐色沉淀的化学方程式
(4)A、B、C、D都是上述元素组成的常见物质,它们之间的关系如图所示(图中“一”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系)。

①若A、B都是盐且A不溶于水,则C的化学式为
②下列说法不正确的是
A.若A、B都是氧化物,则C、D常温可能为气体
B.若A、B都是氧化物,则C和D反应时可能产生白色沉淀
C.若A、B都是金属单质,则B→A、B→C的反应基本类型相同
D.若A、B都是碱,则C在生活中可用作溶剂
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐3】A~G是初中化学常见的物质,它们的类别和其中某种元素的化合价构建的相互关系如图所示(图中“→”表示一种物质可生成另一种物质)。已知A能作干燥剂,E中含有两种元素,F中氧元素的质量分数是30%。请回答下列问题:

(1)写出A的另外一种用途:______ 。
(2)写出下列化学方程式:B→C______ ;E与F_______ 。
(3)下列有关叙述正确的是________ (填序号)。
①D→A的反应是高温下的分解反应
②实验室常用E与G的反应制取氢气
③E能分别与B、C、D发生反应
④B→D的转化途径只有一种

(1)写出A的另外一种用途:
(2)写出下列化学方程式:B→C
(3)下列有关叙述正确的是
①D→A的反应是高温下的分解反应
②实验室常用E与G的反应制取氢气
③E能分别与B、C、D发生反应
④B→D的转化途径只有一种
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐1】2019年我国首艘国产航母山东舰正式入列,中国海军正式迈入双航母时代。
(1)建造航母用到了钛合金,工业制钛有一种反应为: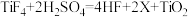 ,X的化学式为
,X的化学式为___________ 。
(2)航母外壳用涂料覆盖是为了防止钢铁材料与_________ 接触而锈蚀,而金属铝在空气中更耐腐蚀的原因是__________ (用化学方程式表示)。
(3)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的是__________ (填序号)。
A 稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉
B ZnCl2溶液中加入足量铁粉后,再加入CuCl2溶液
C ZnCl2溶液中加入足量铜粉后,再加入铁粉
(4)有一包金属粉末,可能由Mg、Zn、Fe、Al、Ag等金属中的一种或几种组成。取该样品4.8g加入100g稀硫酸恰好完全反应,只得到0.4gH2和无色溶液,下列说法正确的是_________ 。
A 样品中一定只含有Mg
B 样品中一定不含有Ag,可能含有Fe
C 稀硫酸的溶质质量分数为9.8%
D 无色溶液中溶质总质量为24g
(1)建造航母用到了钛合金,工业制钛有一种反应为:
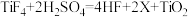 ,X的化学式为
,X的化学式为(2)航母外壳用涂料覆盖是为了防止钢铁材料与
(3)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的是
A 稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉
B ZnCl2溶液中加入足量铁粉后,再加入CuCl2溶液
C ZnCl2溶液中加入足量铜粉后,再加入铁粉
(4)有一包金属粉末,可能由Mg、Zn、Fe、Al、Ag等金属中的一种或几种组成。取该样品4.8g加入100g稀硫酸恰好完全反应,只得到0.4gH2和无色溶液,下列说法正确的是
A 样品中一定只含有Mg
B 样品中一定不含有Ag,可能含有Fe
C 稀硫酸的溶质质量分数为9.8%
D 无色溶液中溶质总质量为24g
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐2】金属制品与我们的日常生活密不可分。
(1)有铝、锌、铜三种金属,其中不能与稀硫酸发生反应的是______ 。
(2)铝的化学性质比较活泼,但铝制品具有很好的抗腐蚀性能,其原因是铝表面容易形成______ 。
(3)为验证Zn、Cu、Ag三种金属的活动性强弱,某同学选用如下试剂组进行验证,其中不合理的一组是______ (用序号①②③填空)
①Zn、 溶液、Ag②
溶液、Ag② 溶液、Cu、
溶液、Cu、 溶液③Zn、Cu、
溶液③Zn、Cu、 溶液
溶液
(4)写出铝丝插入硫酸铜溶液发生反应的化学方程式______ 。
(1)有铝、锌、铜三种金属,其中不能与稀硫酸发生反应的是
(2)铝的化学性质比较活泼,但铝制品具有很好的抗腐蚀性能,其原因是铝表面容易形成
(3)为验证Zn、Cu、Ag三种金属的活动性强弱,某同学选用如下试剂组进行验证,其中不合理的一组是
①Zn、
 溶液、Ag②
溶液、Ag② 溶液、Cu、
溶液、Cu、 溶液③Zn、Cu、
溶液③Zn、Cu、 溶液
溶液(4)写出铝丝插入硫酸铜溶液发生反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】置换反应是化学反应的基本类型之一。
(1)金属与化合物溶液之间的置换反应,一般是活动性比较强的金属可把活动性较弱的金属从其化合物溶液中置换出来,如铁和硫酸铜溶液反应,其化学方程式为_________
(2)非金属单质也具有类似金属与化合物溶液之间的置换反应规律,即活动性较强的非金属可把活动性较弱的非金属从其化合物溶液中置换出来,如在溶液中可发生下列反应;Cl2+2NaBr=2NaCl+Br2;I2+Na2S=2NaI+S↓;Br2+2KI=2KBr+I2
由此可判断:
①S、Cl2、I2、Br2活动性由强到弱顺序是__________ 。
②下列化学方程式书写错误的是__________ 。
A Cl2+2NaI=2NaCl+I2 B I2+2KBr=2KI+Br2
B Br2+Na2S=2NaBr+S↓ D Cl2+K2S=2KCl+S↓
(1)金属与化合物溶液之间的置换反应,一般是活动性比较强的金属可把活动性较弱的金属从其化合物溶液中置换出来,如铁和硫酸铜溶液反应,其化学方程式为
(2)非金属单质也具有类似金属与化合物溶液之间的置换反应规律,即活动性较强的非金属可把活动性较弱的非金属从其化合物溶液中置换出来,如在溶液中可发生下列反应;Cl2+2NaBr=2NaCl+Br2;I2+Na2S=2NaI+S↓;Br2+2KI=2KBr+I2
由此可判断:
①S、Cl2、I2、Br2活动性由强到弱顺序是
②下列化学方程式书写错误的是
A Cl2+2NaI=2NaCl+I2 B I2+2KBr=2KI+Br2
B Br2+Na2S=2NaBr+S↓ D Cl2+K2S=2KCl+S↓
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐1】废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下。
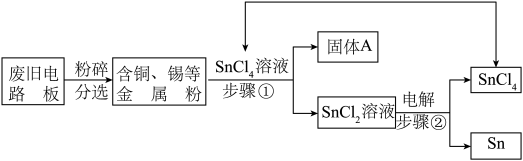
已知:Sn+SnCl4=2SnCl2
(1)SnCl4中锡元素的化合价是_____________________ 。
(2)铜的金属活动性比锡的________ (填“强”或“弱”),固体A中一定含有的金属元素是_______ 。
(3)写出步骤②发生反应的化学方程式________________________________________ 。
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是__________________ (回答一点即可)。

已知:Sn+SnCl4=2SnCl2
(1)SnCl4中锡元素的化合价是
(2)铜的金属活动性比锡的
(3)写出步骤②发生反应的化学方程式
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
【推荐2】闪锌矿(主要成分为ZnS)经焙烧得锌焙砂,锌焙砂主要含ZnO、ZnFe2O4,以及少量CuO,工业上用其制备金属锌,具体过程如图所示。

(1)进行反应①时,要将锌焙砂粉碎成细小颗粒,其目的是_____ ;
(2)ZnFe2O4可看作两种氧化物的结合物,与稀硫酸反应产生两种盐,分别是ZnSO4和____ (填化学式);
(3)参加反应②的物质为ZnSO4和______ (填化学式);
(4)气体M如果直接排放,会造成大气污染,气体M为____ (填名称);
(5)写出反应④的化学方程式:______ 。

(1)进行反应①时,要将锌焙砂粉碎成细小颗粒,其目的是
(2)ZnFe2O4可看作两种氧化物的结合物,与稀硫酸反应产生两种盐,分别是ZnSO4和
(3)参加反应②的物质为ZnSO4和
(4)气体M如果直接排放,会造成大气污染,气体M为
(5)写出反应④的化学方程式:
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】废旧手机的电路板中含有铝、铁、铜、银、金等多种金属,随意丢弃既会造成资源浪费,也会污染土壤和水体。化学兴趣小组为回收其中的铜,设计并进行了如下实验。
已知: ;不考虑金、银发生类似反应。
;不考虑金、银发生类似反应。

(1)电路板粉碎成粉末的目的是___________ ;
(2)滤液 A 中的溶质除硫酸外,还有___________ 、___________ (填化学式);
(3)步骤Ⅱ中的实验现象是:固体部分溶解,___________ ;
(4)步骤Ⅲ中反应的主要化学方程式是___________ ;
(5)上述步骤___________ (选填步骤编号)所包含的反应体现铁的活动性比铜强;
(6)步骤Ⅳ中反应的化学方程式是___________ ;判断步骤Ⅳ中加入的稀硫酸过量的方法是___________ 。
已知:
 ;不考虑金、银发生类似反应。
;不考虑金、银发生类似反应。
(1)电路板粉碎成粉末的目的是
(2)滤液 A 中的溶质除硫酸外,还有
(3)步骤Ⅱ中的实验现象是:固体部分溶解,
(4)步骤Ⅲ中反应的主要化学方程式是
(5)上述步骤
(6)步骤Ⅳ中反应的化学方程式是
您最近一年使用:0次



