解题方法
1 . 我们生活在不断变化的物质世界中,下列变化的主要过程属于物理变化的是
| A.钢铁生锈 | B.葡萄酿酒 | C.塑料老化 | D.海水晒盐 |
您最近一年使用:0次
解题方法
2 . 埋藏地下两千多年的越王勾践剑,出土时锈蚀轻微。下列原因分析错误的是
| A.埋藏的环境中氧气少 | B.剑身表面可能有一层致密的保护膜 |
| C.埋藏的环境非常潮湿 | D.宝剑由抗腐蚀性能好的合金制成 |
您最近一年使用:0次
3 . 《西游记》中描述金箍棒:“棒是九转镔铁炼,老君亲手炉中煅。禹王求得号神珍,四海八河为定验。中间星斗暗铺陈,两头箱裹黄金片。花纹密布神鬼惊,上造龙纹与凤篆”。请回答下列问题:
(1)金箍棒的原材料“镔铁”,是一种钢材料。“镔铁”属于________ (填“合金”或“纯金属”)材料。
(2)金箍棒本是大禹治水时的一个定子,也叫“定海神针”。铁制品易锈蚀是与空气中的______ 和________ 有关,金箍棒在海水中不容易锈蚀的原因是_____ 。
(3)金箍棒表面使“神鬼”惊怕的花纹是用硫酸铁来处理的。制取硫酸铁的原料有铁、稀硫酸、过氧化氢溶液,反应分两步,第一步生成硫酸亚铁和氢气,第二步是向有酸剩余的硫酸亚铁溶液中加入过氧化氢溶液,生成硫酸铁和水。
请写出第一步反应涉及的化学方程式________ ;属于______ (填基本反应类型)反应。
(1)金箍棒的原材料“镔铁”,是一种钢材料。“镔铁”属于
(2)金箍棒本是大禹治水时的一个定子,也叫“定海神针”。铁制品易锈蚀是与空气中的
(3)金箍棒表面使“神鬼”惊怕的花纹是用硫酸铁来处理的。制取硫酸铁的原料有铁、稀硫酸、过氧化氢溶液,反应分两步,第一步生成硫酸亚铁和氢气,第二步是向有酸剩余的硫酸亚铁溶液中加入过氧化氢溶液,生成硫酸铁和水。
请写出第一步反应涉及的化学方程式
您最近一年使用:0次
4 . 中华民族历史悠久,丰富多彩的中华文化记录着中华文明的传承。
(1)二十四节气中立春梅花分外艳,雨水红杏花开鲜。闻到阵阵花香说明分子___________ 。
(2)二十四节气中立秋荞麦白露花,寒露荞麦收到家。种植荞麦时返现土壤显酸性,农民会向田地里撒___________ (写化学式)改良酸性土壤。
(3)饮食文化:大米和面粉滋养了中华儿女。大米和面粉主要成分是淀粉,它能为我们提供的主要营养素是___________ 。
(4)文物锈蚀:汉代铁剪锈迹斑斑(如图所示),其锈蚀是铁与空气中的___________ 发生化学反应的结果。
(5)北宋沈括所著的《梦溪笔谈》中记载了“湿法炼铜”的方法:“熬胆矾铁金,久之亦化为铜”。即在硫酸铜溶液中加入铁,则可得到铜。该反应的化学方程式是___________ 。反应一段时间后溶液还显蓝色,此时溶液中的溶质有___________ 。
(1)二十四节气中立春梅花分外艳,雨水红杏花开鲜。闻到阵阵花香说明分子
(2)二十四节气中立秋荞麦白露花,寒露荞麦收到家。种植荞麦时返现土壤显酸性,农民会向田地里撒
(3)饮食文化:大米和面粉滋养了中华儿女。大米和面粉主要成分是淀粉,它能为我们提供的主要营养素是
(4)文物锈蚀:汉代铁剪锈迹斑斑(如图所示),其锈蚀是铁与空气中的
(5)北宋沈括所著的《梦溪笔谈》中记载了“湿法炼铜”的方法:“熬胆矾铁金,久之亦化为铜”。即在硫酸铜溶液中加入铁,则可得到铜。该反应的化学方程式是
您最近一年使用:0次
解题方法
5 . 下列属于纯净物的是
| A.生锈的铁钉 | B.无色的汽水 | C.淡蓝色的液氧 | D.清澈的河水 |
您最近一年使用:0次
解题方法
6 . 铁在生产、生活中有着广泛的应用。
(1)铁锈蚀实质是铁与空气中的水和_______ 反应。
(2)铁制品表面的铁锈通常可以用_______ (填物质名称)浸泡一段时间即可除去。
(3)工业炼铁原理是利用一氧化碳与氧化铁在高温下反应,该反应的化学方程式为_______ 。
(4)“暖宝宝”利用了铁生锈放热的原理。同学们设计了如表方案对其成分进行探究:
①经过反思,小李认为实验2不能得出固体中有活性炭的结论,理由是_______ (写一点即可)。
②生活中铁制品生锈一般放热不明显,“暖宝宝”打开后却会迅速升温,同学们对此进行了探究。使用如图装置,将3g铁粉、1mL水分别与不同质量的活性炭、食盐均匀混合,测量10min内温度的变化,实验数据见表。请确定实验2中应取用的活性炭的质量。
分析表中数据,可得出的结论是_______ (写一点即可)。
(5)相同条件下铁制品在海水中比在河水中更_______ (选填“难”或“易”)锈蚀。写出一个防止铁质船体生锈的方法_______ 。
(1)铁锈蚀实质是铁与空气中的水和
(2)铁制品表面的铁锈通常可以用
(3)工业炼铁原理是利用一氧化碳与氧化铁在高温下反应,该反应的化学方程式为
(4)“暖宝宝”利用了铁生锈放热的原理。同学们设计了如表方案对其成分进行探究:
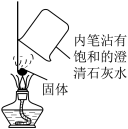
| 序号 | 实验步骤 | 实验现象 | 实验结论 | 内壁涂有饱和固体的澄清石灰水 |
| 1 | 取少量固体于试管中,加入足量稀硫酸 | 有气泡生产 | “暖宝宝”中有铁粉 | |
| 2 | 取少量固体于燃烧匙中,用酒精灯加热,上方罩一个内壁涂有饱和的澄清石灰水的烧杯(如图) | “暖宝宝”中有活性炭 | ||
| 3 | 取少量固体于烧杯中,加入足量水溶解,过滤,往滤液中滴加少量 | 产生白色沉淀 | '暖宝宝“中有氯化钠 |
②生活中铁制品生锈一般放热不明显,“暖宝宝”打开后却会迅速升温,同学们对此进行了探究。使用如图装置,将3g铁粉、1mL水分别与不同质量的活性炭、食盐均匀混合,测量10min内温度的变化,实验数据见表。请确定实验2中应取用的活性炭的质量。
| 实验编号 | 活性炭质量/g | 食盐质量/g | 温度上升值/℃ |
| 1 | 0 | 0 | 0.1 |
| 2 | 0 | 11.6 | |
| 3 | 0 | 1 | 4.2 |
| 4 | 0.5 | 1 | 20.3 |
(5)相同条件下铁制品在海水中比在河水中更
您最近一年使用:0次
解题方法
7 . 分类思想在化学学习中应用广泛,以下物质属于纯净物的是
| A.洁净的空气 | B.铁锈 | C.冰水混合物 | D.稀有气体 |
您最近一年使用:0次
解题方法
8 . 化学变化常常伴随一些现象。下列物质发生变化时出现的现象不是由化学变化引起的是
| A.生石灰与水混合后放热 | B.稀有气体通电后发出不同颜色的光 |
| C.黑色的铁粉锈蚀变为红色 | D.白醋加到水垢中有气泡生成 |
您最近一年使用:0次
解题方法
9 . 化学小组的同学对“暖宝宝”(标签如下图)感到好奇,进行了一系列探究活动。
【查阅资料】
①蛭石:一种天然矿物,加工后具有极强的保温隔热性能。
②吸水性树脂:一种新型高分子材料,吸水能力强,可反复吸收水、释放水。
③暖宝宝的发热原理是铁粉吸氧腐蚀过程中放出热量。加入活性炭能形成微电池,反应更快。
(1)请补全铁吸氧腐蚀的总反应方程式: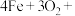
___________ 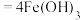 ;
;
【提出问题1】
如何证明“暖宝宝”袋内含有铁粉?
【进行实验】
①取出袋内粉末于滤纸上,用磁铁充分吸引。
②将少量磁铁吸出的粉末置于试管内,加入足量稀盐酸。
【观察现象】
(2)磁铁吸出的粉末与稀盐酸反应,___________ 。
【得出结论】
袋内含有铁粉。
【提出问题2】
哪些因素会影响铁吸氧腐蚀的速率?
【进行实验】
小组同学设计了如图所示的实验装置,进行如下5组实验。
每组实验加入的铁炭总质量为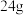 ,食盐水体积为
,食盐水体积为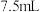 ,恰好能将固体润湿。
,恰好能将固体润湿。
【解释与结论】
(3)通过实验发现,铁炭质量比对铁吸氧腐蚀速率的影响是___________ 。
(4)要分析食盐水浓度对铁吸氧腐蚀速率的影响,应对比实验___________ (填实验序号)。
(5)示数差 是指U型管左侧液面比右侧液面高
是指U型管左侧液面比右侧液面高 。出现该现象的原因是
。出现该现象的原因是___________ 。
【反思与评价】
(6)依据以上实验,你认为最佳原料配比为第几组,并说明理由___________ 。
【查阅资料】
①蛭石:一种天然矿物,加工后具有极强的保温隔热性能。
②吸水性树脂:一种新型高分子材料,吸水能力强,可反复吸收水、释放水。
③暖宝宝的发热原理是铁粉吸氧腐蚀过程中放出热量。加入活性炭能形成微电池,反应更快。
| 【产品名称】一次性发热贴 【主要成分】铁粉、活性炭、水、吸水性树脂、食盐、蛭石 【产品性能】平均温度53℃,持续时间≥10h |
(1)请补全铁吸氧腐蚀的总反应方程式:
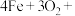
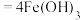 ;
;【提出问题1】
如何证明“暖宝宝”袋内含有铁粉?
【进行实验】
①取出袋内粉末于滤纸上,用磁铁充分吸引。
②将少量磁铁吸出的粉末置于试管内,加入足量稀盐酸。
【观察现象】
(2)磁铁吸出的粉末与稀盐酸反应,
【得出结论】
袋内含有铁粉。
【提出问题2】
哪些因素会影响铁吸氧腐蚀的速率?
【进行实验】
小组同学设计了如图所示的实验装置,进行如下5组实验。
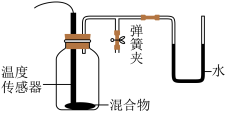
每组实验加入的铁炭总质量为
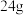 ,食盐水体积为
,食盐水体积为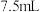 ,恰好能将固体润湿。
,恰好能将固体润湿。| 序号 | 铁炭质量比 | 食盐水浓度/% | 示数差3cm所用时间/s | 10分钟时温度升高值/℃ |
| ① |  | 26 | 90 | 7.8 |
| ② |  | 26 | 170 | 4.2 |
| ③ | 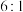 | 26 | 190 | 3.3 |
| ④ |  | 13 | 140 | 6 |
| ⑤ |  | 6.5 | 150 | 6 |
(3)通过实验发现,铁炭质量比对铁吸氧腐蚀速率的影响是
(4)要分析食盐水浓度对铁吸氧腐蚀速率的影响,应对比实验
(5)示数差
 是指U型管左侧液面比右侧液面高
是指U型管左侧液面比右侧液面高 。出现该现象的原因是
。出现该现象的原因是【反思与评价】
(6)依据以上实验,你认为最佳原料配比为第几组,并说明理由
您最近一年使用:0次
名校
解题方法
10 . 金属活动性顺序表是研究金属性质的重要工具,请回答问题:
金属材料的使用作为一个时代的标志,见证了人类文明发展的过程。历史上人类冶炼不同金属的大致年代如图。______ 的物理性质。
(2)铁、铜、铝使用的先后顺序由先到后是______ 。
(3)为验证Fe、Cu、Ag三种金属的活动性顺序,下列选用的药品可行的是______(填字母)。
(4)酸雨多发地区钢铁易受腐蚀,这是因为酸雨中含有的极少量硫酸会与铁发生反应,反应的化学方程式是______ 。
(5)下列有关金属材料的叙述错误的是______。
金属材料的使用作为一个时代的标志,见证了人类文明发展的过程。历史上人类冶炼不同金属的大致年代如图。
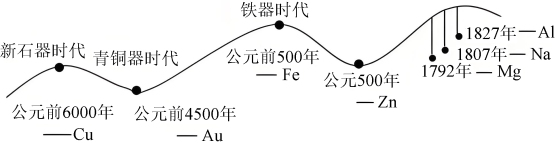
(2)铁、铜、铝使用的先后顺序由先到后是
(3)为验证Fe、Cu、Ag三种金属的活动性顺序,下列选用的药品可行的是______(填字母)。
| A.Fe、CuSO4溶液、Ag | B.FeSO4溶液、Cu、Ag |
| C.Fe2(SO4)3溶液、Cu、AgNO3溶液 | D.FeSO4溶液、CuSO4溶液、Ag |
(4)酸雨多发地区钢铁易受腐蚀,这是因为酸雨中含有的极少量硫酸会与铁发生反应,反应的化学方程式是
(5)下列有关金属材料的叙述错误的是______。
| A.回收利用废旧电池中的铅、汞等可减少对环境的污染 |
| B.铝块能制成铝箔是利用了铝的延展性 |
| C.铝比钢铁中的铁活泼,因而铝的抗腐蚀性能比铁差 |
| D.防止铁制品锈蚀的办法有很多,例如在铁制品表面刷漆或镀耐腐蚀金属,我国中科院研发出了复层脂包覆密封材料,都是有效隔绝了氧气和水 |
您最近一年使用:0次



