铁在生产、生活中有着广泛的应用。
(1)铁锈蚀实质是铁与空气中的水和_______ 反应。
(2)铁制品表面的铁锈通常可以用_______ (填物质名称)浸泡一段时间即可除去。
(3)工业炼铁原理是利用一氧化碳与氧化铁在高温下反应,该反应的化学方程式为_______ 。
(4)“暖宝宝”利用了铁生锈放热的原理。同学们设计了如表方案对其成分进行探究:
①经过反思,小李认为实验2不能得出固体中有活性炭的结论,理由是_______ (写一点即可)。
②生活中铁制品生锈一般放热不明显,“暖宝宝”打开后却会迅速升温,同学们对此进行了探究。使用如图装置,将3g铁粉、1mL水分别与不同质量的活性炭、食盐均匀混合,测量10min内温度的变化,实验数据见表。请确定实验2中应取用的活性炭的质量。
分析表中数据,可得出的结论是_______ (写一点即可)。
(5)相同条件下铁制品在海水中比在河水中更_______ (选填“难”或“易”)锈蚀。写出一个防止铁质船体生锈的方法_______ 。
(1)铁锈蚀实质是铁与空气中的水和
(2)铁制品表面的铁锈通常可以用
(3)工业炼铁原理是利用一氧化碳与氧化铁在高温下反应,该反应的化学方程式为
(4)“暖宝宝”利用了铁生锈放热的原理。同学们设计了如表方案对其成分进行探究:
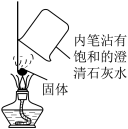
| 序号 | 实验步骤 | 实验现象 | 实验结论 | 内壁涂有饱和固体的澄清石灰水 |
| 1 | 取少量固体于试管中,加入足量稀硫酸 | 有气泡生产 | “暖宝宝”中有铁粉 | |
| 2 | 取少量固体于燃烧匙中,用酒精灯加热,上方罩一个内壁涂有饱和的澄清石灰水的烧杯(如图) | “暖宝宝”中有活性炭 | ||
| 3 | 取少量固体于烧杯中,加入足量水溶解,过滤,往滤液中滴加少量 | 产生白色沉淀 | '暖宝宝“中有氯化钠 |
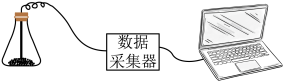
②生活中铁制品生锈一般放热不明显,“暖宝宝”打开后却会迅速升温,同学们对此进行了探究。使用如图装置,将3g铁粉、1mL水分别与不同质量的活性炭、食盐均匀混合,测量10min内温度的变化,实验数据见表。请确定实验2中应取用的活性炭的质量。
| 实验编号 | 活性炭质量/g | 食盐质量/g | 温度上升值/℃ |
| 1 | 0 | 0 | 0.1 |
| 2 | 0 | 11.6 | |
| 3 | 0 | 1 | 4.2 |
| 4 | 0.5 | 1 | 20.3 |
(5)相同条件下铁制品在海水中比在河水中更
更新时间:2024-05-25 08:54:39
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】人类生活离不开金属。
(1)铁是生活中常用的金属。某“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热。
①发热剂需接触到空气才会发热,原因是铁要与_________ 等物质共同作用会生锈。
(2)应用金属活动性顺序能帮助我们进一步学习金属性质。
①已知下列各组物质间均能发生置换反应。
A、Fe和CuSO4溶液 B、Mg和MnSO4溶液 C、Mn和FeSO4溶液
Mn、Fe、Mg、Cu四种金属的活动性由强到弱的顺序_____________ 。
②利用下列各组药品,能完成验证锌、铁、铜活动性顺序的是____________ (填序号)
A. Zn、Cu、FeSO4溶液
B. Fe、Cu、ZnSO4溶液
C. Cu、ZnSO4溶液、FeSO4溶液
D. Fe、ZnSO4溶液、CuSO4溶液
(1)铁是生活中常用的金属。某“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热。
①发热剂需接触到空气才会发热,原因是铁要与
(2)应用金属活动性顺序能帮助我们进一步学习金属性质。
①已知下列各组物质间均能发生置换反应。
A、Fe和CuSO4溶液 B、Mg和MnSO4溶液 C、Mn和FeSO4溶液
Mn、Fe、Mg、Cu四种金属的活动性由强到弱的顺序
②利用下列各组药品,能完成验证锌、铁、铜活动性顺序的是
A. Zn、Cu、FeSO4溶液
B. Fe、Cu、ZnSO4溶液
C. Cu、ZnSO4溶液、FeSO4溶液
D. Fe、ZnSO4溶液、CuSO4溶液
您最近一年使用:0次
【推荐2】化学来源于生活,服务于生活,请你用学到的化学知识解决日常生活中的问题。
问题一、熟练运用燃烧和灭火的知识是同学们应该具备的基本科学素养。

(1)图甲中能够发生燃烧的是______ (选填“a”“b”或“c”)处,气球在实验过程中的变化情况是______ 。
(2)图乙中“用手摁灭烟头”主要的灭火原理是____________ 。
问题二、食品保鲜的措施有添加防腐剂、填充气体、放置干燥剂和脱氧保鲜剂等。
(3)如图是钠元素在元素周期中的部分信息,下列有关说法中正确的是______(填字母)。
(4)铁粉属于脱氧保鲜剂,又称“双吸剂”,其保鲜原理是铁粉与包装袋中的______ 发生化学反应;有的要放置一小包生石灰,作用是____________ (用化学方程式表示)。
问题一、熟练运用燃烧和灭火的知识是同学们应该具备的基本科学素养。

(1)图甲中能够发生燃烧的是
(2)图乙中“用手摁灭烟头”主要的灭火原理是
问题二、食品保鲜的措施有添加防腐剂、填充气体、放置干燥剂和脱氧保鲜剂等。
(3)如图是钠元素在元素周期中的部分信息,下列有关说法中正确的是______(填字母)。
| A.钠元素属于非金属元素 | B.钠的相对原子质量为22.99g |
| C.钠原子核外共有11个电子 | D.钠离子的符号为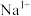 |
(4)铁粉属于脱氧保鲜剂,又称“双吸剂”,其保鲜原理是铁粉与包装袋中的
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】孔雀石又称石绿,主要成分是碱式碳酸铜[Cu2(OH)2CO3]。

(1)石绿可做中国画颜料,不易褪色能保存数百年,说明碱式碳酸铜具有_____ 的性质。
(2)孔雀石是冶炼铜的工业原料,流程如图1。
步骤a:原理是Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑,生产前孔雀石需研磨成粉末的原因是_____ 。
步骤b:金属粉末通常选铁粉是因为铁具有_____ 的性质,铁粉需过量加入的原因是_____ 。
(3)在实验室中,加热11.1g的Cu2(OH)2CO3粉末,剩余固体质量及成分随温度变化的曲线如图2。温度高于_____ ℃时,Cu2(OH)2CO3开始分解得到CuCO3、CuO及一种常温下的常见液态物质;ab段,剩余固体没有减少的原因是_____ ;温度高于1000℃时,CuO受热分解,得到氧气和一种红色物质,写出该物质的化学式_____ 。

(1)石绿可做中国画颜料,不易褪色能保存数百年,说明碱式碳酸铜具有
(2)孔雀石是冶炼铜的工业原料,流程如图1。
步骤a:原理是Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑,生产前孔雀石需研磨成粉末的原因是
步骤b:金属粉末通常选铁粉是因为铁具有
(3)在实验室中,加热11.1g的Cu2(OH)2CO3粉末,剩余固体质量及成分随温度变化的曲线如图2。温度高于
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】A~G是常见的7种物质,其中A为黑色固体,A、E、F为单质,B是易与血红蛋白结合的有毒气体,B、D的组成元素相同,反应①是工业用赤铁矿炼铁的主要反应,F为红色固体,G为黄色溶液。(部分反应条件已略去)。请回答:
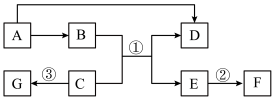
(1)写出由A生成B的的化学反应方程式_______ 。
(2)反应②的现象是_______ 。
(3)反应③的化学方程式_______ 。

(1)写出由A生成B的的化学反应方程式
(2)反应②的现象是
(3)反应③的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐3】制造芯片的基材主要是高纯硅。下图是制备高纯硅的一种工艺流程:
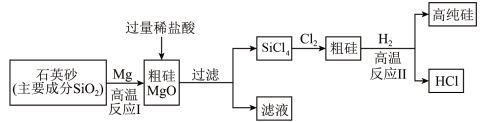
回答下列问题:
(1)反应Ⅰ的化学方程式是_____________________ 。
(2)过滤所得粗硅应充分洗涤,以除去表面可能吸附的HCl和____________ (填化学式)。
(3)反应Ⅱ的基本类型属于_____________ ;反应Ⅱ要在无氧气环境中进行,原因是____________ (答出一种即可)。
(4)上述生产流程中,可以循环利用的物质是____________ (填化学式)。

回答下列问题:
(1)反应Ⅰ的化学方程式是
(2)过滤所得粗硅应充分洗涤,以除去表面可能吸附的HCl和
(3)反应Ⅱ的基本类型属于
(4)上述生产流程中,可以循环利用的物质是
您最近一年使用:0次
【推荐1】有一包白色粉末可能含有硫酸钡、碳酸钾和氢氧化钡中的一种或几种,取一定量该粉末加入到盛有足量水的烧杯中,搅拌、静置,观察到烧杯中有白色不溶物。进一步确定白色固体成分,进行如下实验探究:
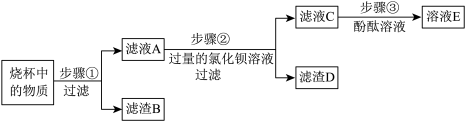
(1)步骤②中发生化学反应的方程式是_______ 。
(2)请完成下面的表格。
(3)若要证明原白色粉末中只含有碳酸钾和氢氧化钡,你的实验方案是_______ (写实验操作和现象)。

(1)步骤②中发生化学反应的方程式是
(2)请完成下面的表格。
| 实验操作 | 现象 | 结论 |
| 步骤③中,加入酚酞溶液 | 若溶液E为无色 | 原白色粉末的组成是 |
| 若溶液E为红色 | 滤液A中一定含有的溶质是 原白色粉末的可能组成分别是 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】化学是在原子、分子水平上研究物质及其变化的学科。
(1)如图是元素周期表中某些元素的原子结构示意图:
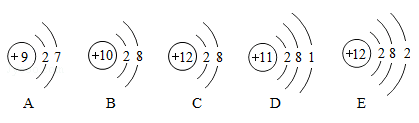
①微粒E最外层电子数是__________ ,在化学反应中容易______ (填“得到”或 “失去)电子形成离子,离子符号为___________ 。
②微粒A、B、C、D、E中,属于同种元素的是________ (填编号)。
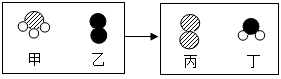
(2)一定条件下,甲和乙反应生成丙和工(四种物质均由分子构成),反应前后微观示意图如下。下列说法正确的是__________。
(3)胃酸过多须服用抗酸药。下表为两种抗酸药的有效成分及其构成微粒:
由于抗酸药有效成分不同,起抗酸作用(即消耗胃液中盐酸)的微粒也有差异。
①Mg(OH)2起抗酸作用的微粒是__________ (填微粒符号,下同)。
②铝碳酸镁与盐酸的反应为AlMg(OH)3CO3+5HCl=MgCl2+AlCl3+4H2O+CO2↑。则铝碳酸镁起抗酸作用的两种微粒是_________ 、_________ 。
(1)如图是元素周期表中某些元素的原子结构示意图:

①微粒E最外层电子数是
②微粒A、B、C、D、E中,属于同种元素的是
(2)一定条件下,甲和乙反应生成丙和工(四种物质均由分子构成),反应前后微观示意图如下。下列说法正确的是__________。

| A.反应前后共有4种原子 |
| B.该反应有单质生成 |
| C.反应前后元素化合价都不变 |
| D.化学变化中分子和原于均可再分 |
| E.该化学反应中,甲、丁两种分子的个数比是2:3 |
| 抗胃酸药 | 复方氢氧化镁片剂 | 铝碳酸镁片 |
| 有效成分 | Mg(OH)2 | AlMg(OH)3CO3 |
| 构成微粒 | Mg2+、OH- | Al3+、Mg2+、OH-、 |
①Mg(OH)2起抗酸作用的微粒是
②铝碳酸镁与盐酸的反应为AlMg(OH)3CO3+5HCl=MgCl2+AlCl3+4H2O+CO2↑。则铝碳酸镁起抗酸作用的两种微粒是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐1】某金属加工厂有大量金属铝、铁、铜的废弃粉末,为充分利用金属资源,分离和回收金属,某化学兴趣小组通过查阅资料设计了如下实验方案:

请完成下列各题:
(1)步骤①中分离得到的金属B是_______ 。
(2)步骤②发生的化学反应方程式是_________________ 。
(3)步骤③生成沉淀的化学反应方程式是_____________________ ;因Al(OH)3既能与酸反应又能与碱反应,步骤③加入试剂时应如何操作_________________________ 。
(4)电解熔融Al2O3制金属铝的化学方程式是______________________ 。

请完成下列各题:
(1)步骤①中分离得到的金属B是
(2)步骤②发生的化学反应方程式是
(3)步骤③生成沉淀的化学反应方程式是
(4)电解熔融Al2O3制金属铝的化学方程式是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】在活动探究课上,老师拿来一包由氯化钠、碳酸钠、碳酸氢钠三种物质中取出的两种物质等质量混合而成的白色粉末和一瓶没有标签的未知酸溶液,请各实验小组同学进行成分确定。甲小组同学查阅课本后设计了如下实验方案:

若他们测知,A为人的正常生理活动所必须不可少的物质,B能使澄清石灰水变浑浊。 请回答下列问题:
(1)写出物质名称:B_______ ,未知酸溶液 ______ 。
(2)这包白色粉末的组成可能是_________ ;有关反应的化学方程式为 ________ 。
(3)若乙小组的同学取10g白色粉末也按照甲组同学的方案进行实验,他们最终得到固体的质量为8.5g。你认为这包白色粉末的组成可能是_________ 。

若他们测知,A为人的正常生理活动所必须不可少的物质,B能使澄清石灰水变浑浊。 请回答下列问题:
(1)写出物质名称:B
(2)这包白色粉末的组成可能是
(3)若乙小组的同学取10g白色粉末也按照甲组同学的方案进行实验,他们最终得到固体的质量为8.5g。你认为这包白色粉末的组成可能是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐3】现有一包固体粉末,可能含有C粉、KMnO4、NaCl、NH4HCO3、MnO2中的一种或几种。现做如下实验:
(1)取少量固体加热,无氨味,则原固体中一定不含___________ 。
(2)另取少量固体溶于足量水过滤,得到无色澄清滤液和黑色固体,则原固体中一定不含___________ 。
(3)取(2)中无色澄清滤液适量,蒸发,出现较多固体,则原固体中一定含有___________ 。
(4)取(2)中黑色固体,加入5%的双氧水,有气体放出,由此判断原固体中还含有___________ 。
(5)待(4)中不再产生气泡,仍有固体剩余,则原固体中___________ (填“一定”、“一定不”或“可能”)含有C粉
(1)取少量固体加热,无氨味,则原固体中一定不含
(2)另取少量固体溶于足量水过滤,得到无色澄清滤液和黑色固体,则原固体中一定不含
(3)取(2)中无色澄清滤液适量,蒸发,出现较多固体,则原固体中一定含有
(4)取(2)中黑色固体,加入5%的双氧水,有气体放出,由此判断原固体中还含有
(5)待(4)中不再产生气泡,仍有固体剩余,则原固体中
您最近一年使用:0次



