2022年贵州省安顺市平坝区乐平中学中考模拟化学试题14
贵州
九年级
模拟预测
2022-08-04
118次
整体难度:
适中
考查范围:
物质的化学变化、身边的化学物质、化学实验、化学与社会发展、物质构成的奥秘
2022年贵州省安顺市平坝区乐平中学中考模拟化学试题14
贵州
九年级
模拟预测
2022-08-04
118次
整体难度:
适中
考查范围:
物质的化学变化、身边的化学物质、化学实验、化学与社会发展、物质构成的奥秘
一、选择题 添加题型下试题
选择题-单选题
|
容易(0.94)
解题方法
1. 下列相关防控新冠肺炎疫情的措施中发生了化学变化的是
| A.裁剪熔喷布制作口罩 | B.喷洒含氯消毒液杀菌 |
| C.配制75%的医用酒精 | D.用水银温度计测量体温 |
【知识点】 化学变化与物理变化判断解读
您最近一年使用:0次
2022-08-03更新
|
210次组卷
|
2卷引用:2022年贵州省安顺市平坝区乐平中学中考模拟化学试题14
选择题-单选题
|
较易(0.85)
名校
解题方法
2. 小涂同学参加中考化学实验操作考试时,抽到的题目是二氧化碳的制取和部分性质检验。以下是他的实验操作,其中操作正确的是
A.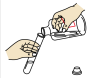 倾倒紫色石蕊溶液 倾倒紫色石蕊溶液 | B. 组装气体发生装置 组装气体发生装置 |
C. 加热石蕊溶液 加热石蕊溶液 | D. 熄灭酒精灯 熄灭酒精灯 |
您最近一年使用:0次
2022-06-10更新
|
144次组卷
|
6卷引用:2022年江西省中考模拟化学试题
2022年江西省中考模拟化学试题2022年贵州省安顺市平坝区乐平中学中考模拟化学试题14(已下线)基础实验2 二氧化碳的制取与性质(练习)-2022-2023学年九年级化学上册同步精品课堂(沪教版)(已下线)黄金卷06-【赢在中考·黄金8卷】备战2023年中考化学全真模拟卷(苏州专用)江西省南昌一中教育集团2023-2024 学年九年级上学期期末阶段性学习质量检测化学试卷江西省新余市第四中学2023-2024学年九年级下学期开学考试化学试题
选择题-单选题
|
容易(0.94)
解题方法
3. 碳中和是指通过植树造林、节能减排,抵消产生的CO2排放量,实现二氧化碳“零排放”列说法正确的是
| A.实现CO2“零排放”,必须禁止使用化石燃料 |
| B.自然界中的CO2主要来自生物的呼吸作用 |
| C.大气中CO2含量过高会导致酸雨现象 |
| D.提倡“低碳生活”,大力推广风能、太阳能等新能源 |
您最近一年使用:0次
选择题-单选题
|
较易(0.85)
名校
解题方法
4. 2022年2月21日,我国科研人员领衔的国际科研团队攻克了催化研究中的世界性难题一甲烷的选择性氧化,其微观反应过程如图所示。下列说法不正确的是
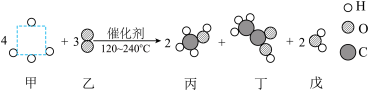

A.虚线框内应补充的是“ ” ” |
| B.反应生成丙、丁两物质的质量比为2:1 |
| C.在化学变化中,分子可分,原子不可再分 |
| D.该反应与甲烷燃烧相比,条件不同产物不同 |
您最近一年使用:0次
2022-06-17更新
|
86次组卷
|
3卷引用:2022年陕西省中考考前模拟冲刺化学试题
选择题-单选题
|
较易(0.85)
解题方法
5. 下列实验不能达到目的的是
| A | B | C | M |
 |  |  |  |
| 测定空气中氧气 | 探究铁生锈的条件 | 探究可燃物燃烧需要与氧气接触 | 鉴别NH4Cl溶液和KCl溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-06-19更新
|
40次组卷
|
2卷引用:2022年陕西省中考考前模拟冲刺化学试题
选择题-单选题
|
适中(0.65)
解题方法
6. 甲、乙为初中化学常见的两种物质,两者之间存在如图转化关系。下列说法不正确的是
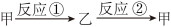
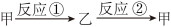
| A.若甲为CaCl2,乙为CaCO3,则反应②可用于实验室制取CO2 |
| B.若甲为CO2,乙为CO,则反应①、②的基本反应类型可能相同 |
| C.若甲为CuSO4,乙为Cu(OH)2,则反应①中溶液质量一定减小 |
| D.若甲为H2O,乙为O2,则反应②中的另一反应物可以是化合物或单质 |
您最近一年使用:0次
2022-06-17更新
|
41次组卷
|
2卷引用:2022年陕西省中考考前模拟冲刺化学试题
二、填空与简答 添加题型下试题
填空与简答-填空题
|
适中(0.65)
解题方法
7. 2022年2月,第24届冬奥会在中国北京成功举行。
(1)①科技冬奥:运动员所穿的衣服中含有石墨烯发热材料,供电后石墨烯发热材料能够产生较高热量,这体现了石墨烯的导热性和_________ 性。
②人文冬奥:冬奥会火炬设计灵感源自青铜材质的“中华第一灯”——西汉长信宫灯。青铜与纯铜相比,硬度______ (填“增大”或“减小”)。
③绿色冬奥:冬奥会首次采用二氧化碳跨临界直冷制冰技术。二氧化碳的循序利用能有效缓解的环境问题是___________________________ 。
④这次北京冬奥会把奥运火炬更改为小火炬,也进一步体现了绿色奥运,你认为这样做的原因是______________________ 。
(2)2022年3月,新冠肺炎疫情呈散发态势,全国人民调集大量物资支援上海与吉林。
①建设上海方舱医院使用的PVC(聚氯乙烯)塑胶地板属于_______ (填选项字母,下同)
A 天然材料 B 合成材料 C 金属材料 D复合材料
②志愿者为居民运送的食品有肉类、鸡蛋、高钙牛奶、大米、菜籽油、碘盐等。为保证人体营养均衡,还应补充的营养素是__________ 。
A 糖类 B 维生素 C 无机盐 D 油脂
③志愿者送来的高钙牛奶中,“钙”可预防的疾病是__________ 。
A 骨质疏松 B 夜盲症 C 甲状腺肿大 D 败血病
(1)①科技冬奥:运动员所穿的衣服中含有石墨烯发热材料,供电后石墨烯发热材料能够产生较高热量,这体现了石墨烯的导热性和
②人文冬奥:冬奥会火炬设计灵感源自青铜材质的“中华第一灯”——西汉长信宫灯。青铜与纯铜相比,硬度
③绿色冬奥:冬奥会首次采用二氧化碳跨临界直冷制冰技术。二氧化碳的循序利用能有效缓解的环境问题是
④这次北京冬奥会把奥运火炬更改为小火炬,也进一步体现了绿色奥运,你认为这样做的原因是
(2)2022年3月,新冠肺炎疫情呈散发态势,全国人民调集大量物资支援上海与吉林。
①建设上海方舱医院使用的PVC(聚氯乙烯)塑胶地板属于
A 天然材料 B 合成材料 C 金属材料 D复合材料
②志愿者为居民运送的食品有肉类、鸡蛋、高钙牛奶、大米、菜籽油、碘盐等。为保证人体营养均衡,还应补充的营养素是
A 糖类 B 维生素 C 无机盐 D 油脂
③志愿者送来的高钙牛奶中,“钙”可预防的疾病是
A 骨质疏松 B 夜盲症 C 甲状腺肿大 D 败血病
您最近一年使用:0次
8. 造纸术、指南针、火药、印刷术并称四大发明,是中国古代劳动人民卓越的智慧成果。

(1)纸张的主要成分是植物纤维,棉纤维是植物纤维的一种,棉纤维燃烧时有_______ 气味产生。
(2)指南针由天然磁石制成,天然磁石的主要成分是四氧化三铁,还含有钴镍等,这里的“钴”“镍”指_______ (填“元素”“原子”或“分子”)。
(3)黑火药是用硝酸钾、炭粉和硫磺按一定比例混合制成的,黑火药爆炸后不可能生成_______(填字母)。
(4)活字印刷的步骤是制模挑字、排版、涂墨、上纸印刷。用墨印刷的字画能够长久保存而不变色,是因为_______ 。

(1)纸张的主要成分是植物纤维,棉纤维是植物纤维的一种,棉纤维燃烧时有
(2)指南针由天然磁石制成,天然磁石的主要成分是四氧化三铁,还含有钴镍等,这里的“钴”“镍”指
(3)黑火药是用硝酸钾、炭粉和硫磺按一定比例混合制成的,黑火药爆炸后不可能生成_______(填字母)。
| A.K2S | B.H2O | C.CO2 | D.N2 |
您最近一年使用:0次
2022-06-17更新
|
75次组卷
|
3卷引用:2022年陕西省中考考前模拟冲刺化学试题
9. 2022年4月16日,神舟十三号载人飞船与空间站天和核心舱成功分离,三名航天员顺利返回地球。
(1)航天员进行出舱任务时所穿的航天服使用了聚氨酯材料,聚氨酯材料属于_______ (填“有机合成”或“无机非金属”)材料。
(2)载人空间站内气体中多余的二氧化碳可用分子筛设备分离出来,其原理类似于实验室中的_______ 操作。
(3)航天员呼出的水蒸气经冷凝、净化后可作为核心舱中的饮用水,水蒸气冷凝为水的微观实质是_______ 。
(4)空间站的梦天实验舱搭载三组冷原子钟,由氢原子钟、铷原子钟和光学钟组成。如图所示是铷元素在元素周期表中的部分信息,铷的相对原子质量是_______ 。

(1)航天员进行出舱任务时所穿的航天服使用了聚氨酯材料,聚氨酯材料属于
(2)载人空间站内气体中多余的二氧化碳可用分子筛设备分离出来,其原理类似于实验室中的
(3)航天员呼出的水蒸气经冷凝、净化后可作为核心舱中的饮用水,水蒸气冷凝为水的微观实质是
(4)空间站的梦天实验舱搭载三组冷原子钟,由氢原子钟、铷原子钟和光学钟组成。如图所示是铷元素在元素周期表中的部分信息,铷的相对原子质量是

您最近一年使用:0次
2022-06-17更新
|
36次组卷
|
2卷引用:2022年陕西省中考考前模拟冲刺化学试题
10. 如图1是硝酸钾和氯化钾的溶解度曲线。某小组进行如图2所示实验,所用的X物质是硝酸钾或氯化钾中的一种。

(1)物质X是__________ (填“硝酸钾”或“氯化钾”)。
(2)t1℃时,物质X的溶解度是_______________ 。
(3)烧杯A内的溶液是____________ (填“饱和”或“不饱和”)溶液。
(4)若烧杯B→烧杯C采用如图3所示方式降温,则固体R可以是___________ 。
(5)t2℃时,将35g的硝酸钾加到50g水中,得到的溶液质量为__________ 。

(1)物质X是
(2)t1℃时,物质X的溶解度是
(3)烧杯A内的溶液是
(4)若烧杯B→烧杯C采用如图3所示方式降温,则固体R可以是
(5)t2℃时,将35g的硝酸钾加到50g水中,得到的溶液质量为
您最近一年使用:0次
三、科学探究题 添加题型下试题
科学探究题
|
适中(0.65)
解题方法
11. 舞蹈诗剧《只此青绿》生还原了北宋名画《千里江山图》。《千里江山图》绘制时使用了石青、石绿等颜料,其中石绿的原料是孔雀石,主要成分是碱式碳酸铜【Cu2(OH)2CO3】。化学小组同学对碱式碳酸铜进行了如下探究。
I.探究碱式碳酸铜受热的变化情况。
【查阅资料】①碱式碳酸铜的物质类别是盐。
②碱式碳酸铜受热分解生成三种氧化物。
【提出问题】碱式碳酸铜受热分解生成哪些物质?
【猜想与假设】可能会生成CuO、CO2和______ 。
【设计实验】同学们设计了下图所示实验装置探究碱式碳酸铜的分解产物。(假设装置B、C、D中的药品足量,忽略反应后装置A中残留的气体)。

【实验过程】
(1)在装置D的导管a处连接一导管,并插入水中,微热试管,观察到导管口有气泡冒出,这一实验步骤的目的是______ 。
(2)向装置A的试管中加入碱式碳酸铜,用酒精灯加热至试管内固体质量不再改变。
【现象与结论】
装置A中绿色固体变黑,装置B中白色固体变蓝,并增重mg,装置C中增重ng,且m:n=_____ (填最简整数比)。通过这些现象证明,上述猜想正确。
【实验反思】
如果上图装置中缺少装置D,则此时测定的m:n的值和“现象与结论”中你填写的值相比,会____ (选填“变大”、“变小”或“不变”)。
Ⅱ.探究碱式碳酸铜中的碳酸根离子。
上述实验步骤中X溶液为_______ ,充分反应后左侧试管内溶液中的阳离子有______ (写离子符号)。
【拓展提升】古代人们发现在孔雀石上燃烧炭火会有红色固体生成,该红色固体是_____ 。
I.探究碱式碳酸铜受热的变化情况。
【查阅资料】①碱式碳酸铜的物质类别是盐。
②碱式碳酸铜受热分解生成三种氧化物。
【提出问题】碱式碳酸铜受热分解生成哪些物质?
【猜想与假设】可能会生成CuO、CO2和
【设计实验】同学们设计了下图所示实验装置探究碱式碳酸铜的分解产物。(假设装置B、C、D中的药品足量,忽略反应后装置A中残留的气体)。

【实验过程】
(1)在装置D的导管a处连接一导管,并插入水中,微热试管,观察到导管口有气泡冒出,这一实验步骤的目的是
(2)向装置A的试管中加入碱式碳酸铜,用酒精灯加热至试管内固体质量不再改变。
【现象与结论】
装置A中绿色固体变黑,装置B中白色固体变蓝,并增重mg,装置C中增重ng,且m:n=
【实验反思】
如果上图装置中缺少装置D,则此时测定的m:n的值和“现象与结论”中你填写的值相比,会
Ⅱ.探究碱式碳酸铜中的碳酸根离子。
| 实验步骤 | 实验现象 | 实验结论 |
 | 左侧试管中产生大量气泡,且溶液变为蓝色;右侧试管中澄清石灰水变浑浊 | 碱式碳酸铜中含有碳酸根离子 |
上述实验步骤中X溶液为
【拓展提升】古代人们发现在孔雀石上燃烧炭火会有红色固体生成,该红色固体是
您最近一年使用:0次
四、实验题 添加题型下试题
实验题
|
适中(0.65)
解题方法
12. 根据下列实验装置图回答问题。

(1)写出标有字母a的仪器名称_________ 。
(2)实验室利用图A装置制取氧气的化学方程式为___________________ 。
(3)请写出用装置B制取二氧化碳的反应方程式________________________ 。
(4)若组装的装置既可以制备氧气又可以制备CO2,应选择的装置组合为_____ (填字母)。
(5)实验室制取气体时,不需要考虑的因素是 (填字母)。
(6)如图F装置所示,实验的现象为_________________________ 。

(1)写出标有字母a的仪器名称
(2)实验室利用图A装置制取氧气的化学方程式为
(3)请写出用装置B制取二氧化碳的反应方程式
(4)若组装的装置既可以制备氧气又可以制备CO2,应选择的装置组合为
(5)实验室制取气体时,不需要考虑的因素是 (填字母)。
| A.药品易获取 | B.反应条件易控制 | C.气体的颜色 |
您最近一年使用:0次
五、科学探究题 添加题型下试题
科学探究题
|
较难(0.4)
解题方法
13. 学习完盐的化学性质后,小黄对厨房中的碱面产生了兴趣,于是和兴趣小组的同学一起进行了如下探究。

【查阅资料】①碱面的主要成分是碳酸钠,其余成分均溶于水且不参与反应。②MgCO3微溶于水,不视为沉淀。③Ba2+是重金属离子,有毒。
【实验过程】取适量碱面于烧杯中,加足量水,充分溶解后,得到溶液A。利用溶液A分别进行如下实验:
【实验分析】(1)试管①中观察到的现象是________________________ 。
(2)写出实验中产生白色沉淀的反应的化学方程式______________________________ 。
实验结束后,同学们将两支试管中的混合物倒入烧杯中,充分反应后过滤,得到无色滤液和白色沉淀。为合理处理废液,同学们对反应后溶液中的溶质进行探究。
【讨论交流】反应后的溶液中一定存在Na+、Cl-,一定不存在_________ (填离子符号) ,可能存在 、Ba2+、OH-中一种或两种,请说出一定不存在这种离子的理由
、Ba2+、OH-中一种或两种,请说出一定不存在这种离子的理由________________ 。
【实验探究】为进一步确定溶液中离子的存在情况,小黄、小李、小罗三位同学分别取烧杯中无色滤液少许于试管中,设计并进行了如下实验:
①小黄:向无色滤液中加入少量氯化镁溶液,观察到有白色沉淀产生。
②小李:向无色滤液中先滴加几滴酚酞溶液,观察到溶液变红,再加入过量的试剂X,观察到有白色沉淀产生,溶液由红色变为无色。
③小罗:向无色滤液中先加入过量碳酸钠溶液,再滴加几滴酚酞溶液,观察到有白色沉淀产生,溶液呈红色。
【实验结论】综合以上实验分析,溶液中还存在Ba2+、OH-。
【方案评价】老师对三位同学的实验方案进行评价和改进意见:
①小黄的方案只能证明OH-的存在。
②小李的方案只需加入过量试剂X,即可证明实验结论,则试剂X为___________ 。
③小罗的方案无法证明OH-的存在,理由是_____________ 。为验证实验结论,该方案可改进为______________ 。
【拓展反思】从环保角度考虑,欲使无色滤液中只含有无毒的NaCl,可向无色滤液中加入过量碳酸钠溶液,过滤后向滤液中再加入适量_______________ ,充分反应后即可。

【查阅资料】①碱面的主要成分是碳酸钠,其余成分均溶于水且不参与反应。②MgCO3微溶于水,不视为沉淀。③Ba2+是重金属离子,有毒。
【实验过程】取适量碱面于烧杯中,加足量水,充分溶解后,得到溶液A。利用溶液A分别进行如下实验:
【实验分析】(1)试管①中观察到的现象是
(2)写出实验中产生白色沉淀的反应的化学方程式
实验结束后,同学们将两支试管中的混合物倒入烧杯中,充分反应后过滤,得到无色滤液和白色沉淀。为合理处理废液,同学们对反应后溶液中的溶质进行探究。
【讨论交流】反应后的溶液中一定存在Na+、Cl-,一定不存在
 、Ba2+、OH-中一种或两种,请说出一定不存在这种离子的理由
、Ba2+、OH-中一种或两种,请说出一定不存在这种离子的理由【实验探究】为进一步确定溶液中离子的存在情况,小黄、小李、小罗三位同学分别取烧杯中无色滤液少许于试管中,设计并进行了如下实验:
①小黄:向无色滤液中加入少量氯化镁溶液,观察到有白色沉淀产生。
②小李:向无色滤液中先滴加几滴酚酞溶液,观察到溶液变红,再加入过量的试剂X,观察到有白色沉淀产生,溶液由红色变为无色。
③小罗:向无色滤液中先加入过量碳酸钠溶液,再滴加几滴酚酞溶液,观察到有白色沉淀产生,溶液呈红色。
【实验结论】综合以上实验分析,溶液中还存在Ba2+、OH-。
【方案评价】老师对三位同学的实验方案进行评价和改进意见:
①小黄的方案只能证明OH-的存在。
②小李的方案只需加入过量试剂X,即可证明实验结论,则试剂X为
③小罗的方案无法证明OH-的存在,理由是
【拓展反思】从环保角度考虑,欲使无色滤液中只含有无毒的NaCl,可向无色滤液中加入过量碳酸钠溶液,过滤后向滤液中再加入适量
您最近一年使用:0次
六、计算题 添加题型下试题
计算题
|
适中(0.65)
解题方法
14. 为测定某氯化钠溶液的溶质质量分数,化学兴趣小组同学进行如下实验:取一定量的氯化钠溶液于烧杯中,加入足量硝酸银溶液,充分反应后,过滤。实验过程中,测得的数据如下表:
(1)生成沉淀的质量是_______ g。
(2)计算氯化钠溶液的溶质质量分数_______ 。
| 反应前 | 反应后 | ||
| 烧杯质量/g | 氯化钠溶液质量/g | 硝酸银溶液质量/g | 烧杯及烧杯内溶液质量/g |
| 145.0 | 50.0 | 70. 0 | 250. 65 |
(1)生成沉淀的质量是
(2)计算氯化钠溶液的溶质质量分数
您最近一年使用:0次
2022-06-19更新
|
49次组卷
|
2卷引用:2022年陕西省中考考前模拟冲刺化学试题
试卷分析
整体难度:适中
考查范围:物质的化学变化、身边的化学物质、化学实验、化学与社会发展、物质构成的奥秘
试卷题型(共 14题)
题型
数量
选择题
6
填空与简答
4
科学探究题
2
实验题
1
计算题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 化学变化与物理变化判断 | 单选题 |
| 2 | 0.85 | 制取二氧化碳的装置 酒精灯的正确使用方法和注意事项 物质的加热 液体药品的取用 | 单选题 |
| 3 | 0.94 | 空气的污染与防治 二氧化碳对生活环境的影响 常见几种燃料使用对环境的影响 空气污染及其保护 | 单选题 |
| 4 | 0.85 | 用质量守恒定律确定物质组成 根据化学方程式计算质量比 微粒图像的分析及应用 甲烷 | 单选题 |
| 5 | 0.85 | 测定空气中氧气的含量实验的过程 探究铁生锈的条件 盐类参与的反应 实验探究燃烧条件 | 单选题 |
| 6 | 0.65 | 复分解反应的实质与应用 制取二氧化碳的原理 碳及其化合物间相互转化 甲烷的燃烧 | 单选题 |
| 二、填空与简答 | |||
| 7 | 0.65 | 合金的认识 人体内的常量元素 合理饮食 常见物品质材的辨别 | 填空题 |
| 8 | 0.85 | 用质量守恒定律确定物质组成 碳单质的稳定性 羊毛、合成纤维、棉的鉴别 多种多样的物质及其组成 | 填空题 |
| 9 | 0.65 | 微粒的观点解释现象 元素周期表信息示意图 塑料、合成橡胶、合成纤维 过滤 | 填空题 |
| 10 | 0.4 | 溶解时能量的变化 饱和溶液和不饱和溶液判断 固体溶解度曲线的应用 溶解度的相关计算 | 简答题 |
| 三、科学探究题 | |||
| 11 | 0.65 | 用质量守恒定律确定物质组成 二氧化碳的检验、验满及净化 碳酸根离子的验证 设计实验探究物质的成分 | |
| 13 | 0.4 | 碳酸氢钠、碳酸钠、碳酸钙 盐类参与的反应 几种常见阴、阳离子的鉴别 设计实验探究物质的成分 | |
| 四、实验题 | |||
| 12 | 0.65 | 高锰酸钾制取氧气实验 氧气的制取中装置的选择 制取二氧化碳的原理 | |
| 五、计算题 | |||
| 14 | 0.65 | 有关质量守恒定律的计算 溶质质量分数结合化学方程式的计算 盐类参与的反应 | |



