2023年四川省攀枝花市西区中考二模化学试题
四川
九年级
二模
2023-05-09
119次
整体难度:
适中
考查范围:
物质的化学变化、化学实验、身边的化学物质、化学与社会发展、物质构成的奥秘
一、选择题 添加题型下试题
| A.研制治疗癌症的新药 | B.研究地壳板块结构及运动规律 |
| C.研制新型航空航天材料 | D.研究将废旧塑料变成汽车燃料 |
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
| A.NH4H2PO4 | B.CO(NH2)2 | C.NH4NO3 | D.KCl |
【知识点】 常见化肥的种类及性质解读
| A.霉变大米蒸煮后食用 | B.甲醛溶液浸泡虾仁防止腐烂 |
| C.按规定使用食品添加剂 | D.卤肉时可加入亚硝酸钠增加色泽 |
【知识点】 对人体健康危害的物质解读 合理饮食解读
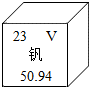
| A.钒为金属元素 | B.钒原子核外电子数为23 |
| C.钒的相对原子质量为50.94g | D.二氧化钒的化学式为VO2 |
【知识点】 元素周期表信息示意图解读 化学式书写及读法解读
| A.硫酸铁的化学式:FeSO4 |
| B.有4个磷原子构成的单质分子:P4 |
| C.3个铝离子:3Al3+ |
| D.2个二氧化硫分子:2SO2 |
溶液 | 白醋 | 盐酸 | 蔗糖水 | 草木灰水 | 石灰水 |
加入攀枝花汁后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
| A.白醋的水溶液呈酸性 | B.草木灰的水溶液呈碱性 |
| C.攀枝花汁可以用作酸碱指示剂 | D.攀枝花汁滴到氯化钠溶液中显绿色 |
| A.属于氧化物 | B.含有氮分子 |
| C.由四种元素组成 | D.氢元素的质量分数最小 |

下列说法不正确的是
| A.反应前后分子种类改变 |
| B.反应前后原子种类不变 |
| C.反应前后氧元素质量减小 |
| D.生成物丙和丁的分子个数比为3:4 |
| 选项 | 项目 | 化学知识 |
| A | 用燃气灶炒菜 | 燃气燃烧放热 |
| B | 用炉具清洁剂去除油污 | NaOH可与油脂反应 |
| C | 用厨余垃圾自制花肥 | 物质发生缓慢氧化 |
| D | 往自制净水器内放入活性炭 | 活性炭具有催化作用 |
| A.A | B.B | C.C | D.D |
选项 | 实验目的 | 实验方案 |
A | 稀释浓硫酸 | 将水倒入浓硫酸中并用玻璃棒不断搅拌 |
B | 鉴别NaOH 和NH4NO3固体 | 取样,分别溶于水中,测量溶液温度的变化 |
C | 除去NaCl固体中少量的NH4Cl | 加入Ca(OH)2固体,研磨 |
D | 验证Zn、Cu、Ag三种金属的活动性强弱 | 将Zn、Cu分别加入AgNO3溶液中,观察现象 |
| A.A | B.B | C.C | D.D |
实验一:取少量样品于试管中,滴加1~2滴酚酞溶液,溶液显红色。
实验二:取少量样品于试管中,加入适量稀硫酸,有气泡放出。
实验三:取少量样品于试管中,加入足量的BaCl2溶液,有白色沉淀生成。过滤,向滤液中滴加1~2滴酚酞溶液,溶液显红色。
下列结论正确的是
| A.实验一说明NaOH溶液没有变质 | B.实验二说明NaOH溶液全部变质 |
| C.实验三中生成的沉淀为Ba(OH)2 | D.实验三说明NaOH溶液部分变质 |
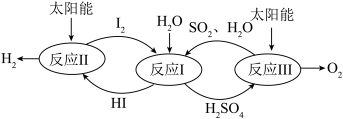
A.反应I的化学方程式: |
| B.理论上每生成2gH2,同时生成32gO2 |
| C.反应Ⅲ中生成SO2和O2的分子个数比为2:1 |
| D.反应I、Ⅱ和Ⅲ在反应前后均有元素化合价发生改变 |
| A.1.6g | B.2.56g | C.3.2g | D.4.8g |
二、填空与简答 添加题型下试题
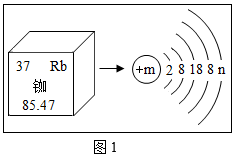
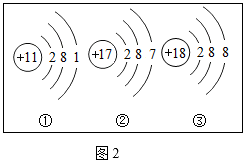
(1)如图1所示,m的数值为
(2)图2中与铷元素化学性质相似的是
(3)试写出氢氧化铷与稀盐酸反应的化学方程式
(1)冬奥会环保人员的服装面料是利用回收废弃的塑料瓶加工制成。塑料属于
a.金属材料 b.复合材料 c.合成材料
(2)冬奥会火炬"飞扬”首次采用液氢作燃料。关于氢气液化的过程说法正确的是
a.氢分子的体积变小 b.氢分子间的间隔变小 c.氢分子的数目变少
(3)冬奥会上提供经过二氧化氯消毒处理的直饮水。
①二氧化氯的化学式为
②证明该直饮水是软水应取样并向其中加入
(4)冬奥会为运动员提供的某运动饮料包装标签部分说明如图。

其中能预防骨质疏松、佝偻病的阳离子是


(1)A处对应的物质为CH4,其中数字“4”的含义为
(2)图中D处对应的物质的化学式为
(3)价类图中的物质在一定条件下可以相互转化。汽车的“催化转化器"可将尾气中的有毒气体CO转化为无毒的CO2,反应的微观示意图如图2所示,参加反应的X与Y的质量比为

(1)t1℃时,物质A的溶解度与物质
(2)当A中含有少量B时,可采用
(3)t1℃时,A、B、C三种物质的饱和溶液中溶质质量分数最大的是
(4)t2℃时,将30克A物质放入50克水中,充分溶解后所得溶液的质量是
(5)t1℃时,取等质量的A C饱和溶液分别置于如图2所示R甲、乙两支试管中,在大烧杯中加入一定质量的氢氧化钠固体溶解后,A、C溶液的溶质质量分数是否改变
a.A不变,C变小 b.A变大,C变小 c.A变小,C不变
食品标签上的背养素参考值是消费者选择食品的依据之一,它的计算公式为:营养素参考值%=
 ×100%,营养素的推荐日摄入量由中国营养学会制定。
×100%,营养素的推荐日摄入量由中国营养学会制定。饼干配料表 | 饼干营养成分表 | ||
小麦粉、植物油、白砂糖鸡蛋。 食品添加剂(磷酸氢钙、碳酸 氢钠、柠檬酸等)、食用盐 | 项目 | 每100g | 营养素参考值% |
蛋白质 | 6.8g | 11% | |
脂肪 | 33.0 | 55% | |
碳水化合物 | 12.0g | 14% | |
膳食纤维 | 6.2g | 25% | |
钠 | 240mg | 12% | |
a.厨余垃圾
 b.可回收垃圾
b.可回收垃圾
c.其他垃圾
 d.有害垃圾
d.有害垃圾
(2)饼干配料中富含糖类的是
(3)添加剂磷酸氢钙(CaHPO4)中磷元素的化合价为
(4)表中“营养素参考值%”最低的是
三、实验题 添加题型下试题
相关实验装置如图所示。

(1)仪器a的名称是
(2)小明想用同一套装置分别制取O2和CO2,应选用制取装置为
Ⅱ组:溶液酸碱性的检验和酸碱的化学性质
(3)为了鉴别稀盐酸和NaOH溶液,小英使用pH试纸测得pH=1的溶液是
(4)稀盐酸和NaOH溶液反应无明显现象。为使该反应“可视化”,小英向NaOH溶液中滴加
四、科学探究题 添加题型下试题
查阅资料:
①食用级碳酸氢铵比较纯净,可作膨松剂,一般用在油炸食品中,水蒸食品中不用;
②常温常压下,1体积水约能溶解600体积氨气,其水溶液呈弱碱性。
③碱石灰是氧化钙和氢氧化钠的混合物。
产生疑惑:臭粉为何可以作脚松剂?为何一般适用于油炸食品面不适用于水燕食品?
实验设计:实验装置如图。图一是检验装置,图二是收集装置,取适量碳酸氢铵分别置于两试管中,按如图进行实验。

①图一:B中现象是
②图二:装置E的作用是
(2)解释与结论:
①有臭味的碳酸氢按添加到食品中,如果油炸,则含有的少量碳酸氢铵受热时完全分解、产生的气体使食品膨胀。且生成物可以迅速挥发而离开食品,没有残留物,其臭味会消失,碳酸氢铵受热发生反应的化学方程式是
②添加碳酸氢铵的食品如果水蒸,则
通过上述探究该明白了:高纯度的碳酸铵传可以作为食品添加剂,但同一食品添加剂并不适合所有食品。使用食品添加剂需产格控制用量。
五、填空与简答 添加题型下试题

(1)类比CO2与NaOH的反应写出“碱浸”时发生反应的化学方程式:
(2)“沉碲”时,发生的反应有Na2TeO3+2H2SO4=Na2SO4+H2O+TeO3↓,生成TeO2沉淀时需控制溶液的pH在4.5 - 5.0之间,其原因是
(3)“酸溶”后,在TeCl4溶液中通入SO2,反应生成碲和初中化学中两种常见的酸,则该反应的化学方程式是
(1)实验室将金属钠保存在煤油中,可能的原因是
(2)初中常见的钠的化合物主要有NaCl、NaHCO3、Na2CO3,实验室有三瓶失去标签的白色粉末可能是NaCl、NaHCO3、Na2CO3,请你通过实验把它们鉴到出来(请写出实验步骤、实验现象和实验结论):
六、计算题 添加题型下试题
实验次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
加入稀硫酸的质量/g | 30 | 30 | 30 | 30 | 30 |
剩余固体的质量/g | 16 | a | 12 | 11 | 11 |
(1)表中a的值为
(2)所用稀硫酸的溶质质量分数为
(3)反应后所得溶液的溶质质量分数是多少?(写出计算过程,结果精确到0.1%)
(4)在坐标中画出加入稀硫酸的质量与剩余固体质量的相应曲线关系,标注必要的数据。

试卷分析
试卷题型(共 26题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 化学研究对象 | 单选题 |
| 2 | 0.94 | 常用危险化学品标志 | 单选题 |
| 3 | 0.85 | 化合反应 分解反应 置换反应 | 单选题 |
| 4 | 0.85 | 常见化肥的种类及性质 | 单选题 |
| 5 | 0.65 | 对人体健康危害的物质 合理饮食 | 单选题 |
| 6 | 0.85 | 元素周期表信息示意图 化学式书写及读法 | 单选题 |
| 7 | 0.85 | 离子符号的含义及书写 化学式书写及读法 化学符号周围数字的含义 | 单选题 |
| 8 | 0.65 | 酸的通性 酸碱指示剂的应用 常见的酸碱指示剂及其变色情况 碳酸氢钠、碳酸钠、碳酸钙 | 单选题 |
| 9 | 0.85 | 氧化物的定义 化学式、分子式及涵义 根据化学式计算元素质量分数 | 单选题 |
| 10 | 0.65 | 质量守恒定律分析 质量守恒定律的微观解释 根据化学方程式计算质量比 | 单选题 |
| 11 | 0.65 | 缓慢氧化 简易净水器的构造和各部分的作用 几种常见碱的物理性质及用途 化学反应中能量变化的实际应用 | 单选题 |
| 12 | 0.65 | 化合价代数和的计算与应用 金属之最和分类 常见合金 着火点 | 单选题 |
| 13 | 0.65 | 金属活动性强弱的探究 溶解时能量的变化 浓硫酸的稀释 盐类参与的反应 | 单选题 |
| 14 | 0.85 | 强碱露置在空气中的变质 碳酸根离子的验证 几种常见阴、阳离子的鉴别 设计实验探究物质的成分 | 单选题 |
| 15 | 0.65 | 有关质量守恒定律的计算 用质量守恒定律确定物质组成 化学方程式的书写 化合价代数和的计算与应用 | 单选题 |
| 16 | 0.65 | 根据化学方程式计算质量比 不含杂质的化学方程式计算 含杂质的化学方程式计算 化学方程式与实验的计算 | 单选题 |
| 二、填空与简答 | |||
| 17 | 0.65 | 最外层电子在化学变化中的作用 元素周期表信息示意图 原子结构示意图与元素在周期表中的位置相互推断 碱的通性 | 填空题 |
| 18 | 0.65 | 微粒的观点解释现象 化学式书写及读法 硬水和软水定义及鉴别 塑料、合成橡胶、合成纤维 | 填空题 |
| 19 | 0.65 | 化学方程式的书写 根据化学方程式计算质量比 化学符号周围数字的含义 甲烷的燃烧 | 填空题 |
| 20 | 0.65 | 溶解时能量的变化 结晶分离混合物 固体溶解度曲线的应用 图像分析溶质质量分数的变化 | 填空题 |
| 21 | 0.85 | 化合价代数和的计算与应用 糖类的来源 塑料、合成橡胶、合成纤维 计算混合物中物质或元素的质量分数 | 填空题 |
| 24 | 0.65 | 化学方程式的书写 二氧化碳与碱的反应及实验 酸的通性 | 流程题 |
| 25 | 0.65 | 质量守恒定律的微观解释 化学方程式的书写 盐类参与的反应 药品的保存 | 填空题 |
| 三、实验题 | |||
| 22 | 0.65 | 制取二氧化碳的原理 无明显现象的中和反应的判断 溶液酸碱性及pH相关关系 常见仪器及制材的辨认 | |
| 四、科学探究题 | |||
| 23 | 0.4 | 化学方程式的书写 碱的通性 常见的酸碱指示剂及其变色情况 装置的作用 | |
| 五、计算题 | |||
| 26 | 0.4 | 溶质质量分数结合化学方程式的计算 溶液和化学方程式的综合计算 酸的通性 | |





 着火点
着火点 硫的化合价
硫的化合价 年产量
年产量 含碳量(%)
含碳量(%)

