23. 某考古工作中发现一种生锈的铜铁合金,为了检验其组成,设计如下实验。
资料:1.铜在空气中生锈产物是Cu
2(OH)
2CO
3, Cu
2(OH)
2CO
3属于盐能与酸反应。
2. 2FeCl
3 + Fe =3FeCl
2, 2FeCl
3 + Cu = 2FeCl
2 + CuCl
2。
步骤Ⅰ:取一定量生锈的铜铁合金,加入足量盐酸,充分反应,将所得气体X通入澄清石灰水,澄清石灰水变浑浊;过滤,得到滤渣A和滤液B;
步骤Ⅱ:向滤渣A中加入足量稀盐酸,无现象;
步骤Ⅲ:向滤液B中逐滴加入一定质量分数的氢氧化钠溶液,直至过量。
某同学依据步骤Ⅲ实验事实绘制了如图所示的曲线。
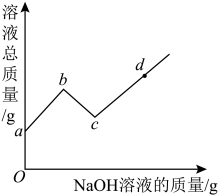
根据上述实验回答下列问题:
(1)气体X的组成可能是
___________,滤液B中一定有
___________。
(2)铜铁合金的组成有
___________种情况。
(3)下列说法正确的是_________
| A.a至b段对应溶液的pH逐渐减小 | B.b点对应溶液中的溶质为氯化钠 |
| C.c点对应溶液中的溶质种类最少 | D.a至c段氯化钠的质量逐渐增大 |
(4)在上述实验基础上设计实验回收铜。
________