21. 氯化钠是一种生活中常见的盐,在实验、生产、生活中有广泛的用途。
(一)配制50g质量分数为6%的氯化钠溶液
(1)计算。需要氯化钠
______g,蒸馏水
______mL。
(2)称量、量取。用量筒量取水的体积时,量筒必须放平,视线要与
______保持水平,再读出水的体积。
(3)溶解。用玻璃棒搅拌的目的是
______。
(4)装瓶、贴标签。
(二)探究氯化钠溶液的导电性
【查阅资料】
溶液的导电性可以用电导率传感器等测定出的电导率数值大小进行衡量。电导率数值越大,溶液的导电性越强。一定条件下,电导率的大小还能反映离子浓度大小。
【实验探究1】氯化钠溶液的导电性是否受溶液浓度和温度的影响?
【进行实验1】30℃时,测定不同浓度氯化钠溶液的电导率,将数据记录下表。
| 氯化钠溶液浓度(%) | 1.4 | 2.8 | 4.2 | 5.6 | 7.0 |
| 电导率值(S/m) | 2.000 | 3.219 | 4.533 | 5.800 | 7.133 |
【进行实验2】测定不同温度、不同浓度氯化钠溶液的电导率。
【实验结论】
(1)根据实验1,能够得出的结论是
______;
(2)根据实验2,能够得出的结论是
______。
【实验探究2】氯化钠溶于水形成溶液的过程中,导电性如何变化?
第一步:室温为26℃时,取100mL蒸馏水,加入烧杯中,放入磁力搅拌器磁珠;
第二步:校准传感器,组装仪器,设定搅拌档位;
第三步:用电导率传感器采集数据,迅速将一定质量的氯化钠加入烧杯中、实验数据如图所示。
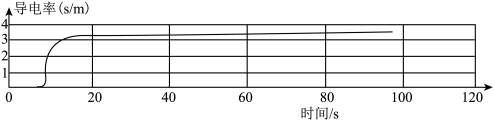
请说明实验过程中液体的电导率变化的原因
______。
(三)电解饱和氯化钠溶液
工业上用电解饱和食盐水的方法生产烧碱、氢气、氯气等化工产品。某学习小组在老师的指导下,用自制的实验装置(如图所示)进行电解饱和食盐水制取氢氧化钠的实验。
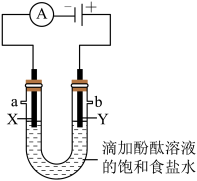
【查阅资料】:Ι、在氯化钠溶液中存在Na
+、Cl
-、H
+、OH
-四种离子。
Ⅱ、氯气能使湿润的淀粉碘化钾试纸变蓝。
【实验探究】
接通电源一段时间后,观察到X、Y电极周围均有气泡产生,溶液由无色变为红色。用小试管在a端收集气体,移近酒精灯火焰,松开拇指,发出轻微的爆鸣声,说明该气体为
______。将湿润的淀粉碘化钾试纸放在b端,试纸变蓝。电解饱和食盐水的化学方程式是
______。
【实验反思】电解水时,为增加导电性可向水中加入稀硫酸或氢氧化钠溶液,
______(填可以或不可以)加入氯化钠溶液进行水的电解。