2017届广东省广州市荔湾区八校九年级中考一模化学试卷
广东
九年级
一模
2017-05-13
475次
整体难度:
适中
考查范围:
身边的化学物质、化学与社会发展、物质的化学变化、物质构成的奥秘、化学实验
一、选择题 添加题型下试题
| A.油锅着火,立刻用锅盖熄灭或放入较多蔬菜 |
| B.生活中可以用过滤的方法降低水的硬度 |
| C.蚁虫叮咬后在人的皮肤内分泌蚁酸,涂含氨水的药水减轻痛痒 |
| D.广州目前推进生活垃圾分类,易拉罐、废纸是可回收物 |
| A.不锈钢和生理盐水属于纯净物 | B.液态氧属于氧化物 |
| C.乙醇属于有机物 | D.鸡蛋、水果属于蛋白质 |
【知识点】 单质和化合物的判断解读 有机物定义和常见的有机物解读
选项 | 共性 | 差异性 |
A | 均由分子构成 | 分子的结构不同 |
B | 均由碳元素和氧元素组成 | 元素的质量比不同 |
C | 常温下均是无色气体 | 相同条件下气体的密度不同 |
D | 均能与水化合 | 化合现象不同 |
| A.A | B.B | C.C | D.D |
【知识点】 碳的氧化物的全面比较解读
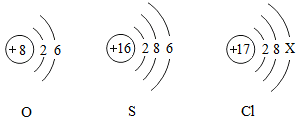
| A.硫原子在化学反应中失去电子 | B.氯原子的结构示意图中x的数值是7 |
| C.氧和氯两种元素最本质的区别是它们原子的中子数不同 | D.氧和硫两种元素的化学性质具有相似性是原子的电子数相同 |

| A.物质C一定是铜 | B.铁能从B中盐溶液中置换出B |
| C.金属A不能制氢气 | D.四种金属的活动顺序为A>B>Fe>C |
【知识点】 金属活动顺序表及应用 金属活动性强弱的探究解读
| A.HClO | B.H2 | C.HCl | D.NaCl |
【知识点】 根据方程式推测化学式解读
| A.水通电分解时产生的氢气和氧气质量比为2:1 | B.海水经过滤后可直接饮用 |
| C.用肥皂水区分硬水和软水 | D.活性炭吸附水中的色素和异味是化学变化 |
| A.桂花开放时满园飘香:说明分子在不断运动 |
| B.气体可压缩储于钢瓶中:说明分子之间有间隔 |
| C.品红在热水中扩散比冷水中要快:说明分子在受热的情况下运动加快 |
| D.分离液态空气制氧气:说明分子可以再分 |
| A.青蒿素比双氢青蒿素少两个氢原子 |
| B.青蒿素中C、H、O三种元素的质量比是90:11:40 |
| C.青蒿素和双氢青蒿索分子中碳、氧原子个数比都为3:1 |
| D.青蒿素中氧元素的质量分数比双氢青蒿素中氧元素的质量分数大 |
| A.铁制品锈蚀的过程实际上是铁与氧气发生的化学反应 |
| B.铝制品不易锈蚀的原因是铝与氧气作用在表面形成致密薄膜 |
| C.电池中含有铅、镍、镉、汞等金属,随意丢弃电池会造成污染 |
| D.合金的很多性能与组成它们的纯金属不同,合金具有更广泛的用途 |
| A.一氧化碳可作燃料,体现了一氧化碳的可燃性 |
| B.石墨可作电极,是利用了石墨的导电性 |
| C.氧化钙可做食品干燥剂,是利用氧化钙溶于水中放热 |
| D.氢氧化钙可用来改良酸性土壤,是因为氢氧化钙能中和酸性 |

| A.从肥效角度看,这种肥料共有两种营养元素 |
| B.化肥能提高粮食产量,施用越多越好 |
| C.从图示可知,这种复合肥料是可溶于水的 |
| D.从图示可知,这种复合肥料受热不易变质 |
【知识点】 常见化肥的种类及性质解读 合理使用化肥和农药解读
| A.配制15%的过氧乙酸溶液100克,需要过氧乙酸15克 |
| B.配制时把过氧乙酸倒入量筒中搅拌溶解 |
| C.量筒量取水时,如果视线俯视,则配制溶质的质量分数偏大 |
| D.配制好的溶液装入试剂瓶中,盖好瓶塞并贴上标签 |
【知识点】 配制一定溶质质量分数的计算解读
| 选项 | 实验目的 | 实验方案 |
| A | 鉴别NaOH、Ca(OH)2两种无色溶液 | 溶液中通入CO2 |
| B | 鉴别NaCl、CuSO4、KCl 三种白色物质 | 加水溶解 |
| C | 除去CO2中的CO | 将混合气体通过NaOH固体 |
| D | 除去生石灰中CaCO3 | 向固体中加稀盐酸 |
| A.A | B.B | C.C | D.D |
【知识点】 除杂解读 物质鉴别——选用试剂鉴别解读
| A.从环境保护的角度考虑,理想的燃料是煤 |
| B.为了预防贫血,多吃鱼、蛋等食物补充人体需要的钙元素 |
| C.蔬菜、水果等食物是人体获取维生素的主要食物 |
| D.用甲醛溶液处理海鲜,延长食物保质期 |
 |  |  |
| A.实验①中的固体溶解,形成紫红色溶液;实验②中的固体几乎不溶解 |
| B.设计实验②、③的目的是比较高锰酸钾和碘在汽油中溶解情况 |
| C.对比实验①、②可得出的结论是高锰酸钾在水中的溶解性比汽油中的好 |
| D.实验说明不同物质在同一溶剂中溶解性是相同的,同一种物质在不同溶剂中溶解性也是相同的 |
【知识点】 溶解性相关的实验探究解读
二、填空与简答 添加题型下试题
(1)不锈钢主要成分是铁、铬(Cr)、镍(Ni)。其中,铬常见化合价是+2、+3和+6,铬的+3价的氧化物的化学式是
(2)目前广州使用主要燃气是天然气,燃烧时热量高且产物都是无毒气体。它燃烧的化学方程式是
(3)早期的加碘盐中的KI,在食盐保存过程,由于受到空气中氧气和水蒸气的作用,生成单质碘(I2)和氢氧化钾,容易使碘损失。该反应的化学方程式是
(1)下图是某反应的微观示意图:

B框中的物质属于
(2)写出下图A所示的反应化学方程式

(1)氢氧化钠溶液和碳酸钠溶液都能使酚酞变红色,它们的溶液pH
(2)试管中内壁残留下列物质,用盐酸浸泡能除去的是
A.铁锈锈渍 B.用碳粉还原氧化铜附着的红色固体
C.长时间盛放石灰水留下的白色固体 D.氢氧化钠和硫酸铜反应后的留下的蓝色固体
(3)工业上把浓海水除钙后,再加入碱性沉淀剂可以制备氢氧化镁。若海水中钙离子含量太高,氢氧化钙会存在于氢氧化镁颗粒中,从而影响氢氧化镁的纯净度。
某研究小组在控制反应温度是20~25℃和浓海水质量为1109g不变的条件下,进行下述对比实验,数据如下:
| 实验 | 碳酸钠加入量/g | 搅拌速度r/min | 反应时间/h | 钙除去率/% |
a | 1.78 | 200 | 3 | 44.8 |
b | 2.32 | 200 | 3 | 60.2 |
c | 2.32 | 125 | 4 | 55.1 |
d | 2.32 | 200 | 4 | 64.6 |
②搅拌速率越快,反应时间越长则消耗能源越多。为了节约能源,获得较高的钙除去率,进一步优化“搅拌速率”和“反应时间”的反应条件。在其他实验条件不变情况下,设计对比实验,你应选择的反应条件是
A.200r/min,3.5h B. 200r/min,4.5h C.175 r/min,4h D. 225 r/min,4h
三、综合应用题 添加题型下试题
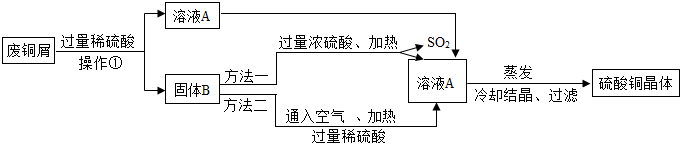
(1)铜屑表面呈绿色的物质化学式是Cu2(OH)2CO3,从组成分析,预测它除了能与稀硫酸反应后,还能与
(2)方法二的化学反应的化学方程式为2Cu+2H2SO4+
(3)硫酸铜晶体广泛应用在电镀、印染、农药等方面,波尔多液是一种农业常用杀菌剂,它由硫酸铜、生石灰加水配制而成,不能用铁制容器来配制波尔多液的原因是(用化学方程式表示)
(4)理论上废铜屑中的铜完全可以转化为硫酸铜。已知废铜屑的质量为100kg,若最后所得的硫酸铜质量为80kg,则废铜屑中铜的质量分数为
四、填空与简答 添加题型下试题
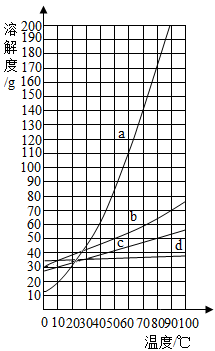
右图是a、b、c、d四种固体物质的溶解度曲线;下表是这些固体物质在部分温度时的溶解度。
| NaCl | KCl | NH4Cl | KNO3 | |
| 10℃ | 35.8g | 31.0g | 33.3g | 20.9g |
| 60℃ | 37.3g | 45.5g | 55.2g | 110.0g |

(1)图中a曲线表示
(2)40℃时,比较a、c溶解度的大小:a
(3)60℃时硝酸钾饱和溶液中溶质的质量分数约为
(4)60℃时配制100g硝酸钾饱和溶液,下图是配制过程的一些操作:

用序号A、B、C、D、E表示正确的实验操作顺序:
A.先移动游码到所需要位置,再左盘添加硝酸钾直到天平平衡
B.先左盘添加所需要的硝酸钾,再右盘加砝码,移动游码直到天平平衡
C.先右盘加砝码,再移动游码,最后左盘加硝酸钾直到天平平衡
五、实验题 添加题型下试题

(1)A实验中a仪器的名称是
(2)B实验中导致实验结果偏小的原因是
(3)C实验中当蒸发皿中
六、填空与简答 添加题型下试题
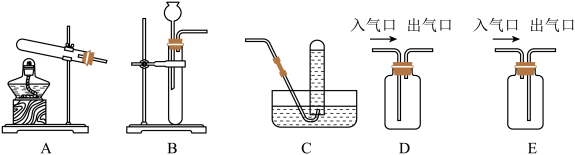
(1)实验室用碳酸钙制取二氧化碳气体时,应选用气体发生装置
(2)实验室用氯酸钾和二氧化锰制取氧气,其反应的化学方程式为
(3)实验室常用氯化铵和氢氧化钙固体加热反应来制取NH3。NH3是一种没有颜色而有刺激性气味的气体,极易溶于水,密度比空气小。那么,
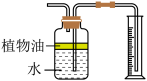
(4)将E装置改为下图,可用来测量生成的CO2气体的体积,在水面上放一层植物油的目的是
(1)20℃时,在实验室用98 %的浓硫酸配制20%的硫酸溶液:
①若要配制49g质量分数为20%硫酸,所需要水的质量为
②用到的仪器有:烧杯、玻璃棒和
A.托盘天平(带砝码盒) B.药匙 C. 胶头滴管
D. 200mL量筒 E.50mL量筒 F. 10mL量筒
③从下表中找出稀释过程需要用到的数据:
硫酸溶液的密度(单位:g/cm3)
| 质量分数/ % | 10℃ | 20℃ | 30℃ |
| 20 % | 1.145 | 1.139 | 1.133 |
| 98 % | 1.846 | 1.836 | 1.826 |

该同学观察实验现象是
(3)某化学学习小组研究硫酸的性质,将20%硫酸溶液放入试管中,如图所示(装置气密性良好),再向试管中加入某物质后,温度计温度升高,该物质是
A. 锌粒 B. 冰块 C. 铜块
D. 氯化钠 E.氢氧化钠

七、科学探究题 添加题型下试题
(1)小红在少量配方溶液中滴入稀HCl溶液,观察有气泡产生,证明配方溶液中含有的离子是
(2)小明查阅资料可知,用上述配方溶液浸泡制作皮蛋,不同量的生石灰、纯碱会配制出不同浓度的氢氧化钠溶液,影响皮蛋的质量。请你设计实验,验证配方溶液中含有氢氧化钠。
限选试剂:BaCl2溶液、Ca(OH)2溶液、盐酸溶液、酚酞试液。
实验操作 | 预期现象 | 结论 |
配方溶液中含有氢氧化钠 |
试卷分析
试卷题型(共 29题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 废弃金属对环境的影响及回收 硬水的危害及软化方法 中和反应的实际应用 灭火原理与方法 | 单选题 |
| 2 | 0.94 | 化学性质和物理性质 | 单选题 |
| 3 | 0.85 | 单质和化合物的判断 有机物定义和常见的有机物 | 单选题 |
| 4 | 0.94 | 空气中各成分的用途 | 单选题 |
| 5 | 0.65 | 碳的氧化物的全面比较 | 单选题 |
| 6 | 0.4 | 原子中各类微粒的数值关系 原子结构示意图含义及应用 最外层电子在化学变化中的作用 元素的概念 | 单选题 |
| 7 | 0.65 | 金属活动顺序表及应用 金属活动性强弱的探究 | 单选题 |
| 8 | 0.85 | 根据方程式推测化学式 | 单选题 |
| 9 | 0.85 | 化学变化与物理变化判断 常见几种净化水操作的比较 硬水和软水定义及鉴别 电解水实验的现象和结论 | 单选题 |
| 10 | 0.65 | 微粒的观点解释现象 | 单选题 |
| 11 | 0.4 | 分子、原子的区别与联系 根据化学式计算元素质量比 根据化学式计算元素质量分数 | 单选题 |
| 12 | 0.85 | 浓硫酸的稀释 酒精灯的正确使用方法和注意事项 固体药品的取用 | 单选题 |
| 13 | 0.85 | 合金的认识 金属与氧气反应 废弃金属对环境的影响及回收 钢铁的锈蚀 | 单选题 |
| 14 | 0.85 | 石墨的相关知识 一氧化碳的可燃性 生石灰的性质及用途 中和反应的实际应用 | 单选题 |
| 15 | 0.94 | 合成材料 | 单选题 |
| 16 | 0.85 | 常见化肥的种类及性质 合理使用化肥和农药 | 单选题 |
| 17 | 0.85 | 配制一定溶质质量分数的计算 | 单选题 |
| 18 | 0.4 | 除杂 物质鉴别——选用试剂鉴别 | 单选题 |
| 19 | 0.94 | 对人体健康危害的物质 维生素的来源 某些元素的食物来源 氢能源的优点 | 单选题 |
| 20 | 0.4 | 溶解性相关的实验探究 | 单选题 |
| 二、填空与简答 | |||
| 21 | 0.15 | 化学方程式的书写 化学式书写及读法 化合价代数和的计算与应用 | 填空题 |
| 22 | 0.4 | 质量守恒定律的微观解释 纯净物和混合物的判断 单质和化合物的判断 分子、原子的区别与联系 微粒图像的分析及应用 | 填空题 |
| 23 | 0.15 | 化学方程式的书写 酸的通性 溶液酸碱性及pH相关关系 | 填空题 |
| 25 | 0.15 | 饱和溶液和不饱和溶液的转换 固体溶解度曲线的应用 溶质质量分数概念 固体配制一定质量分数溶液 | 填空题 |
| 27 | 0.4 | 化学方程式的书写 浓硫酸做干燥剂 气体制备综合考查 气体净化、干燥 | 填空题 |
| 28 | 0.65 | 配制一定质量分数溶液的仪器 配制一定溶质质量分数的计算 浓硫酸的物理、化学性质 常见吸热反应及放热反应 | 填空题 |
| 三、综合应用题 | |||
| 24 | 0.4 | 置换反应 含杂质的化学方程式计算 金属与盐溶液反应 酸的通性 | |
| 四、实验题 | |||
| 26 | 0.85 | 测定空气中氧气含量的实验误差分析 铁在氧气中燃烧及其实验 蒸发 | |
| 五、科学探究题 | |||
| 29 | 0.65 | 盐类参与的反应 碳酸根离子的验证 设计实验探究物质的成分 | |

 点燃酒精灯
点燃酒精灯 取用碳酸钠
取用碳酸钠 稀释浓硫酸
稀释浓硫酸 加入大理石
加入大理石

