21. 工业废料石膏(CaSO
4·2H
2O)可以“变废为宝”,用于生产氧化钙、硫酸钾、 电石(化学名称为碳化钙)等,某化学兴趣小组展开了如下系列研究。
一、高纯 CaO 的制备
【资料一】 I.石膏(CaSO
4·2H
2O)与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。 II.SO
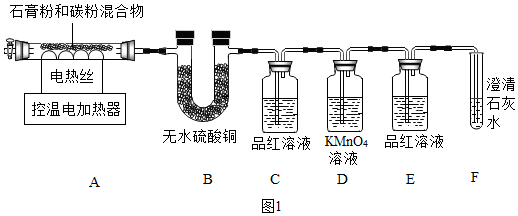
2 能使品红溶液褪色,也能使澄清石灰水变浑浊。甲同学用如图1 装置制备 CaO,并验证石膏与焦炭高温反应的其他产物。实验过程中发现:B 中无水硫酸铜变蓝,证明有 H
2O 生成;C 中产生品红溶液褪色现象证 明有 SO
2 生成;装置
_________中无明显变化和装置 F 中
______现象证明有 CO
2 生成。
二、硫酸钾和电石的制备
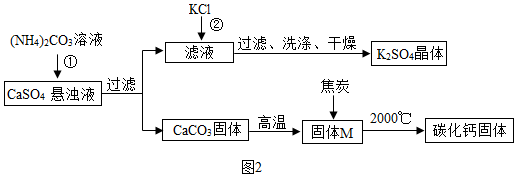
(1)证明固体 M 中不含 CaCO
3 的方法是
_____________(写出实验的方法、现象)
(2)反应②的化学方程式为(NH
4)
2SO
4+2KCl=K
2SO
4↓+2NH
4Cl。
三、假设上述流程中制得的碳化钙(化学式为 CaCx)固体中只含杂质 CaO。乙小组同学为 测定 CaCx 中 x 的值进行如下实验。
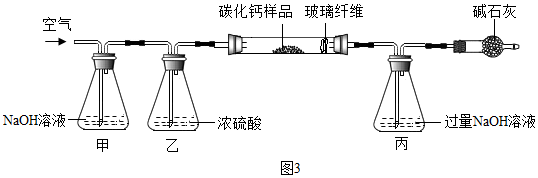
【资料三】CaCx 在空气中灼烧生成 CaO 和 CO
2。Ca(OH)
2+Na
2CO
3=CaCO
3↓+2NaOH 步骤一:称取 3.76g 样品于图 3 所示石英管中(测定装置图如图 3,夹持及加热装置省略), 反应前缓缓通入空气,高温灼烧石英管中的样品至反应完全后继续缓缓通入空气。测得丙溶 液的质量比反应前增重了 4.4g。(玻璃纤维可防止固体粉末进入导管) 步骤二:将石英管内剩余固体全部转移到水中,加入足量碳酸钠溶液,经搅拌、过滤、洗涤、 干燥等操作得到碳酸钙固体 6 克。试回答下列问题:
(1)装置甲的作用是
_______。反应完全后继续缓缓通入空气的目的是
_____________。
(2)根据步骤一、二计算该样品中钙、碳、氧的质量比为
_____。计算确定 CaCx的化学式
_____。
(3)若碳酸钙未能完全干燥,则会导致 CaCx中的x的值
______________(填“偏大”、“偏小”、 “无影响”)。