【区级联考】四川省成都市金牛区2019届九年级上学期期末考试化学试题
四川
九年级
期末
2019-02-19
429次
整体难度:
适中
考查范围:
物质的化学变化、身边的化学物质、化学与社会发展、物质构成的奥秘、化学实验
一、选择题 添加题型下试题
| A.草船借箭 | B.火烧新野 | C.水淹七军 | D.挂印封金 |
【知识点】 化学变化与物理变化判断解读
| A.过滤中玻璃棒的主要作用是搅拌 |
| B.水的净化过程中,活性炭可以降低水的硬度 |
| C.量取一定量液体时,读数时应将量筒平放,视线应与凹液面最低处保持水平 |
| D.电解水实验中,与电源负极相连的一端产生的气体可以用带火星的木条检验 |
【知识点】 简易净水器的构造和各部分的作用解读 电解水生成物的验证解读
| A.二氧化碳可以灭火 | B.二氧化碳能作化工原料和气体肥料 |
| C.含碳物质在氧气中燃烧均可能产生二氧化碳 | D.干冰是二氧化碳的固体,所以二氧化碳也俗称“干冰” |
| A.物质是由分子、原子或离子构成的 | B.分子、原子和离子都在不停运动 |
| C.分子与原子的区别是分子可分,而原子不可再分 | D.篮球中能充入较多气体是因为气体分子间间隙较大,易于压缩 |

| A.铝原子核内中子数为13 |
| B.铝的相对原子质量为26.98g |
| C.铝离子的原子核外有三个电子层 |
| D.铝元素在化合物中呈+3价 |
【知识点】 周期表信息示意图及结构示意图的综合考查解读
| A.金属材料在常温下都是固体 | B.人类最早大量使用的金属是铁 |
| C.金属的性质是决定用途的唯一因素 | D.生铁和钢都属于铁的合金 |
| A.CaO + H2O=Ca(OH)2 | B.Fe+CuSO4=FeSO4+Cu↓ |
| C.Zn+H2SO4=ZnSO4+H2 | D.CH4 + 2O2=CO2+2H2 O |
| A.该物质有氢原子、碳原子、氧原子构成 |
| B.该物质中碳元素与氢元素的质量比为9:13 |
| C.该分子由C、H、N三种元素组成 |
| D.该分子中C、H、N三种原子个数比为9:13:1 |
【知识点】 化学式的简单计算 化学式、分子式及涵义解读

| A.反应中涉及三种氧化物 |
| B.反应前后分子、原子数目不变 |
C.该反应的化学方程式是 4NH3+6NO 5N2+6H2O 5N2+6H2O |
| D.该反应前后,催化剂的质量和性质不变 |
【知识点】 质量守恒定律分析 微粒图像的分析及应用解读
| A.乙醇汽油的使用可以适当节省石油资源 | B.汽油着火时,用水浇灭 |
| C.煤、石油、天然气三种化石燃烧的使用中,煤的污染最小 | D.氢气与空气混合点燃容易发生爆炸,所以氢气不能作为燃料 |
【知识点】 灭火原理与方法解读 常见几种燃料使用对环境的影响解读
A.盐酸与碳酸钠反应前后质量守恒 |
B.除去水中杂质,得到蒸馏水 |
C.品红在水中扩散证明分子的运动 |
D.纯金属与合金的硬度比较 |
 2X+2TiCl4+6CO的说法正确的是
2X+2TiCl4+6CO的说法正确的是| A.该反应体现了碳的可燃性 | B.该反应必须进行尾气处理 |
| C.该反应中X 为 FeCl2 | D.FeTiO3中Ti的化合价可能是负价 |
【知识点】 用质量守恒定律确定物质组成解读
| 物 质 | X | O2 | CO2 | H2O |
| 反应前的质量/g | 1.6 | 8 | 2.2 | 1.8 |
| 反应后的质量/g | 0 | 1.6 | 待测 | 5.4 |
| A.该反应可能是化合反应 | B.表中“待测”数据为 4.4 |
| C.反应中的X 与 O2 变化的质量比是 1:4 | D.X可能是乙醇 |
【知识点】 质量守恒定律的应用
二、填空与简答 添加题型下试题
(1)石墨烯是从石墨中分离出来的单层石墨片,它是目前人工制得的最薄的材料,理论上可以用于在地球与月球之间架设电梯,它的一些用途如图:

①石墨烯、金刚石的物理性质
②石墨烯的导电性
③石墨烯还具有密度
(2)以空气为主要成分的一种气凝胶,是目前人工制得的最轻的固体,具有疏松多孔的结构,高温灼烧时几乎无变化。
①该气凝胶属于
②该气凝胶化学性质
③该气凝胶像活性炭一样具有
(1)上述物质中,属于氧化物的有
(2)空气中二氧化碳含量的不断上升,会导致
(3)如果要将110g CO2完全吸收,理论上会消耗多少克氢氧化钙
【知识点】 二氧化碳对生活环境的影响解读
三、实验题 添加题型下试题

(1)图A 是燃烧条件的探究实验。将大小相同的滤纸片和乒乓球碎片放在薄铜片的两侧,加热铜片的中部,观察到
(2)图 B 是木炭在氧气中燃烧的实验示意图。操作方法是:把加热到红热的木炭
(3)在图 C集气瓶中,放入用石蕊溶液染成紫色的小花,小花一半干燥一半润湿。可观察的实验现象是
(4)用图 D 装置在实验室中制取二氧化碳,化学方程式为
(5)用图 E 装置收集一瓶二氧化碳气体,请在图中将导管补画完整。证明该装置中二氧化碳收集满的方法是
四、填空与简答 添加题型下试题

【查阅资料】常压下,氧气的沸点是-183℃,氮气的沸点是-196℃。
(1)操作1的名称是
(2)如果将燃着的木条置于盛满液态空气的容器口,观察到的现象是木条
(3)除分离液态空气外,现在还有一种膜分离技术制氧法,原理是在一定压力下,让空气通过薄膜,氧气能透过薄膜,从而达到分离空气的目的。据此推测氮分子比氧分子体积
(4)下列属于氧气用途的是
A.气体肥料 B.工厂炼钢 C.充气包装 D.霓虹彩灯
Ⅱ.甲、乙、丙为初中化学上册中常见物质,它们之间均能一步实现如图所示的转化关系。

(1)如果丙能使带火星的木条复燃,则甲的名称是
(2)如果乙是一种易与血液中的血红蛋白结合的有毒气体,则甲
五、科学探究题 添加题型下试题
【探究目的】探究黑色固体时镁与空气中什么物质反应产生的?
【查阅资料】
(1)稀有气体一般不与其它物质反应;
(2)光亮的镁条与水反应,表面会生成白色固体。
【分析猜想】分析空气中各成分,进行猜想:
(1)猜想①是氧气 猜想②是氮气 猜想③是
【实验一】镁带与氧气的反应
(一)甲同学探究了影响过氧化氢制取氧气速度的某种因素,进行了三次实验并记录了各种收集相同体积氧气所需要的实验如下表:
| 实验 | 过氧化氢的浓度 | 过氧化氢溶液的质量(g) | 二氧化锰的质量(g) | 收集时间(s) |
| 1 | 10% | 20 | 1 | 40 |
| 2 | 15% | 20 | 1 | 20 |
| 3 | 20% | X | 1 | 12 |
(2)第3次实验中,X的值应为
(3)实验结论:在相同条件下,
(二)乙同学在量筒中盛满水,倒置与水槽中,通过分液漏斗把20 mL某浓度得过氧化氢溶液加入锥形瓶中,记录量筒中气体得体积(图1)。数据如下表:
| 时间/min | 1 | 3 | 5 | 7 | 9 | 10 |
| 量筒读数/mL | 60.0 | 82.0 | 88 | 89.5 | 90 | 90 |
(4)请根据以上过程和实验数据综合分析,最终生成氧气得体积是
(5)请在下面坐标中绘制出0~10min生成氧气体积随时间变化得曲线

(三)燃烧镁带,观察现象
将镁带打磨光亮,点燃,伸入盛满氧气的集气瓶中,产生大量白烟,生成白色固体。
实验结论:镁与氧气反应生成白色的氧化镁。
【实验二】镁带与氮气的反应
(一)收集纯净的氮气
(二)燃烧镁带,观察现象
将镁带打磨光亮,点燃,伸入盛有氮气的集气瓶中,瓶内壁附着一层淡黄色的固体。
(6)实验结论:镁与氮气在点燃得的条件下发生化合反应生成淡黄色的氮化镁(Mg3N2),该反应的化学方程式是
【探究结论1】
(7)综上所述,关于镁在空气中燃烧产生黑色固体的猜想是猜想
【探究结论2】
(8)如果用足量的镁替代红磷进行空气组成实验,实验测得氧气的体积分数比实际值
【实验回顾】实验室常用红磷燃烧的方法测定空气中氧气含量(图2),由于红磷需要在瓶外点燃再伸入瓶内,常常带来污染以及误差。
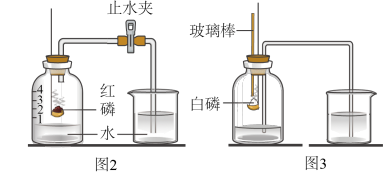
【实验改进】同学们选择了着火点更低的白磷,并对装置图做了改进(图3).主要操作是:再实际容积为180mL的集气瓶里,先装进50 mL的水,再按图连接好仪器,按下热的玻璃棒,白磷立即被点燃。
(9)白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是
(10)若实验中无误差,最终集气瓶中水的体积约为
(11)集气瓶里预先装进50 mL水的作用,其一是为了加快集气瓶的冷却速度;其二则主要是
【实验与交流】
(12)为了帮助同学们更好地理解空气中氧气含量测定的实验原理,老师利用传感器技术定时测量了实验装置(图4)内的压强、温度和氧气浓度,三条曲线变化趋势如图5所示。Y曲线表示的是

【知识点】 测定空气中氧气含量实验的改进解读
试卷分析
试卷题型(共 20题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 化学变化与物理变化判断 | 单选题 |
| 2 | 0.65 | 空气的污染与防治 | 单选题 |
| 3 | 0.65 | 水体的污染及保护 | 单选题 |
| 4 | 0.65 | 简易净水器的构造和各部分的作用 电解水生成物的验证 | 单选题 |
| 5 | 0.65 | 碳单质的可燃性 二氧化碳不可燃、不支持燃烧性质 二氧化碳的用途 | 单选题 |
| 6 | 0.65 | 物质的微粒性 分子、原子的关系 | 单选题 |
| 7 | 0.65 | 周期表信息示意图及结构示意图的综合考查 | 单选题 |
| 8 | 0.85 | 金属的物理通性与用途 合金的认识 常见合金 | 单选题 |
| 9 | 0.65 | 化学方程式的书写 | 单选题 |
| 10 | 0.85 | 化学式的简单计算 化学式、分子式及涵义 | 单选题 |
| 11 | 0.65 | 质量守恒定律分析 微粒图像的分析及应用 | 单选题 |
| 12 | 0.65 | 灭火原理与方法 常见几种燃料使用对环境的影响 | 单选题 |
| 13 | 0.65 | 实验探究质量守恒定律 微粒的观点解释现象 合金的认识 蒸馏 | 单选题 |
| 14 | 0.4 | 用质量守恒定律确定物质组成 | 单选题 |
| 15 | 0.4 | 质量守恒定律的应用 | 单选题 |
| 二、填空与简答 | |||
| 16 | 0.65 | 纯净物和混合物的判断 同种元素组成的物质 石墨的相关知识 活性炭的吸附性 | 填空题 |
| 17 | 0.65 | 二氧化碳对生活环境的影响 | 简答题 |
| 19 | 0.4 | 工业制取氧气 | 流程题 |
| 三、实验题 | |||
| 18 | 0.4 | 木炭在氧气中燃烧及其实验 制取二氧化碳的原理 二氧化碳与水的反应及实验 实验探究燃烧条件 | |
| 四、科学探究题 | |||
| 20 | 0.4 | 测定空气中氧气含量实验的改进 | |



