18. 氨用于制造氮肥(尿素、碳铵等)、复合肥料、硝酸、纯碱等,广泛应用于化工、轻工、化肥制药、合成纤维等领域。
Ⅰ.工业制氨是以哈伯法通过氮气和氢气在高温高压和催化剂的作用下化合生成的,请算出氮气与氢气恰好完全反应时的质量比
________ ;
Ⅱ.目前有一种“人工固氮”的新方法反应过程示意图如下:

(1)根据反应的微观示意图写出化学方程式:
_____________ ;
(2)氨气进入大气后与雨水作用,可能形成“碱雨”。写出碱雨中碱的化学式,并标出其中氮元素的化合价:
_________ ;
Ⅲ.氨是氮肥的重要原料。某化肥厂生产铵态氮肥(NH
4)
2SO
4的工艺流程如下:

(1)操作Ⅰ中的玻璃棒作用是
_________ ;
(2)加入的X应为
_____ (填字母)
A H
2SO
4 B CaSO
4 C SO
2Ⅳ.氨也是工业索维尔法制纯碱的重要原料。
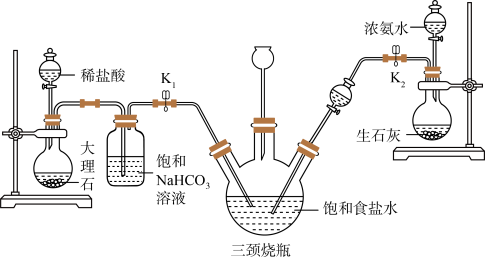
某兴趣小组采用下列装置模拟索维尔法制备碳酸氢钠,实验操作如下:
a.关闭K
1,打开K
2通入NH
3,调节气流速率,待其稳定后,打开K
1通入CO
2;
b.待三颈烧瓶内出现较多NaHCO
3固体时,关闭K
2停止通NH
3,一段时间后,关闭K
1停止通CO
2;
c.将三颈烧瓶内的反应混合物过滤、洗涤、低温干燥,并将所得固体置于敞口容器中加热,记录剩余固体质量。
| 加热时间/min | t0 | t1 | t2 | t3 | t4 | t5 |
| 剩余固体质量/g | 未记录 | 30.6 | 27.4 | 23.8 | 21.2 | 21.2 |
【资料】常温常压下,1体积水约能溶解700体积氨气,1体积水约能溶解1体积二氧化碳。请回答下列问题:
(1)三颈烧瓶内生成的另一产物是一种铵态氮肥,写出其中发生的化学反应方程式:
__________ ;加热过滤得到的NaHCO
3,发生反应:2NaHCO
3
Na
2CO
3 + CO
2↑+ H
2O。
(2)三颈烧瓶上连接的长颈漏斗的主要作用是
__________ ;
(3)打开K
2通入NH
3一段时间后,才打开K
1通入CO
2,原因是
__________ ;
(4)饱和碳酸氢钠溶液的作用是
______________ ;
(5)根据实验记录,计算t
2 min时NaHCO
3固体的分解率(已分解的NaHCO
3质量与加热前原NaHCO
3质量的比值),请写出计算过程
__________ 。