山东省潍坊市山东寿光实验中学2020-2021学年九年级上学期12月月考化学试题
山东
九年级
阶段练习
2021-01-18
226次
整体难度:
适中
考查范围:
身边的化学物质、化学与社会发展、物质构成的奥秘、化学实验、物质的化学变化
一、选择题 添加题型下试题
| A.面粉 | B.汽油 | C.碳酸钙 | D.硫酸铜 |
【知识点】 判断物质是否能形成溶液解读 悬浊液、乳浊液解读
| A.禁放烟花爆竹 | B.废气达标排放 | C.工地洒水除尘 | D.秸秆露天焚烧 |
| A.降低氧气浓度使煤燃烧的更充分 |
| B.使温度降到着火点以下可以灭火 |
| C.物质与氧气发生的反应都是燃烧 |
| D.人类利用的能量都是通过燃烧获得的 |
| A.浓硫酸可用于干燥O2 |
| B.浓硫酸可使纸张炭化 |
| C.实验室可用块状石灰石与稀硫酸制备CO2 |
| D.稀硫酸可用于金属表面除锈 |
| A.实验步骤:计算、量取、混匀、装瓶贴标签 |
| B.实验仪器:量筒、胶头滴管、烧杯、玻璃棒、细口瓶 |
| C.稀释浓硫酸时将水沿烧杯内壁慢慢注入浓硫酸中,并不断搅拌 |
| D.浓硫酸不慎沾到皮肤上,应立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液 |
| A.金刚石是天然存在的最硬的物质,可用来裁玻璃 |
| B.石墨有金属光泽,有导电性,所以是一种金属 |
| C.活性炭具有吸附性,可以吸附所有物质 |
| D.金刚石、石墨和足球烯(C60)都是由碳原子直接构成的 |
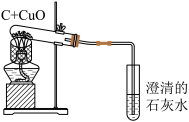
| A.导管口刚有气泡冒出说明反应开始 |
| B.实验结束应立即倒出粉末 |
| C.木炭能使氧化铜还原为铜 |
| D.固体减少的质量一定等于生成二氧化碳质量 |
【知识点】 木炭还原氧化铜的实验解读
| A.白醋、酒精、汽油易挥发,是由于分子在不停运动,其挥发过程是化学变化 |
| B.井水含有较多钙、镁离子,是硬水,危害人体健康,生活中常采用煮沸的方法将其软化 |
| C.通常的燃烧需要同时具备三个条件:可燃物、氧气(空气)、温度达到着火点。灭火就是破坏燃烧的条件,如:吹灭蜡烛就是降低蜡烛的着火点 |
| D.餐厅洗碗工用洗洁精清洗餐具上的油污,汽车修理工用汽油清洗手上的油污,二者的原理都是溶解 |

| A.物质①中碳元素的化合价为+4价 |
| B.物质②中阳离子符号为Ca+2 |
| C.物质③由2种元素组成 |
D.物质①和⑤发生反应转化为④的化学方程式为: |
【知识点】 碳单质与二氧化碳的反应解读 碳及其化合物间相互转化解读
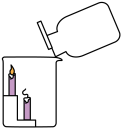
| A.实验室制取二氧化碳的药品为块状大理石和稀硫酸 |
| B.实验室可采用向上排空气法收集二氧化碳 |
| C.图示实验可说明二氧化碳密度比空气大 |
| D.图示实验可说明二氧化碳不支持蜡烛的燃烧 |
| A.不锈钢是绝对不会生锈的铁合金 |
| B.武德合金的熔点比其成分金属高 |
| C.日常生活中,钢铁表面刷油漆可以防止生锈 |
| D.“曾青得铁则化为铜”的原理是用铜置换出铁 |
| A.泥土与水混合不能形成溶液 |
| B.硝酸铵溶于水能使水温降低 |
| C.升高温度可使大多数固体物质的饱和溶液变为不饱和溶液 |
| D.饱和溶液的溶质质量分数一定大于不饱和溶液 |
【知识点】 判断物质是否能形成溶液解读 溶液浓稀与溶液饱和的关系解读
| A.D>C>A>B | B.A>B>C>D | C.B>A>C>D | D.D>C>B>A |
【知识点】 金属与盐溶液反应 金属活动性强弱的探究解读
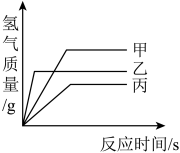
| A.完全反应所需时间:丙>甲>乙 | B.生成氢气的质量:甲>乙>丙 |
| C.相对原子质量:乙>丙>甲 | D.消耗硫酸的质量:甲>乙>丙 |
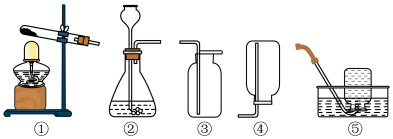
| A.装置①和③组合可以用来制取氢气 |
| B.装置②和③组合可以用来制取氧气 |
| C.装置②和⑤组合可以用来制取二氧化碳 |
| D.装置②可以控制反应的随时发生随时停止 |

| A.B处玻璃管内发生的化学反应是氧化还原反应,还原剂是CO |
| B.在点燃酒精喷灯前,应先通入CO气体排尽装置中的空气 |
| C.该实验可以观察到B处固体从黑色逐渐变成红色 |
| D.该模拟实验缺少尾气处理装置,会污染空气 |
【知识点】 一氧化碳还原氧化铁实验解读 污染性、可燃性尾气的处理解读

| A.①中所得溶液一定是不饱和溶液 |
| B.②③中所得溶液溶质的质量分数相等 |
| C.若②中溶液升温到30°C,溶液的质量一定不变 |
| D.若③中溶液恒温蒸发,溶质的质量分数一定变大 |
【知识点】 饱和溶液和不饱和溶液判断解读 溶质质量分数的涵义解读

| A.a的溶解度大于b的溶解度 |
| B.P点表示t1℃时a、c两物质溶解度相等 |
| C.将t1℃饱和的c溶液升温到t2℃,得到的是不饱和溶液 |
| D.将t2℃,a、b、c三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质量分数由大到小的顺序为:b>a=c |

| A.阴影区域中,A、C均处于不饱和状态 |
| B.除去B固体中含有的少量A杂质,可采用配成热饱和溶液,降温结晶、过滤、洗涤、干燥的方法提纯B |
| C.将A和B的饱和溶液从t2℃降到t1℃时,析出晶体的质量关系为A>B |
| D.t1℃时,将50g固体A加入到200g水中,所得溶液溶质的质量分数约为16.7% |
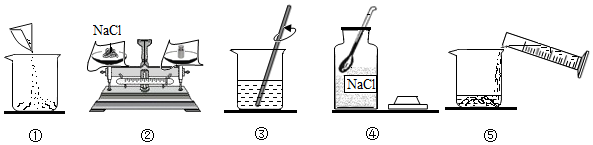
| A.实验操作顺序为④②①⑤③ |
| B.②中需称量NaCl的质量为16.0g |
| C.选用100mL量筒量取所需水的体积 |
| D.用量筒量取水时仰视读数所得溶液的溶质质量分数偏大 |
【知识点】 固体配制一定质量分数溶液解读
二、填空与简答 添加题型下试题
(1)地壳中含量最多的金属元素
(2)空气中含量最多的气体单质
(3)天然气的主要成分
(4)硝酸钾溶液中的阴离子
(5)铝在空气中具有很好的抗腐蚀性能的原因是
(6)用砂纸去除铝片表面的氧化膜,将其浸入硫酸铜溶液中,一段时间后,观察到铝片表面有红色物质析出,并有气泡产生,经检验气体为氢气。
①写出生成红色物质的化学方程式:
②硫酸铜溶液中的阳离子有
(7)放置的铁锅出现锈蚀,主要是铁与
(1)“众志成城、全民抗疫”必须依靠科学。下列是小浩一家人日常的抗疫措施,其中有科学依据且利用乳化原理的是
① 爷爷每天喝酒消毒② 奶奶靠吃保健品提高免疫力③ 爸爸将“84”消毒液稀释拖地④ 妈妈用汽油清洗衣服上的油污⑤ 姐姐用沐浴露洗澡⑥ 小浩用洗手液洗手
(2)低碳生活从细节做起,你的一个低碳举措是
(3)安全是永恒的主题。消防员用高压水枪灭火,主要依据的灭火原理是
(4)沼气可以作燃料,在大棚中燃烧沼气还可以提高作物产量,沼气的主要成分燃烧的微观示意图如下:

下列说法正确的是
A.该反应过程中
 与
与  的分子个数比为
的分子个数比为
B.该反应属于氧化反应
C.点燃沼气前需要检验其纯度防止发生爆炸
D.生成的
 可做气肥
可做气肥
三、实验题 添加题型下试题
(1)实验是学习化学的重要途径,对比法是一种常用的实验方法。请完成下列实验中的问题:
实验一:探究燃烧的条件

如图所示,为证明燃烧需要可燃物,可用玻璃棒分别蘸取蒸馏水和
实验二:探究铁锈性的条件

①试管
②通过对比试管B、C中的现象,可以得出铁生锈需要与
(2)在“宏观一微观一符号”之间建立联系,是学习化学特有的思维方式。一氧化碳燃烧的微观模拟示意图如下所示:

依据图中所给信息,回答下列问题:
①写出该反应的化学方程式:
②从微观角度分析
a、CO和CO2的组成元素相同,但化学性质不同,其原因是
b、化学反应前后

(1)写出标有序号的仪器名称:①
(2)图中装置A有明显错误,请指出
(3)改正后,若用氯酸钾制取氧气,可选择的发生装置为
(4)用双氧水和二氧化锰制取氧气时,可选用的装置组合是
(5)用B装置制取CO2,反应的化学方程式为
(6)实验室常用氯化铵固体与碱石灰固体共热来制取氮气,常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,NH3极易溶于水,制取并收集NH3,选择的装置组合是(填字母序号)
四、填空与简答 添加题型下试题

| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | 甲 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| 乙 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | |
(1)观察溶解度曲线和溶解度表,判断物质乙是指
(2)60℃时,饱和KNO3溶液中混有少量KCl,应采用
(3)60℃时,分别将等质量的KNO3和KCl两种物质的饱和溶液温度降至t ℃,析出晶体的质量关系为:KNO3
(4)如图所示,20℃时,将一定质量的KNO3固体放入盛水的试管中,发现有少量固体未溶解,向烧杯的水中加入某物质后,试管内固体能完全溶解。则加入的物质可以是

①冰块 ②生石灰固体 ③硝酸铵固体 ④干冰 ⑤浓硫酸 ⑥氢氧化钠固体
A ①③④ B ②⑤⑥ C ①③⑤ D ②④⑥
(5)60 ℃时,将45g KCl固体溶解于100 g水中,降温至20 ℃,析出晶体的质量是
五、科学探究题 添加题型下试题
【提出问题】M、铜、铝的金属活动性顺序是怎样的?
【猜想与假设】小敏的猜想是Al>Cu>M;小强的猜想是Al>M>Cu;你的猜想是
【设计与实验】为了探究三种金属的活动性顺序,同学们取粗细相同的M丝、铝丝及相关溶液,进行了如图所示的实验:

观察到只有试管乙中发生明显变化,那么试管乙中观察到的现象是
【交流与表达】(1)同学们一致认为试管丙中也应该有明显变化,之所以出现这种情况的原因可能是
(2)于是同学们对实验进行了改进,把甲、丙中的铝丝打磨干净后又分别插入原试管中,结果甲、丙试管中都出现了明显变化,则丙试管中发生反应的化学方程式为
【解释与结论】通过以上实验,同学们得出了三种金属的活动性顺序。
【评价与反思】实验结束后,同学们对实验过程进行了如下反思:
(1)同学们经过讨论后认为该实验可以优化,去掉试管
(2)除了上述实验外,还可以将铝丝、铜丝分别插入到盛有
【知识点】 金属活动性强弱的探究解读
六、计算题 添加题型下试题
第一次 | 第二次 | 第三次 | |
加入稀盐酸的体积/mL | 10 | 10 | 10 |
生成氢气的质量/g | 0.08 | 0.08 | 0.04 |
(2)求合金中铜的质量分数。
【知识点】 含杂质的化学方程式计算解读 金属与酸反应原理解读
试卷分析
试卷题型(共 27题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 判断物质是否能形成溶液 悬浊液、乳浊液 | 单选题 |
| 2 | 0.94 | 空气的污染与防治 | 单选题 |
| 3 | 0.94 | 燃烧的定义及条件 燃料充分燃烧的方法及其重要性 灭火原理与方法 化学反应中能量变化的实际应用 | 单选题 |
| 4 | 0.85 | 制取二氧化碳的原理 浓硫酸的物理、化学性质 酸的通性 | 单选题 |
| 5 | 0.85 | 浓溶液稀释配制一定质量分数溶液 浓硫酸的稀释 酸碱的腐蚀性及安全使用 | 单选题 |
| 6 | 0.85 | 金刚石的相关知识 石墨的相关知识 C60的相关知识 活性炭的吸附性 | 单选题 |
| 7 | 0.85 | 木炭还原氧化铜的实验 | 单选题 |
| 8 | 0.85 | 微粒的观点解释现象 硬水的危害及软化方法 乳化现象及应用 灭火原理与方法 | 单选题 |
| 9 | 0.85 | 碳单质与二氧化碳的反应 碳及其化合物间相互转化 | 单选题 |
| 10 | 0.65 | 制取二氧化碳的原理 制取二氧化碳的装置 二氧化碳物理性质及实验 二氧化碳不可燃、不支持燃烧性质 | 单选题 |
| 11 | 0.94 | 合金的认识 金属与盐溶液反应 金属的防锈措施 | 单选题 |
| 12 | 0.85 | 判断物质是否能形成溶液 溶液浓稀与溶液饱和的关系 | 单选题 |
| 13 | 0.65 | 金属与盐溶液反应 金属活动性强弱的探究 | 单选题 |
| 14 | 0.65 | 金属与酸反应原理 金属与酸反应的图像 | 单选题 |
| 15 | 0.85 | 过氧化氢制取氧气实验 氧气的制取中装置的选择 制取二氧化碳的装置 氢气的制备及应用 | 单选题 |
| 16 | 0.65 | 一氧化碳还原氧化铁实验 污染性、可燃性尾气的处理 | 单选题 |
| 17 | 0.65 | 饱和溶液和不饱和溶液判断 溶质质量分数的涵义 | 单选题 |
| 18 | 0.65 | 饱和溶液和不饱和溶液的转换 固体溶解度曲线的应用 溶质质量分数的涵义 | 单选题 |
| 19 | 0.65 | 固体溶解度曲线的应用 溶解度的相关计算 溶质质量分数的涵义 | 单选题 |
| 20 | 0.65 | 固体配制一定质量分数溶液 | 单选题 |
| 二、填空与简答 | |||
| 21 | 0.85 | 化学式书写及读法 铝与氧气反应原理及探究 金属与盐溶液反应 钢铁的锈蚀 | 填空题 |
| 22 | 0.85 | 微粒图像的分析及应用 乳化现象及应用 灭火原理与方法 爆炸、燃烧、缓慢氧化与自燃 | 填空题 |
| 25 | 0.65 | 结晶分离混合物 固体溶解度曲线的应用 固体溶解度的影响因素 溶解度的相关计算 | 填空题 |
| 三、实验题 | |||
| 23 | 0.65 | 微粒图像的分析及应用 探究铁生锈的条件 实验探究燃烧条件 控制变量法在实验设计中的应用 | |
| 24 | 0.65 | 过氧化氢制取氧气实验 氧气的制取中装置的选择 制取二氧化碳的原理 气体发生、收集装置 | |
| 四、科学探究题 | |||
| 26 | 0.4 | 金属活动性强弱的探究 | |
| 五、计算题 | |||
| 27 | 0.65 | 含杂质的化学方程式计算 金属与酸反应原理 | |



