20. 蜡烛是生活中常见的物品,随着社会进步和科学技术的发展,蜡烛逐渐从照明工具转化为装饰品和艺术品。小明同学对蜡烛展开研究。
Ⅰ.蜡烛的构成
(1)普通蜡烛由石蜡(主要成分为C
25H
52)和烛芯构成。制作时在烛芯中添加少量高锰酸钾可使蜡烛燃烧更旺,高锰酸钾分解的化学方程式为
_________。
Ⅱ.蜡烛的燃烧
(2)点燃蜡烛,将直角导管一端伸入内焰,另一端管口点燃有火焰产生,由此可知,“子火焰”由
________(填“固态”或“气态”)物质燃烧形成;撤去导管,将烧杯罩在蜡烛火焰上方,观察到烧杯内壁有黑色物质产生,该黑色物质是
_________,烧杯位置越低黑色物质越多,出现此现象的原因是
_________。

(3)查阅资料发现二氧化碳能与过氧化钠反应:
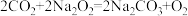
。取6g含碳量为84%的蜡烛,充分燃烧,将产生的CO
2通入足量过氧化钠使其完全吸收。
计算:
①该蜡烛中含有碳元素
__________g。
②过氧化钠完全吸收二氧化碳后产生的氧气质量是多少?(写出计算过程)
__________Ⅲ.蜡烛的发展
小明发现市面上有种“吹不灭的蜡烛”,需点燃30秒到60秒后再吹,吹灭后很快复燃。该蜡烛的烛芯上裹有一层打火石粉末,粉末中含单质镁、铝、铁中的一种,其着火点约为150℃。
【提出问题】
①粉末的成分是什么?
②为什么要点燃30秒后再吹?
【查阅资料】
镁、铝、铁都能溶于稀盐酸;铝能溶于氢氧化钠溶液,镁和铁不能。
【实验探究】
(4)将一支蜡烛在热水中熔化,取出烛芯,刮下表面银白色金属备用。
| 实验① | 取样于试管中,加入足量稀盐酸,观察到有气泡产生,反应后溶液呈无色,则该金属不可能是_________。 |
| 实验② | 取样于试管中,_________,该金属是镁。 |
(5)另取一支“吹不灭的蜡烛”,点燃后立即吹灭,发现蜡烛未复燃,从燃烧的条件分析,原因是
__________。