胃酸过多须服用抗酸药物(能与盐酸反应),常用的抗酸药物有碳酸氢钠片、铝碳酸镁片,兴趣小组的同学对这两种药物开展如下探究。
【查阅资料】①铝碳酸镁片的主要成分的化学式为AlMg(OH)3CO3;
活动一:定性探究抗酸药物与“胃酸”的反应。
(1)铝碳酸镁片中含有铝离子、镁离子、氢氧根离子和碳酸根离子。结合上述知识分析,该药物起抗酸作用的微粒是_____ (填化学符号)。
(2)小王取一定量碳酸氢钠片与4mLpH═1的稀盐酸(模拟胃酸)反应。药片中其他成分不溶于水也不参加反应。他对反应后溶液的成分产生了兴趣。
【作出猜想】
猜想 1:只含 NaCl;
猜想 2:_____ ;
猜想 3:NaCl、NaHCO3
【设计实验】
实验二中涉及反应的化学方程式为______ 。
活动二:定量探究抗酸药物与“胃酸”的反应,对比分析产生 CO2的速率快慢和中和酸的能力强弱。
如图 1,利用数字化实验分别测定碳酸氢钠片、铝碳酸镁片与“胃酸”反应时,产生 CO2的速率快慢和 pH的变化,得到“二氧化碳浓度与时间”曲线(如图 2)、“pH与时间”曲线(如图 3)。
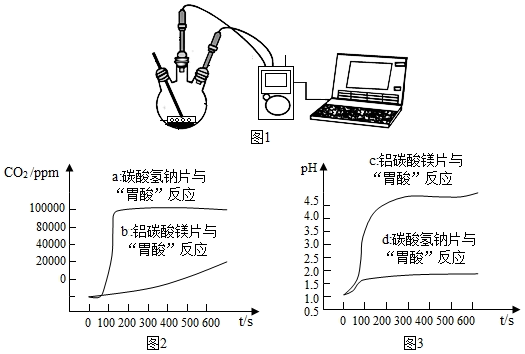
(1)服用碳酸氢钠片更易造成胃胀气,原因是_____ 。
(2)铝碳酸镁片中和酸的能力更强,理由是_____ 。
【反思与提升】日常生活中,我们应该根据个人的具体病情,选择合适种类的胃药。
【查阅资料】①铝碳酸镁片的主要成分的化学式为AlMg(OH)3CO3;
②抗酸原理:抗酸药物中的离子和胃酸中的氢离子反应,降低胃液酸性。
活动一:定性探究抗酸药物与“胃酸”的反应。
(1)铝碳酸镁片中含有铝离子、镁离子、氢氧根离子和碳酸根离子。结合上述知识分析,该药物起抗酸作用的微粒是
(2)小王取一定量碳酸氢钠片与4mLpH═1的稀盐酸(模拟胃酸)反应。药片中其他成分不溶于水也不参加反应。他对反应后溶液的成分产生了兴趣。
【作出猜想】
猜想 1:只含 NaCl;
猜想 2:
猜想 3:NaCl、NaHCO3
【设计实验】
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 取一定量反应后的溶液于试管中,滴加 | 无明显现象 | 猜想 3错误 |
| 实验二 | 另取一定量反应后的溶液于试管中, | 猜想 2正确 |
实验二中涉及反应的化学方程式为
活动二:定量探究抗酸药物与“胃酸”的反应,对比分析产生 CO2的速率快慢和中和酸的能力强弱。
如图 1,利用数字化实验分别测定碳酸氢钠片、铝碳酸镁片与“胃酸”反应时,产生 CO2的速率快慢和 pH的变化,得到“二氧化碳浓度与时间”曲线(如图 2)、“pH与时间”曲线(如图 3)。

(1)服用碳酸氢钠片更易造成胃胀气,原因是
(2)铝碳酸镁片中和酸的能力更强,理由是
【反思与提升】日常生活中,我们应该根据个人的具体病情,选择合适种类的胃药。
更新时间:2020-05-11 18:05:13
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某课外活动小组的同学在整理化学药品柜时,发现一瓶标签受损的无色液体,如图所示。

老师告诉大家,该瓶液体是下列5种液体中的某一种:稀H2SO4、H2O、NaNO3溶液、NaOH溶液、CuSO4溶液。
(1)根据以上信息判断,该无色液体一定不是_________ 和 _________ 。
(2)为确定该液体的成分,同学们设计了下列实验方案,请你一起探究。
(3)
(4)实验操作②中发生反应的化学方程式是_____________________________ 。

老师告诉大家,该瓶液体是下列5种液体中的某一种:稀H2SO4、H2O、NaNO3溶液、NaOH溶液、CuSO4溶液。
(1)根据以上信息判断,该无色液体一定不是
(2)为确定该液体的成分,同学们设计了下列实验方案,请你一起探究。
| 实验操作 | 实验现象 | 实验结论 |
| ①取该液体适量于试管中,向其中滴加无色酚酞溶液。 | 溶液颜色无变化。 | 该液体不是 |
| ②另取该液体适量于试管中,向其中加入锌粒。 | 该液体是稀H2SO4,不是NaNO3溶液。 |
(3)
(4)实验操作②中发生反应的化学方程式是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】小明在做实验时,不小心将镁条掉入到碳酸氢钠溶液中,发现产生大量的气泡和白色不溶物。他非常好奇,进行了如下探究。
【提出问题】镁条与碳酸氢钠溶液反应,产生的气体和白色不溶物分别是什么?
【查阅资料】
①MgHCO3能溶于水;Mg(OH)2、MgCO3难溶于水。
②Mg(OH)2、MgCO3受热易分解,分别生成两种氧化物。
③碱石灰的主要成分为氧化钙和氢氧化钠。
【作出猜想】
小明认为白色不溶物的组成存在3种可能,分别为①Mg(OH)2②MgCO3③_______ 。
【进行实验】
探究镁条与碳酸氢钠溶液反应产生什么气体
通过上述实验得到的结论是_______ 。
探究镁条与碳酸氢钠反应后产生的白色不溶物中是否含有MgCO3
定量测定白色不溶物的组成,老师的帮助下,小明设计了如下装置进行实验。

(1)实验中通过A中浓硫酸的吸收作用可判断白色不溶物_______ (填Mg(OH)2或MgCO3)是否存在,C中碱石灰的作用是_______ 。
(2)若白色不溶物为22.6g,实验前后装置A增重1.8g,装置B增重8.8g,则该白色不溶物的组成及质量比为_______ 。
【提出问题】镁条与碳酸氢钠溶液反应,产生的气体和白色不溶物分别是什么?
【查阅资料】
①MgHCO3能溶于水;Mg(OH)2、MgCO3难溶于水。
②Mg(OH)2、MgCO3受热易分解,分别生成两种氧化物。
③碱石灰的主要成分为氧化钙和氢氧化钠。
【作出猜想】
小明认为白色不溶物的组成存在3种可能,分别为①Mg(OH)2②MgCO3③
【进行实验】
探究镁条与碳酸氢钠溶液反应产生什么气体
| 实验操作 | 实验现象 |
| ①点燃产生的气体 | 气体燃烧,产生蓝色火焰 |
| ②火焰上罩内壁涂有石灰水的烧杯 | 无现象 |
探究镁条与碳酸氢钠反应后产生的白色不溶物中是否含有MgCO3
| 实验操作及现象 | 实验结论 |
| 白色不溶物中一定含有MgCO3 |

(1)实验中通过A中浓硫酸的吸收作用可判断白色不溶物
(2)若白色不溶物为22.6g,实验前后装置A增重1.8g,装置B增重8.8g,则该白色不溶物的组成及质量比为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】在探究酸和碱的化学性质时,同学们准备了四支试管,分别装入如下图所示的物质,然后加入相应的物质进行实验。回答下列问题。

(1)小玉向试管①中加入稀硫酸后观察到的现象是_____ ,发生反应的化学方程式为_____ 。
(2)小刚向试管②中滴加稀盐酸后,发现试管中产生无色气泡。小刚对反应后试管中溶液的溶质成分产生了好奇,经过思考后,他提出以下猜想:
I.只含有NaCl
II. NaCl和HCl
III. NaCl和Na2 CO3
IV. NaCl、HCl和Na2CO3
小明认为小刚的猜想_____ 不合理,理由是_____ 。
(3)小红向试管③中加入稀盐酸后,没有观察到明显现象。为了证明NaOH溶液能够和稀盐酸发生化学反应,小红提出,可以先向装有NaOH溶液的试管中滴加几滴_____ ,再加入足量的稀盐酸,就可以观察到_____ ,从而证明二者发生了化学反应。
(4)小兰向试管④中通入CO2,一段时间后也没有观察到明显现象。她又向试管④中滴加几滴稀盐酸,也没有观察到有气泡产生。于是她得出结论,NaOH溶液与CO2不反应。但是小强不同意小兰的结论,小强的理由是_____ 。

(1)小玉向试管①中加入稀硫酸后观察到的现象是
(2)小刚向试管②中滴加稀盐酸后,发现试管中产生无色气泡。小刚对反应后试管中溶液的溶质成分产生了好奇,经过思考后,他提出以下猜想:
I.只含有NaCl
II. NaCl和HCl
III. NaCl和Na2 CO3
IV. NaCl、HCl和Na2CO3
小明认为小刚的猜想
(3)小红向试管③中加入稀盐酸后,没有观察到明显现象。为了证明NaOH溶液能够和稀盐酸发生化学反应,小红提出,可以先向装有NaOH溶液的试管中滴加几滴
(4)小兰向试管④中通入CO2,一段时间后也没有观察到明显现象。她又向试管④中滴加几滴稀盐酸,也没有观察到有气泡产生。于是她得出结论,NaOH溶液与CO2不反应。但是小强不同意小兰的结论,小强的理由是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】实验室中有一包白色粉末,可能是碳酸钠,也可能是氧化钙或氢氧化钙。为确定其组成,某同学设计了以下实验方案进行探究,请你按要求帮助完成探究活动。
(1)提出假设:
假设① 白色粉末是碳酸钠
假设② 白色粉末是氧化钙
假设③ 白色粉末是氢氧化钙
(2)设计实验,通过实验分析进行判断并填空:
(3)实验后思考:假定这包白色粉末是混有少量氧化钙的碳酸钠粉末,将混合物溶于水可观察到的现象是____________ ;若恰好完全反应,将反应后的混合物进行分离,分离的方法是________ ;再将分离后的溶液蒸干,得到的固体物质是______ (填化学式)。
(1)提出假设:
假设① 白色粉末是碳酸钠
假设② 白色粉末是氧化钙
假设③ 白色粉末是氢氧化钙
(2)设计实验,通过实验分析进行判断并填空:
| 假设 | 设计的相关实验操作 | 实验中观察到的现象 | 假设是否成立 |
| ① | 取一定量粉末加入稀盐酸 | 假设①不成立 | |
| ② | 取一定量粉末溶于水 | 溶液浑浊且温度升高 | 假设②成立 |
| ③ | 取一定量粉末溶于水,静置后取上层清液再通入二氧化碳 | 没有沉淀产生 | 假设③ |
(3)实验后思考:假定这包白色粉末是混有少量氧化钙的碳酸钠粉末,将混合物溶于水可观察到的现象是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】果蔬洗涤盐能有效除去水果和蔬菜表面的农药,又能杀菌消毒。如图所示是某品牌果蔬洗涤盐说明书的部分内容,某兴趣小组对果蔬洗涤盐进行了探究。
【提出问题1】食用盐的来源?
【分析讨论】
(1)海水中含有大量的食盐,蒸发海水得到粗盐,粗盐经过溶解、沉淀、_______ 、蒸发、结晶等处理得到初步提纯的食用盐。
【提出问题2】果蔬洗涤盐中还有什么成分?
【查阅资料】①果蔬洗涤盐的成分除食用盐,还可能有碳酸钠、碳酸氢钠等;
②碳酸钠很稳定,受热不分解;碳酸氢钠不稳定,受热易分解,生成碳酸钠、水和二氧化碳;
③碳酸氢钠不与氯化钙溶液反应。
【作出猜想】猜想一:碳酸钠猜想二:碳酸氢钠猜想三:碳酸钠和碳酸氢钠。
(2)【进行实验】
【表达交流】
(3)实验1:发生反应的化学方程式为_______ 。
(4)实验2:实验结束时先从试管B中拿出导管,再停止给试管A加热,这样操作的目的是_______ 。
(5)实验1中的氯化钙溶液换成稀盐酸能否达到实验目的,并说明理由_______ 。
【反思总结】
果蔬洗涤盐不能直接食用。
(6)生活中使用和存放果蔬洗涤盐时应注意_______ 。
| 主要成分:食用盐、……、表面活化剂 使用方法:将本品溶于清水中,将蔬菜水果浸泡其中5分钟,取出再用清水冲洗干净即可。 |
【分析讨论】
(1)海水中含有大量的食盐,蒸发海水得到粗盐,粗盐经过溶解、沉淀、
【提出问题2】果蔬洗涤盐中还有什么成分?
【查阅资料】①果蔬洗涤盐的成分除食用盐,还可能有碳酸钠、碳酸氢钠等;
②碳酸钠很稳定,受热不分解;碳酸氢钠不稳定,受热易分解,生成碳酸钠、水和二氧化碳;
③碳酸氢钠不与氯化钙溶液反应。
【作出猜想】猜想一:碳酸钠猜想二:碳酸氢钠猜想三:碳酸钠和碳酸氢钠。
(2)【进行实验】
| 实验操作 | 实验现象 | 实验结论 |
| 实验1:取少量果蔬洗涤盐于烧杯中,加适量水溶解,滴加氯化钙溶液 | 猜想三正确 | |
实验2: |
【表达交流】
(3)实验1:发生反应的化学方程式为
(4)实验2:实验结束时先从试管B中拿出导管,再停止给试管A加热,这样操作的目的是
(5)实验1中的氯化钙溶液换成稀盐酸能否达到实验目的,并说明理由
【反思总结】
果蔬洗涤盐不能直接食用。
(6)生活中使用和存放果蔬洗涤盐时应注意
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】以饱和NaCl溶液和饱和NH4HCO3溶液为原料制备NaHCO3的原理为:
NaCl + NH4HCO3 = NaHCO3↓ + NH4Cl。为了探究NaHCO3析出的最佳条件,完成以下几组实验:(已知NaHCO3在40℃受热易分解)
回答下列问题:
(1)为了探究在相同的反应温度下,反应时间对NaHCO3产率的影响,可选用______ (填选项)进行对比研究。
A.实验a和b B.实验b和d C.实验c和d D.实验d和e
(2)实验a和c的目的是____________ 。
(3)从经济效益的角度考虑,NaHCO3析出的最佳条件是________ (填选项)。
A.30℃、60 min B.30℃、120 min C.35℃、60min D.35℃、120min
(4)在相同反应时间, 40℃时NaHCO3的产率比35℃时低的原因是_______
NaCl + NH4HCO3 = NaHCO3↓ + NH4Cl。为了探究NaHCO3析出的最佳条件,完成以下几组实验:(已知NaHCO3在40℃受热易分解)
| 实验序号 | 反应温度/℃ | 反应时间/min | NaHCO3产率/% |
| a | 30 | 60 | 86.8 |
| b | 30 | 120 | 91.1 |
| c | 35 | 60 | 89.4 |
| d | 35 | 120 | 92.5 |
| e | 40 | 60 | 85.3 |
回答下列问题:
(1)为了探究在相同的反应温度下,反应时间对NaHCO3产率的影响,可选用
A.实验a和b B.实验b和d C.实验c和d D.实验d和e
(2)实验a和c的目的是
(3)从经济效益的角度考虑,NaHCO3析出的最佳条件是
A.30℃、60 min B.30℃、120 min C.35℃、60min D.35℃、120min
(4)在相同反应时间, 40℃时NaHCO3的产率比35℃时低的原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
真题
名校
【推荐1】为探究盐酸的化学性质,某化学小组做了如下实验:
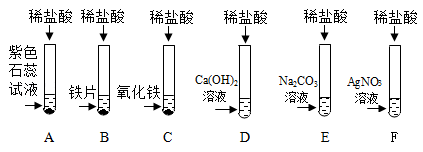
(1)上述反应中无现象的为_______ (填字母序号,下同),有白色沉淀出现的是_______ ;B试管中所发生反应的化学方程式为_______________________________ 。
(2)将反应后D和E试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行
探究。
【提出问题】滤液中溶质的成分是什么?
【假设与猜想】猜想一:NaCl 猜想二:NaCl和CaCl2
猜想三:NaCl、Ca(OH)2和HCl 猜想四:_____
【讨论与交流】经讨论,同学们一致认为猜想________ 是错误的。
【实验与结论】
【拓展与迁移】稀盐酸和稀硫酸有相似的化学性质,是因为它们的溶液中都存在__________ 。

(1)上述反应中无现象的为
(2)将反应后D和E试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行
探究。
【提出问题】滤液中溶质的成分是什么?
【假设与猜想】猜想一:NaCl 猜想二:NaCl和CaCl2
猜想三:NaCl、Ca(OH)2和HCl 猜想四:
【讨论与交流】经讨论,同学们一致认为猜想
【实验与结论】
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,滴加适量碳酸钠溶液 | 无现象 | 猜想四成立 |
| 取少量滤液于试管中,滴加适量 |
【拓展与迁移】稀盐酸和稀硫酸有相似的化学性质,是因为它们的溶液中都存在
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】几位同学对蜡烛燃烧火焰的焰心进行了以下探究,请你完成其中的步骤:
(1)点燃蜡烛,将一根小木条迅速平放入火焰中,约1s后取出,现象如图,这证明焰心_____________ 。

(2)向焰心斜向插入一支细短玻璃管,发现玻璃管中无明显现象(如图),在玻璃管的上口点燃,上口产生火焰,这说明焰心物质的性质是____________ 、___________ 。

(3)猜想和验证
资料:一氧化碳在加热的条件下能将黑色的氧化铜还原为红色的铜。
(1)点燃蜡烛,将一根小木条迅速平放入火焰中,约1s后取出,现象如图,这证明焰心

(2)向焰心斜向插入一支细短玻璃管,发现玻璃管中无明显现象(如图),在玻璃管的上口点燃,上口产生火焰,这说明焰心物质的性质是

(3)猜想和验证
资料:一氧化碳在加热的条件下能将黑色的氧化铜还原为红色的铜。
| 猜想 | 操作 | 现象 | 结论 |
| 假设①:焰心气体含 CO2 | 在未点燃的短玻璃管上口 | 假设①不成立 | |
| 假设②:焰心气体含CO | 用表面烧黑的灼热铜丝迅速插入短玻璃管上口 | 烧黑的铜丝变成红色 | |
| 假设③:焰心气体含石蜡蒸气 | 取一较长的细玻璃管,用湿冷毛巾包住中部,将玻璃管下端插入焰心,上端试用火焰点燃 | 假设③成立 | |
| 取下长玻璃管,打开湿毛巾 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】实验室有一瓶常用无色液体的标签模糊了(如图)。为确定该瓶溶液的溶质是什么,同学们进行了如下探究。

【提出问题】这瓶溶液的溶质是什么?
【作出猜想】
(1)猜想①:NaOH;猜想②:Na2CO3;猜想③:NaCl;猜想④:NH4Cl。同学们一致认为猜想___ 不成立。
【查阅资料】在一定浓度的溶液中,有微溶物生成的复分解反应也能发生。
【实验探究】
(2)同学们设计不同方案进行如下实验,请完成如表。
【交流讨论】
(3)同学们经过讨论,认为方案一不严密,理由是_____ (用化学方程式表示)。
(4)鉴别该瓶溶液溶质的成分,还可以用下列试剂_____ (填字母序号)。
A. MgCl2溶液、稀盐酸
B. Ba(NO3)2溶液、酚酞
C. AgNO3溶液
D. 澄清石灰水

【提出问题】这瓶溶液的溶质是什么?
【作出猜想】
(1)猜想①:NaOH;猜想②:Na2CO3;猜想③:NaCl;猜想④:NH4Cl。同学们一致认为猜想
【查阅资料】在一定浓度的溶液中,有微溶物生成的复分解反应也能发生。
【实验探究】
(2)同学们设计不同方案进行如下实验,请完成如表。
| 实验方案 | 实验操作 | 实验现象 | 实验结论 |
| 方案一 | 取2mL该无色溶液于试管中,滴加CaCl2溶液 | 溶液变浑浊 | 猜想②成立 |
| 方案二 | 取2mL该无色溶液,滴入装有2mL稀盐酸的试管中 | 猜想②成立 | |
| 方案三 | 用 | 试纸变色,对照标准比色卡,pH>7 | 猜想 |
【交流讨论】
(3)同学们经过讨论,认为方案一不严密,理由是
(4)鉴别该瓶溶液溶质的成分,还可以用下列试剂
A. MgCl2溶液、稀盐酸
B. Ba(NO3)2溶液、酚酞
C. AgNO3溶液
D. 澄清石灰水
您最近一年使用:0次




