氯碱工业以粗盐(主要成分是NaCl,含少量泥沙、CaCl2、 MgCl2)为原料,生产氯气和氢氧化钠,模拟流程如图:
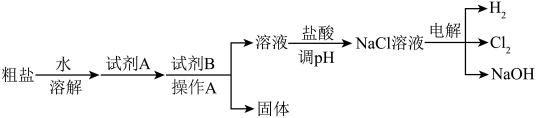
(1)试剂A与试剂B的组合为____ (填序号)。
①KOH ②NaOH ③K2CO3 ④Na2CO3
(2)操作A需使用玻璃棒,玻璃棒的作用是________ 。
(3)流程中Mg元素必须转化成________ (填化学式)才能完全除去。
(4)写出电解NaCl溶液的化学方程式____________ 。

(1)试剂A与试剂B的组合为
①KOH ②NaOH ③K2CO3 ④Na2CO3
(2)操作A需使用玻璃棒,玻璃棒的作用是
(3)流程中Mg元素必须转化成
(4)写出电解NaCl溶液的化学方程式
更新时间:2020-05-16 22:24:59
|
相似题推荐
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】请用化学方程式表示下列反应原理。
(1)用生石灰做干燥剂。_______________________
(2)废旧钢铁制品表面的铁锈可以用稀盐酸除去。_______________________
(3)可以用氢氧化钡来除去氢氧化钠溶液中混有的碳酸钠杂质。_______________________
(1)用生石灰做干燥剂。
(2)废旧钢铁制品表面的铁锈可以用稀盐酸除去。
(3)可以用氢氧化钡来除去氢氧化钠溶液中混有的碳酸钠杂质。
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】小艾同学以稀硫酸为主题,绘制的“多彩酸世界”思维导图如下。结合图示信息回答有关问题:_______ (填名称)。
(2)若用Cu(OH)2实现②,会得到_______ 色溶液。
(3)若想实现③,得到浅绿色溶液,选用的单质是_______ (填物质名称)。
(4)若想实现④,得到黄色溶液,可选用的金属氧化物是_______ (填化学式)。
(5)若选用BaCl2溶液实现⑤,此反应的化学方程式为_______ 。

(2)若用Cu(OH)2实现②,会得到
(3)若想实现③,得到浅绿色溶液,选用的单质是
(4)若想实现④,得到黄色溶液,可选用的金属氧化物是
(5)若选用BaCl2溶液实现⑤,此反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】请对以下方案及现象做出合理补充或解释:
(1)将NaOH溶液滴在________ 上,再与标准比色卡比较,便可粗略测定氢氧化钠溶液的酸碱度。
(2)用一种试剂分别与食盐水、氢氧化钠溶液、稀硫酸作用,就能把它们直接鉴别出来,这种试剂是________ 。
(3)不能服用NaOH治疗胃酸过多,原因是NaOH具有______ 性。
(4)用Na2CO3和KOH在溶液中进行反应制取NaOH,无法达到目的的原因是________ 。
(5)氢氧化钠暴露在空气中容易变质,是由于________ (用方程式表示),请用一种试剂检验氢氧化钠变质__________ ,除去氢氧化钠中少量碳酸钠用_______ 溶液。
(1)将NaOH溶液滴在
(2)用一种试剂分别与食盐水、氢氧化钠溶液、稀硫酸作用,就能把它们直接鉴别出来,这种试剂是
(3)不能服用NaOH治疗胃酸过多,原因是NaOH具有
(4)用Na2CO3和KOH在溶液中进行反应制取NaOH,无法达到目的的原因是
(5)氢氧化钠暴露在空气中容易变质,是由于
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】请分析下图知识网络完成下列问题:

(1)图中的X属于______ (填物质的类别);
(2)若非金属氧化物为二氧化碳,碱为氢氧化钠,请写出反应②的化学方程式______ ;
(3)请根据下表提供的部分物质的溶解性表,写出符合反应③的化学方程式______ 。

(1)图中的X属于
(2)若非金属氧化物为二氧化碳,碱为氢氧化钠,请写出反应②的化学方程式
(3)请根据下表提供的部分物质的溶解性表,写出符合反应③的化学方程式
| OH- |  |  | |
| K+ | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 不 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)按要求从氯化银、二氧化硫、氧化铝、碳酸中选取合适的物质,将其化学式填写在下列横线上。
①一种可导致酸雨的气体:________ ;②一种易分解的酸:__________ ;
③铝表面致密的氧化膜:__________ ;④一种难溶于水的盐:_________ 。
(2)电池的发明是贮能和供能技术的巨大进步,是化学对人类的一项重大贡献,极大地推进了现代化的进程,改变了人们的生活方式,提高了人们的生活质量。
表1:水果电池
Ⅰ.铅酸电池是一种电极主要由铅及其氧化物制成,电解液是硫酸溶液的蓄电池。_______ (填“增大”“减小”或“不变”)。
②铅蓄电池在放电时,是将_______ 能转化为电能。
Ⅱ.水果电池通常是用金属活动性较强的金属做负极,用金属活动性较弱的金属做正极,利用水果汁内的有机酸与活泼金属反应,导致回路中的电子定向移动形成稳定的电流。
①苹果中含有苹果酸,其化学式为C4H6O5。苹果酸中氢、氧元素的质量比为_________ (填最简整数比)。
②请简述用pH试纸测定水果果汁pH的方法____________________ 。
③某学习小组用大小、形状相同的铜片和锌片为电极研究水果电池,得到的实验数据如表1所示。下列说法中,正确的是_____ (填选项序号之一)。
A.该水果电池锌片为正极,铜片为负极
B.实验证明电极间距离越小,产生的电流越大
C.实验证明水果酸性越强,产生的电流越小
(1)按要求从氯化银、二氧化硫、氧化铝、碳酸中选取合适的物质,将其化学式填写在下列横线上。
①一种可导致酸雨的气体:
③铝表面致密的氧化膜:
(2)电池的发明是贮能和供能技术的巨大进步,是化学对人类的一项重大贡献,极大地推进了现代化的进程,改变了人们的生活方式,提高了人们的生活质量。
表1:水果电池
| 水果种类 | 果汁pH | 电极间距/cm | 电流大小/A |
| 西红柿 | 3.1 | 1 | 98.7 |
| 西红柿 | 3.1 | 2 | 72.5 |
| 苹果 | 3.8 | 2 | 27.2 |

②铅蓄电池在放电时,是将
Ⅱ.水果电池通常是用金属活动性较强的金属做负极,用金属活动性较弱的金属做正极,利用水果汁内的有机酸与活泼金属反应,导致回路中的电子定向移动形成稳定的电流。
①苹果中含有苹果酸,其化学式为C4H6O5。苹果酸中氢、氧元素的质量比为
②请简述用pH试纸测定水果果汁pH的方法
③某学习小组用大小、形状相同的铜片和锌片为电极研究水果电池,得到的实验数据如表1所示。下列说法中,正确的是
A.该水果电池锌片为正极,铜片为负极
B.实验证明电极间距离越小,产生的电流越大
C.实验证明水果酸性越强,产生的电流越小
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】水是一种重要的自然资源,是生活、生产必不可少的物质。请回答下列问题:
(1)在实验室里,若要得到净化程度最高的水,可用_______________ 的方法;实验室蒸发食盐水时用到的仪器有_______________ (填序号)。
①带铁圈的铁架台 ②酒精灯 ③漏斗 ④玻璃棒 ⑤量筒 ⑥蒸发皿
(2)鱼类可以在水中呼吸,是因为水中溶有_______________ 。水还是一种良好的溶剂,下列物质在水中能配成溶液的是_____________ (填字母)
A 氢氧化镁
B 氯化镁
C 植物油
D 金属镁
(3)在沉淀池中,经常用到生石灰。生石灰与水反应的化学方程式为_______________ 。净水器常用活性炭,主要是利用活性炭的_______________ 性。
(1)在实验室里,若要得到净化程度最高的水,可用
①带铁圈的铁架台 ②酒精灯 ③漏斗 ④玻璃棒 ⑤量筒 ⑥蒸发皿
(2)鱼类可以在水中呼吸,是因为水中溶有
A 氢氧化镁
B 氯化镁
C 植物油
D 金属镁
(3)在沉淀池中,经常用到生石灰。生石灰与水反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】在抗击“新冠肺炎病毒”期间,消毒剂在公共场所进行卫生防疫时发挥着重要作用。二氧化氯( )是一种高效、广谱、安全的杀菌消毒剂。以粗盐水(含可溶性杂质
)是一种高效、广谱、安全的杀菌消毒剂。以粗盐水(含可溶性杂质 、
、 )为原料,制取
)为原料,制取 的工艺流程如图:
的工艺流程如图:

(1)步骤②加入的试剂A是________ (填写化学式)。
(2)固体乙的成分是_______ (填写化学式)。
(3)步骤③加入适量盐酸的目的是__________ 。
(4)步骤④中是氯化钠水溶液在通电的条件下反应,生成氯酸钠(NaClO3)和氢气,该反应的化学方程式为_______ 。
(5)步骤⑤中涉及的反应物和生成物中含氯元素化合价最高的物质是________ (填写化学式)。
 )是一种高效、广谱、安全的杀菌消毒剂。以粗盐水(含可溶性杂质
)是一种高效、广谱、安全的杀菌消毒剂。以粗盐水(含可溶性杂质 、
、 )为原料,制取
)为原料,制取 的工艺流程如图:
的工艺流程如图:
(1)步骤②加入的试剂A是
(2)固体乙的成分是
(3)步骤③加入适量盐酸的目的是
(4)步骤④中是氯化钠水溶液在通电的条件下反应,生成氯酸钠(NaClO3)和氢气,该反应的化学方程式为
(5)步骤⑤中涉及的反应物和生成物中含氯元素化合价最高的物质是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】某小组的同学为了将氯化钠和氯化钙两种固体分离,设计了以下实验方案:

请根据上述操作流程,回答下列问题:
(1)加入碳酸钠溶液至过量的目的是__________ 。
(2)B物质是(填化学式)__________ ,C 溶液中的溶质有________ 和HCl ,滤液中的溶质有___________ 、____________ 。
(3)操作②的名称是_____________ ,操作④的名称是_____________ 。
(4)在进行第⑤步操作前,应向滤液中加入足量的盐酸,其目的是___________ ,有关化学方程式为_____________ 。

请根据上述操作流程,回答下列问题:
(1)加入碳酸钠溶液至过量的目的是
(2)B物质是(填化学式)
(3)操作②的名称是
(4)在进行第⑤步操作前,应向滤液中加入足量的盐酸,其目的是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】地球是一颗美丽的蓝色星球,海水占了全球水资源的97%。海水资源的开发和利用具有非常广阔的前景。海水中含有大量的NaCl,可用于制备钠及其化合物,其流程如图:
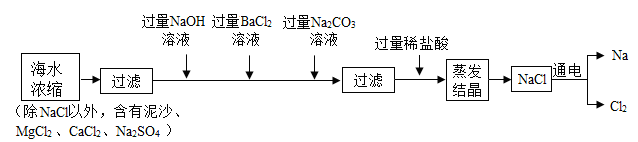
(1)加入过量Na2CO3溶液的目的是除去______ 。
(2)写出流程中制备钠的化学方程式______ ,若制得 23 kg金属钠,至少需要NaCl的质量为______ kg。
(3)实验所得NaCl质量______ 浓缩海水中的氯化钠质量(选填“大于”、“小于”或“等于”)。

(1)加入过量Na2CO3溶液的目的是除去
(2)写出流程中制备钠的化学方程式
(3)实验所得NaCl质量
您最近一年使用:0次



