某小组同学做氧化铜与稀盐酸反应的兴趣实验,发现有的同学得到蓝色溶液,有的同学得到绿色溶液。老师提示这种现象可能与所得氯化铜溶液有关。于是,同学们对这个现象进行探究。
实验1:探究影响氯化铜溶液颜色的因素
取溶质质量分数不同的氯化铜溶液各20 mL置于同样的烧杯中,分别置于不同温度的水浴箱中加热(忽略溶剂蒸发)。待溶液温度恒定后,观察溶液颜色,记录如下:
实验2:探究室温下氯化铜溶液的变色浓度范围
a 室温下,称取15.4g的氯化铜固体溶于35.0g水中,配制成溶质质量分数30.6%的氯化铜溶液。
b 将上述氯化铜溶液依次加入等质量的水稀释,配制成不同溶质质量分数的氯化铜溶液,观察溶液颜色,记录如下:
【结果与讨论】
(1)氧化铜和稀盐酸反应的化学方程式为______ 。
(2)实验1中,④⑤⑥的实验目的是______ 。
(3)根据实验1的结果可知,③⑥⑨中影响氯化铜溶液颜色的因素是______ 。
(4)实验2中,步骤a中用到的玻璃仪器有量筒、滴管、玻璃棒和________ 。
【反思与评价】
(5)室温下,小文将20g氯化铜固体溶于80g水中,则此溶液的颜色为______ 。
(6)小昕配制了一杯质量分数为12%的氯化铜溶液,溶液为浅蓝色,若要使此溶液由蓝向绿色转变,可进行的操作有______ (填字母序号)。
A 将溶液放在水浴箱中加热到70°C
B 加入适量的氯化铜固体并使之溶解
C 加入适量的水稀释
实验1:探究影响氯化铜溶液颜色的因素
取溶质质量分数不同的氯化铜溶液各20 mL置于同样的烧杯中,分别置于不同温度的水浴箱中加热(忽略溶剂蒸发)。待溶液温度恒定后,观察溶液颜色,记录如下:
| 烧杯编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
| 溶质质量分数/ % | 5 | 5 | 5 | 10 | 10 | 10 | 20 | 20 | 20 |
| 水浴箱 温度/°C | 30 | 50 | 70 | 30 | 50 | 70 | 30 | 50 | 70 |
| 溶液颜色 | 浅蓝 | 浅蓝 | 蓝 | 蓝 | 蓝绿 | 翠绿 | 蓝绿 | 翠绿 | 墨绿 |
a 室温下,称取15.4g的氯化铜固体溶于35.0g水中,配制成溶质质量分数30.6%的氯化铜溶液。
b 将上述氯化铜溶液依次加入等质量的水稀释,配制成不同溶质质量分数的氯化铜溶液,观察溶液颜色,记录如下:
| 溶质质量分数/ % | 30.6 | 25.5 | 21.9 | 19.2 | 17.0 | 15.3 |
| 溶液颜色 | 深绿 | 翠绿 | 蓝绿 | 蓝绿 | 蓝 | 浅蓝 |
(1)氧化铜和稀盐酸反应的化学方程式为
(2)实验1中,④⑤⑥的实验目的是
(3)根据实验1的结果可知,③⑥⑨中影响氯化铜溶液颜色的因素是
(4)实验2中,步骤a中用到的玻璃仪器有量筒、滴管、玻璃棒和
【反思与评价】
(5)室温下,小文将20g氯化铜固体溶于80g水中,则此溶液的颜色为
(6)小昕配制了一杯质量分数为12%的氯化铜溶液,溶液为浅蓝色,若要使此溶液由蓝向绿色转变,可进行的操作有
A 将溶液放在水浴箱中加热到70°C
B 加入适量的氯化铜固体并使之溶解
C 加入适量的水稀释
2020九年级下·北京·专题练习 查看更多[6]
(已下线)2020年北京9区中考一模化学试题分类汇编-科学探究2020年北京市海淀区中考一模化学试题(已下线)北京市2020年一、二模汇编-科学探究2020年安徽省合肥市瑶海区卓越中学中考模拟化学试题(已下线)必刷卷01-2021年中考化学考前信息必刷卷(北京专用)北京市海淀区北京一零一中学2021--2022学年九年级下学期3月月考化学试题
更新时间:2020-05-22 07:06:55
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某实验小组的同学利用氢氧化钠溶液和稀盐酸进行酸碱中和反应的实验时,他们在向盛有氢氧化钠溶液的烧杯中滴加一定量的稀盐酸后,才发现忘记滴加了酸碱指示剂,此时,他们停止滴加稀盐酸,并对烧杯内溶液中所含溶质的成分 进行探究。
【提出猜想】
猜想一:只有NaCl 猜想二:______________ 猜想三:NaCl和NaOH
【实验设计与验证】
(1)小猛同学设计用无色酚酞溶液验证“猜想一”是否成立。取少量上述实验中烧杯里的溶液于试管中,并向试管中滴加几滴无色酚酞溶液,振荡,观察到溶液不变色。于是可以确定“猜想三”不成立,其理由是_________________ ;
(2)小华同学设计用碳酸钠溶液验证“猜想一”和“猜想二”是否成立。取少量上述实验中烧杯里的溶液于试管中,并向试管中逐滴加入碳酸钠溶液,观察到的现象是:有_____ 生成,于是可以确定_______ 成立。
【交流与反思】
经过同学们讨论和交流,发现只需用下列一种物质就能验证得出以上三种猜想中的哪一种猜想成立,请在下列物质的选项中选择出你认为合理的物质是________ (填序号)
A.锌粒 B.紫色石蕊溶液 C.二氧化碳
【提出猜想】
猜想一:只有NaCl 猜想二:
【实验设计与验证】
(1)小猛同学设计用无色酚酞溶液验证“猜想一”是否成立。取少量上述实验中烧杯里的溶液于试管中,并向试管中滴加几滴无色酚酞溶液,振荡,观察到溶液不变色。于是可以确定“猜想三”不成立,其理由是
(2)小华同学设计用碳酸钠溶液验证“猜想一”和“猜想二”是否成立。取少量上述实验中烧杯里的溶液于试管中,并向试管中逐滴加入碳酸钠溶液,观察到的现象是:有
【交流与反思】
经过同学们讨论和交流,发现只需用下列一种物质就能验证得出以上三种猜想中的哪一种猜想成立,请在下列物质的选项中选择出你认为合理的物质是
A.锌粒 B.紫色石蕊溶液 C.二氧化碳
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】某同学发现家里的铜质水龙头表面出现了一层绿色的锈渍,经查阅资料,了解到这层锈渍的化学成分是碱式碳酸铜[Cu2(OH)2CO3],并对Cu2(OH)2CO3受热完全分解后的产物进行探究。
【查阅资料】(1)碱式碳酸铜受热分解生成水蒸气、二氧化碳和一种黑色固体。
(2)白色无水硫酸铜遇水变成蓝色。
【提出猜想】该同学根据碱式碳酸铜的化学式对黑色固体产物作出以下猜想:
①可能是碳;
②可能是氧化铜;
③可能是碳和氧化铜的混合物。
他猜想的依据是_____ ,且碳和氧化铜都是黑色的。
【实验探究】实验Ⅰ:按下图进行实验,证明分解产物中有H2O和CO2(图中夹持装置省略)。
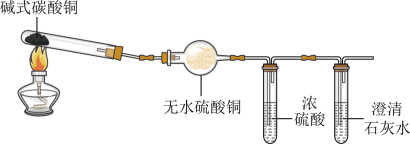
实验Ⅱ:为验证猜想,他做了如下实验:向盛有少量黑色固体的试管中加入足量的稀硫酸,振荡,待完全反应后静置,观察现象。
【实验分析及结论】
实验Ⅰ中:证明产物中有水生成的依据是_____ ;澄清石灰水变浑浊,产物中有_____ 生成。
实验Ⅱ中:因为黑色粉末溶逐渐消失且_____ ,所以猜想②正确,故碱式碳酸铜受热分解的化学方程式为_____ 。
通过上述实验及结论分析可知,铜质水龙头生锈过程中与水、二氧化碳、_____ 有关。
【实验反思】为了防止铜质水龙头生锈,通常可采取的有效措施是_____ 。
【拓展应用】依据碱式碳酸铜受热分解的产物及所学酸碱盐的知识,该同学认为可以用稀盐酸除去铜质水龙头表面的锈渍,反应的化学方程式为_____ 。
【查阅资料】(1)碱式碳酸铜受热分解生成水蒸气、二氧化碳和一种黑色固体。
(2)白色无水硫酸铜遇水变成蓝色。
【提出猜想】该同学根据碱式碳酸铜的化学式对黑色固体产物作出以下猜想:
①可能是碳;
②可能是氧化铜;
③可能是碳和氧化铜的混合物。
他猜想的依据是
【实验探究】实验Ⅰ:按下图进行实验,证明分解产物中有H2O和CO2(图中夹持装置省略)。

实验Ⅱ:为验证猜想,他做了如下实验:向盛有少量黑色固体的试管中加入足量的稀硫酸,振荡,待完全反应后静置,观察现象。
【实验分析及结论】
实验Ⅰ中:证明产物中有水生成的依据是
实验Ⅱ中:因为黑色粉末溶逐渐消失且
通过上述实验及结论分析可知,铜质水龙头生锈过程中与水、二氧化碳、
【实验反思】为了防止铜质水龙头生锈,通常可采取的有效措施是
【拓展应用】依据碱式碳酸铜受热分解的产物及所学酸碱盐的知识,该同学认为可以用稀盐酸除去铜质水龙头表面的锈渍,反应的化学方程式为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】用砂纸打磨过的镁条加入盛有稀盐酸的试管中,产生大量气泡,且试管发热。在分组实验中,部分小组的同学发现试管中出现白色不溶物。
【提出问题一】为什么有的小组会出现白色不溶物?
【实验探究一】在4支试管中分别加入相同质量、相同溶质质量分数的稀盐酸,形状大小相同、用砂纸打磨过的镁条,实验记录如下表:
【实验结论】通过上表可知,出现白色不溶物与_______ 有关。
【提出问题二】白色不溶物是什么?
【查阅资料】
①AgNO3与可溶性氯化物反应,生成不溶于水,也不与稀硝酸反应的白色沉淀;
② 和Mg(OH)C1均为白色固体,不溶于水但能与稀盐酸,稀硫酸等反应生成盐和水。
和Mg(OH)C1均为白色固体,不溶于水但能与稀盐酸,稀硫酸等反应生成盐和水。
【提出猜想】
猜想1:是没有参加反应的镁条
猜想2:是生成的 过多而析出晶体
过多而析出晶体
猜想3:是生成的 白色沉淀
白色沉淀
猜想4:是生成的Mg(OH)Cl白色沉淀。
【实验探究二】
将上述【实验探究一】D试管反应后的物质过滤,并将得到的白色不溶物分成三份,分别放入三支试管中进行实验。
【实验反思】
①同学对上述实验3的结论提出质疑,他认为实验3设计不严密,要验证猜想4是否成立,在进行实验3之前应该进行的操作是_______ 。
②老师的指导下,实验小组最终确定白色不溶物是Mg(OH)C1,请写出Mg(OH)C1与稀盐酸反应的化学方程式______ 。
【提出问题一】为什么有的小组会出现白色不溶物?
【实验探究一】在4支试管中分别加入相同质量、相同溶质质量分数的稀盐酸,形状大小相同、用砂纸打磨过的镁条,实验记录如下表:
| 试管 | A | B | C | D |
| 镁条的长度cm | 1 | 2 | 3 | 4 |
| 不溶物 | 无 | 少量 | 较多 | 很多 |
【提出问题二】白色不溶物是什么?
【查阅资料】
①AgNO3与可溶性氯化物反应,生成不溶于水,也不与稀硝酸反应的白色沉淀;
②
 和Mg(OH)C1均为白色固体,不溶于水但能与稀盐酸,稀硫酸等反应生成盐和水。
和Mg(OH)C1均为白色固体,不溶于水但能与稀盐酸,稀硫酸等反应生成盐和水。【提出猜想】
猜想1:是没有参加反应的镁条
猜想2:是生成的
 过多而析出晶体
过多而析出晶体猜想3:是生成的
 白色沉淀
白色沉淀 猜想4:是生成的Mg(OH)Cl白色沉淀。
【实验探究二】
将上述【实验探究一】D试管反应后的物质过滤,并将得到的白色不溶物分成三份,分别放入三支试管中进行实验。
| 实验序号 | 实验操作 | 实验现象 | 实验结论 |
| 实验1 | 滴加适量稀盐酸 | 白色不溶物消失,无气体产生 | 猜想1不成立 |
| 实验2 | 加入适量蒸馏水,充分振荡 | 白色不溶物没有减少 | 猜想2 |
| 实验3 | ①滴入足量的稀硝酸 ②再向①中继续滴入足量的硝酸银溶液 | 白色不溶物一定含有氯元素,说明猜想3不成立,猜想4成立 |
①同学对上述实验3的结论提出质疑,他认为实验3设计不严密,要验证猜想4是否成立,在进行实验3之前应该进行的操作是
②老师的指导下,实验小组最终确定白色不溶物是Mg(OH)C1,请写出Mg(OH)C1与稀盐酸反应的化学方程式
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】氢氧化钠是常见的化工品之一,也是化学实验室里一种必备的化学试剂。
同学们在探究碱溶液与酚酞溶液作用的实验时,发现了一个意外现象:向氢氧化钠溶液中滴入酚酞溶液(如图),溶液变成了红色,但是一会儿红色就消失了。为此某化学小组的同学进行了如下探究。
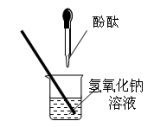
【提出猜想】猜想A:可能是氢氧化钠溶液与酚酞溶液混合后与空气中氧气反应,使红色消失。
猜想B:可能与氢氧化钠溶液的溶质质量分数有关。
【设计并进行实验】
实验一:
【解释、结论一】
(1)①氢氧化钠溶液的pH______ 7(填“大于”、“小于”或“等于”)
②配制2%的氢氧化钠溶液时,用煮沸过的蒸馏水目的是________ 。
③分析实验一,得出的结论是________ 。
实验二:
【解释、结论二】
(2)①实验二的目的是___________
② X的数值是_________
③如果你是化学老师,做氢氧化钠溶液中滴入酚酞试剂的演示实验,为了保证本节课堂内实验现象相对稳定,你应该选用溶质质量分数为________ 氢氧化钠溶液。
【拓展】实验室盛有氢氧化钠溶液的试剂瓶,使用后忘了盖上盖子,敞口放置了一段时间。小敏取少量该试剂瓶内溶液于试管中,加入足量的稀盐酸,发现产生气泡,她认为该氢氧化钠溶液已经全部变质。你认为小敏的结论是否合理,并说明理由_______ 。
同学们在探究碱溶液与酚酞溶液作用的实验时,发现了一个意外现象:向氢氧化钠溶液中滴入酚酞溶液(如图),溶液变成了红色,但是一会儿红色就消失了。为此某化学小组的同学进行了如下探究。

【提出猜想】猜想A:可能是氢氧化钠溶液与酚酞溶液混合后与空气中氧气反应,使红色消失。
猜想B:可能与氢氧化钠溶液的溶质质量分数有关。
【设计并进行实验】
实验一:
| 试管编号 | 1 | 2 |
| 配制NaOH溶液的蒸馏水 | 未煮沸的蒸馏水 | 煮沸的蒸馏水 |
| NaOH溶液溶质质量分数(%) | 2.0 | 2.0 |
| NaOH溶液体积(mL) | 5 | 5 |
| 酚酞试液(滴) | 5 | 5 |
| 有无液封 | 无植物油液封 | 有植物油液封 |
| 溶液变红色后红色褪去时间(min) | 8~9 | 8~9 |
(1)①氢氧化钠溶液的pH
②配制2%的氢氧化钠溶液时,用煮沸过的蒸馏水目的是
③分析实验一,得出的结论是
实验二:
| 试管编号 | 1 | 2 | 3 | 4 | 5 | 6 |
| NaOH溶液溶质质量分数(%) | 8.0 | 5.0 | 3.0 | 2.0 | 1.0 | 0.5 |
| NaOH溶液体积(mL) | 5 | 5 | X | 5 | 5 | 5 |
| 酚酞溶液(滴) | 5 | 5 | 5 | 5 | 5 | 5 |
| 溶液变红色后红色褪去时间(min) | 0.4 | 2.0 | 5~6 | 8~9 | 12min后慢慢褪色,到30min,后变成无色 | 45min后慢慢褪色,直至2h后仍能看到淡红色 |
(2)①实验二的目的是
② X的数值是
③如果你是化学老师,做氢氧化钠溶液中滴入酚酞试剂的演示实验,为了保证本节课堂内实验现象相对稳定,你应该选用溶质质量分数为
【拓展】实验室盛有氢氧化钠溶液的试剂瓶,使用后忘了盖上盖子,敞口放置了一段时间。小敏取少量该试剂瓶内溶液于试管中,加入足量的稀盐酸,发现产生气泡,她认为该氢氧化钠溶液已经全部变质。你认为小敏的结论是否合理,并说明理由
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】铁暴露在空气中会生锈、不知你注意了没有,将苹果切开不久,果肉上就会产生一层咖啡色的物质,也好像是生了“锈”一样、某化学活动小组对此进行了探究
【提出问题】切开的苹果“生锈”与什么因素有关?
【猜想与假设】
猜想①:可能与空气没有关系,只是果肉内的物质自身相互反应而“生锈”
猜想②:可能是果肉中的物质与空气中的氧气作用而“生锈”
猜想③:可能是果肉中的物质与空气中的氮气作用而“生锈”
猜想④:可能是果肉中的物质与空气中的二氧化碳作用而“生锈”
猜想⑤:可能是果肉中的物质与空气中的氧气作用而“生锈”,并且苹果“生锈”的速度还可能与温度有关
【收集证据】
(一)查阅有关资料:已知苹果“生锈”是果肉里的物质(酚和酶)与空气中的二种物质发生反应,生成咖啡色的物质.
(二)实验探究:针对上面的猜想①至猜想⑤,化学活动小组依次设计了实验方案,进行了实验验证,并依次
观察到下列实验现象、请你将他们设计的可行的实验探究方案,填写在下表中:
【得出结论】___________________________________________
【反思与评价】
(1)在②一⑤四种猜想中,你认为猜想_________ (填代号)最不合理,理由是___________ 。
(2)在验证猜想①时,同学们发现,如果水不与空气隔绝,果肉放在水中时间长了也会变色,其可能的原因是_________ 。
【应用】根据上述结论,要防止果汁变质,果品加工厂加工和保存果汁时可采取的措施_______ 。
【提出问题】切开的苹果“生锈”与什么因素有关?
【猜想与假设】
猜想①:可能与空气没有关系,只是果肉内的物质自身相互反应而“生锈”
猜想②:可能是果肉中的物质与空气中的氧气作用而“生锈”
猜想③:可能是果肉中的物质与空气中的氮气作用而“生锈”
猜想④:可能是果肉中的物质与空气中的二氧化碳作用而“生锈”
猜想⑤:可能是果肉中的物质与空气中的氧气作用而“生锈”,并且苹果“生锈”的速度还可能与温度有关
【收集证据】
(一)查阅有关资料:已知苹果“生锈”是果肉里的物质(酚和酶)与空气中的二种物质发生反应,生成咖啡色的物质.
(二)实验探究:针对上面的猜想①至猜想⑤,化学活动小组依次设计了实验方案,进行了实验验证,并依次
观察到下列实验现象、请你将他们设计的可行的实验探究方案,填写在下表中:
| 猜想 | 可行的实验方案 | 观察到的实验现象 |
| 猜想① | 将一小块果肉浸入盛有蒸馏水的烧杯中,观察现象 | 果肉表面不变色 |
| 猜想② | 将一小块苹果果肉放入盛有氧气的集气瓶中,观察现象 | 果肉表面变色 |
| 猜想③ | 将一小块苹果果肉放入盛有氮气的集气瓶中,观察现象 | 果肉表面不变色 |
| 猜想④ | 将一小块苹果果肉放入盛有二氧化碳的集气瓶中,观察现象 | 果肉表面不变色 |
| 猜想⑤ | 温度高的先变色 |
【得出结论】
【反思与评价】
(1)在②一⑤四种猜想中,你认为猜想
(2)在验证猜想①时,同学们发现,如果水不与空气隔绝,果肉放在水中时间长了也会变色,其可能的原因是
【应用】根据上述结论,要防止果汁变质,果品加工厂加工和保存果汁时可采取的措施
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】淀粉是一种天然高分子化合物,在硫酸的催化下能够发生水解,产生葡萄糖等小分子化合物。某小组同学为研究影响淀粉水解效果的因素进行了如下探究:
【提出问题】影响淀粉水解效果的因素有哪些?
【作出猜想】影响淀粉水解效果的因素有硫酸浓度、硫酸体积、温度等。
【查阅资料】淀粉与碘液(主要成分为I2)在酸碱性不同的溶液中会显示不同的颜色:
pH≤2时,呈现蓝紫色;3≤pH≤8时,呈蓝色;pH≥9时,不显蓝色。
【进行实验】取A、B、C、D 4支试管,每支试管中分别加入0.3g干淀粉、和不同浓度和体积的硫酸溶液,水浴加热5min后取出四支试管冷却,用NaOH溶液调节pH在3至8范围内,分别向试管中滴加1滴碘液,观察现象。
【实验记录】
【解释与结论】
(1)当溶液pH≥9时,I2会与NaOH反应,从而不能与淀粉结合呈现出蓝色。补全该反应的化学方程式:I2+2NaOH=NaI+NaIO+______ 。
(2)试管B作为对照实验,a为______ %。
(3)设计实验A和B的目的是______ 。
(4)对比实验B和C可得出的结论是_______ 。
(5)探究H2SO4体积对淀粉水解效果影响的实验是________ 。
【反思与交流】
(6)影响该反应效果的因素除温度、H2SO4浓度和体积外,还可能有_______ 。
【提出问题】影响淀粉水解效果的因素有哪些?
【作出猜想】影响淀粉水解效果的因素有硫酸浓度、硫酸体积、温度等。
【查阅资料】淀粉与碘液(主要成分为I2)在酸碱性不同的溶液中会显示不同的颜色:
pH≤2时,呈现蓝紫色;3≤pH≤8时,呈蓝色;pH≥9时,不显蓝色。
【进行实验】取A、B、C、D 4支试管,每支试管中分别加入0.3g干淀粉、和不同浓度和体积的硫酸溶液,水浴加热5min后取出四支试管冷却,用NaOH溶液调节pH在3至8范围内,分别向试管中滴加1滴碘液,观察现象。
【实验记录】
| 序号 | H2SO4浓度/% | H2SO4体积/mL | 水浴温度/℃ | 实验现象 |
| A | 40 | 4 | 90 | 不变蓝 |
| B | a | 4 | 80 | 变蓝 |
| C | 50 | 4 | 80 | 不变蓝 |
| D | 40 | 6 | 80 | 不变蓝 |
【解释与结论】
(1)当溶液pH≥9时,I2会与NaOH反应,从而不能与淀粉结合呈现出蓝色。补全该反应的化学方程式:I2+2NaOH=NaI+NaIO+
(2)试管B作为对照实验,a为
(3)设计实验A和B的目的是
(4)对比实验B和C可得出的结论是
(5)探究H2SO4体积对淀粉水解效果影响的实验是
【反思与交流】
(6)影响该反应效果的因素除温度、H2SO4浓度和体积外,还可能有
您最近一年使用:0次



