今后学习常见物质时会从“价”和“类”两个方面进行学习。下图表示铁元素的常见化合价与含铁物质类别的关系。

(1)X的物质类别是_____________ 。
(2)铁和稀硫酸反应生成的含铁化合物属于上图中的___________ (填序号)。
(3)某同学想用物质a制取物质b,设计了以下实验步骤
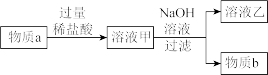
①物质a与稀盐酸反应的化学反应方程式为____________________________ 。
②溶液乙中的溶质一定有____________________________ 。
③如果向盛有溶液甲的烧杯中滴加NaOH溶液至过量,下列图像能正确表示烧杯中溶液质量变化的是__________ (填序号)。


(1)X的物质类别是
(2)铁和稀硫酸反应生成的含铁化合物属于上图中的
(3)某同学想用物质a制取物质b,设计了以下实验步骤
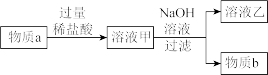
①物质a与稀盐酸反应的化学反应方程式为
②溶液乙中的溶质一定有
③如果向盛有溶液甲的烧杯中滴加NaOH溶液至过量,下列图像能正确表示烧杯中溶液质量变化的是

2020·重庆·中考真题 查看更多[3]
更新时间:2020-07-14 12:28:12
|
相似题推荐
【推荐1】为探究某塑料的组成元素,设计了实验I和Ⅱ根据图1和图2回答下列问题∶


(1)若用一种暗紫色固体制取O2,发生反应的化学方程式为_______ 。发生装置应选用上述装置A。
(2)欲制取干燥的O2,装置合理的连接顺序为∶ 发生装置→C→_______ (填标号)连接装置时,发生装置的出气口应与装置C中_______ (填"a"或"b")端相连。
Ⅱ.组成探究(1)定性检测(已知∶无水CuSO4遇水变蓝色)
③由上述实验可知,该塑料一定含有的元素是_______ (填元素符号)
(3)定量测定
①为进一步确定组成,将1.4g该塑料在足量O2中完全燃烧,共产生了4.4gCO2和1.8gH2O,依据质量守恒定律,可判断该塑料_______ 除上述③中结论之外的元素。
②写出L装置中瓶内发生的化学反应方程式∶_______ 。


(1)若用一种暗紫色固体制取O2,发生反应的化学方程式为
(2)欲制取干燥的O2,装置合理的连接顺序为∶ 发生装置→C→
Ⅱ.组成探究(1)定性检测(已知∶无水CuSO4遇水变蓝色)
| 实验操作 | 实验现象 | 结论 |
| 连接装置,检查气密性,装入试剂并按如图进行实验。通入O2,一段时间后,点燃J处酒精灯 | 装置K中无水CuSO4变 | 塑料燃烧产物中有H2O |
| 装置L中 | 塑料燃烧产物中有CO2 |
(3)定量测定
①为进一步确定组成,将1.4g该塑料在足量O2中完全燃烧,共产生了4.4gCO2和1.8gH2O,依据质量守恒定律,可判断该塑料
②写出L装置中瓶内发生的化学反应方程式∶
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组同学用下列仪器和装置制取乙烯(C2H4),并用过量的氧气将C2H4氧化成CO2和H2O,从而测定乙烯中碳、氢两种元素的质量比,如图所示,请回答下列问题。(据资料:有机物可能伴随少量不完全燃烧生成一种有毒气体;无水氯化钙是一种常见的吸水的干燥剂;NaOH固体可吸收二氧化碳气体。)
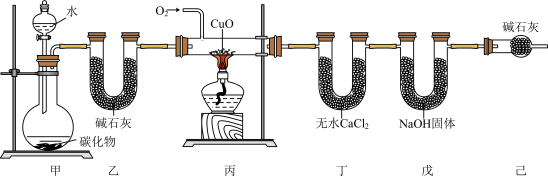
(1)实验室制备乙炔的化学方程式是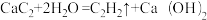 ;该小组同学受实验制备C2H2的启发,拟用Mg2C2与水反应来制备乙烯,写出该反应的化学方程式
;该小组同学受实验制备C2H2的启发,拟用Mg2C2与水反应来制备乙烯,写出该反应的化学方程式______ 。
(2)装置巳的作用是______ ;
(3)实验前称得丁、戊两装置的质量分别为m1g和n1g,实验完毕,称得丁、戊两装置的质量分别变为m2g和n2g,则测定乙烯中碳、氢两种元素的质量比为______ (列出算式)。
(4)若不接乙装置,则测定结果______ (填“偏高”、“偏低”或“不变”)。

(1)实验室制备乙炔的化学方程式是
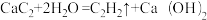 ;该小组同学受实验制备C2H2的启发,拟用Mg2C2与水反应来制备乙烯,写出该反应的化学方程式
;该小组同学受实验制备C2H2的启发,拟用Mg2C2与水反应来制备乙烯,写出该反应的化学方程式(2)装置巳的作用是
(3)实验前称得丁、戊两装置的质量分别为m1g和n1g,实验完毕,称得丁、戊两装置的质量分别变为m2g和n2g,则测定乙烯中碳、氢两种元素的质量比为
(4)若不接乙装置,则测定结果
您最近一年使用:0次
【推荐3】下图所示为实验室中常见气体制备、干燥、收集和进行实验探究的部分装置(组装实验装置时,可重复选择装置),某化学小组的同学利用其进行下列化学实验。______ 。
(2)以石灰石和未知浓度的盐酸为原料,在实验室中制备并收集干燥、纯净的二氧化碳气体,按照要求设计实验装置,连接装置。(提示:盐酸中挥发出的少量HCl气体可用饱和碳酸氢钠溶液吸收)
①所选装置的连接顺序为______ (从左到右填写装置序号字母)。
②上述制二氧化碳的化学方程式为______ 。
③为探究石灰石和稀盐酸反应后的剩余废液中盐酸是否有剩余,该实验小组同学想用pH试纸测定反应后剩余溶液的酸碱度,测定的具体方法是______ 。
(3)该实验小组同学以过氧化氢溶液为原料(MnO2为催化剂)制备氧气,并对E中塑料的组成进行分析探究(资料显示该塑料中含碳、氢、氧三种元素),所选装置按“A→B1→E→B2→C→碱石灰干燥管”的顺序连接,实验前检验装置气密性。该塑料碎屑在纯氧气中充分燃烧,观察现象,收集有关实验数据(假设发生的化学反应都充分反应),试回答下列问题:
①该实验中,装置C的作用是______ 。
②塑料碎屑充分燃烧后,测得装置B2质量增加3.6g,测得装置C质量增加8.8g,则该塑料碎屑分子中C、H两种元素的质量比为______ (填最简整数比)。

(2)以石灰石和未知浓度的盐酸为原料,在实验室中制备并收集干燥、纯净的二氧化碳气体,按照要求设计实验装置,连接装置。(提示:盐酸中挥发出的少量HCl气体可用饱和碳酸氢钠溶液吸收)
①所选装置的连接顺序为
②上述制二氧化碳的化学方程式为
③为探究石灰石和稀盐酸反应后的剩余废液中盐酸是否有剩余,该实验小组同学想用pH试纸测定反应后剩余溶液的酸碱度,测定的具体方法是
(3)该实验小组同学以过氧化氢溶液为原料(MnO2为催化剂)制备氧气,并对E中塑料的组成进行分析探究(资料显示该塑料中含碳、氢、氧三种元素),所选装置按“A→B1→E→B2→C→碱石灰干燥管”的顺序连接,实验前检验装置气密性。该塑料碎屑在纯氧气中充分燃烧,观察现象,收集有关实验数据(假设发生的化学反应都充分反应),试回答下列问题:
①该实验中,装置C的作用是
②塑料碎屑充分燃烧后,测得装置B2质量增加3.6g,测得装置C质量增加8.8g,则该塑料碎屑分子中C、H两种元素的质量比为
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】化学是一门以实验为基础的科学,请结合图表信息回答问题:

Ⅰ.写出图中①②仪器的名称:①__________________ ,②__________________ 。
Ⅱ.实验室用氯酸钾和二氧化锰的固体混合物制取氧气,反应的化学方程式为_____________ ,加热时试管口应略向下倾斜的原因是_______________ 。
Ⅲ.①为研究实验室制取二氧化碳的适宜条件(温度、浓度、固体的颗粒大小等因素会影响化学反应的快慢),进行了如下四组实验:
大理石与盐酸反应的化学方程式是__________________________ ;实验甲与_________ 对照(填编号),是为了研究固体反应物颗粒大小对反应快慢的影响;上述实验中,另一个影响反应快慢的因素是________________________ 。
实验室制取二氧化碳气体,可随时控制反应发生或停止的装置为_______ (填序号),若
用E装置收集该气体,气体应从_____ (填“a”或“b”)端通入。若在收集得到二氧化碳的集气瓶中滴加紫色石蕊试液,稍作振荡,试液颜色变为______ 色,变色的原因是____________ 。
Ⅳ.甲烷是一种无色气体,密度比空气小,难溶于水的气体。实验室用无水醋酸钠(固体)与碱石灰(固体)混合加热制得,则可选择的发生装置为___________ (填序号),选择装置D收集甲烷气体的理由是__________ 。

Ⅰ.写出图中①②仪器的名称:①
Ⅱ.实验室用氯酸钾和二氧化锰的固体混合物制取氧气,反应的化学方程式为
Ⅲ.①为研究实验室制取二氧化碳的适宜条件(温度、浓度、固体的颗粒大小等因素会影响化学反应的快慢),进行了如下四组实验:
| 实验编号 药品 | 甲 | 乙 | 丙 | 丁 |
| m g大理石 | 块状 | 块状 | 粉末状 | 粉末状 |
| n g盐酸(过量) | 稀盐酸 | 浓盐酸 | 稀盐酸 | 浓盐酸 |
实验室制取二氧化碳气体,可随时控制反应发生或停止的装置为
用E装置收集该气体,气体应从
Ⅳ.甲烷是一种无色气体,密度比空气小,难溶于水的气体。实验室用无水醋酸钠(固体)与碱石灰(固体)混合加热制得,则可选择的发生装置为
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】实验课上,同学们利用下列装置进行气体制备的学习。请回答下列问题:

(1)用装置A制取O2的化学方程式为__________ ;
(2)装置B或C均可用于实验室制取氢气,与装置B相比,装置C的优点是__________ ;
(3)实验室用装置D、E或F收集气体,收集O2和CO2都能用的装置是______ 。(填序号)

(1)用装置A制取O2的化学方程式为
(2)装置B或C均可用于实验室制取氢气,与装置B相比,装置C的优点是
(3)实验室用装置D、E或F收集气体,收集O2和CO2都能用的装置是
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】请根据如图实验装置,回答问题。

(1)写出仪器a的名称:_______ 。
(2)用加热高锰酸钾的方法制取氧气,选择的发生装置是_______ (填字母),该反应的化学方程式为_______ 。能用C装置收集氧气是因为氧气_______ 且不与水反应的性质,若收集的氧气不纯,原因可能是_______ (写出一点即可)。
(3)若使用B装置制取气体,装药液时需要注意_______ 。
(4)结合A-E装置图,归纳实验室制取氧气和二氧化碳的共同点_______ (填字母)。
a.都需要加热 b.都需要用催化剂
c.都能用B作发生装置 d.生成物都只有一种

(1)写出仪器a的名称:
(2)用加热高锰酸钾的方法制取氧气,选择的发生装置是
(3)若使用B装置制取气体,装药液时需要注意
(4)结合A-E装置图,归纳实验室制取氧气和二氧化碳的共同点
a.都需要加热 b.都需要用催化剂
c.都能用B作发生装置 d.生成物都只有一种
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐1】已知:①Cu+2H2SO4(浓) CuSO4+2H2O+SO2↑;②二氧化硫的化学性质与二氧化碳很相似。为探究铜与浓硫酸的反应及二氧化硫气体的部分性质,某兴趣小组设计了如图所示实验(注:a.图中脱脂棉团蘸有紫色石蕊试液;b.可以上下移动的粗铜丝能控制反应物间是否接触,从而控制反应的发生和停止)。
CuSO4+2H2O+SO2↑;②二氧化硫的化学性质与二氧化碳很相似。为探究铜与浓硫酸的反应及二氧化硫气体的部分性质,某兴趣小组设计了如图所示实验(注:a.图中脱脂棉团蘸有紫色石蕊试液;b.可以上下移动的粗铜丝能控制反应物间是否接触,从而控制反应的发生和停止)。

(1)铜丝绕成螺旋状的目的是_____ ,
(2)鼓气球鼓入空气的作用是_____ ,
(3)已知①的反应中,反应后化合价升高的元素是_____ ;
(4)实验中可观察到脱脂棉团_____ ;
(5)氢氧化钠溶液的作用是_____ ,其反应原理为 _____ 。
 CuSO4+2H2O+SO2↑;②二氧化硫的化学性质与二氧化碳很相似。为探究铜与浓硫酸的反应及二氧化硫气体的部分性质,某兴趣小组设计了如图所示实验(注:a.图中脱脂棉团蘸有紫色石蕊试液;b.可以上下移动的粗铜丝能控制反应物间是否接触,从而控制反应的发生和停止)。
CuSO4+2H2O+SO2↑;②二氧化硫的化学性质与二氧化碳很相似。为探究铜与浓硫酸的反应及二氧化硫气体的部分性质,某兴趣小组设计了如图所示实验(注:a.图中脱脂棉团蘸有紫色石蕊试液;b.可以上下移动的粗铜丝能控制反应物间是否接触,从而控制反应的发生和停止)。
(1)铜丝绕成螺旋状的目的是
(2)鼓气球鼓入空气的作用是
(3)已知①的反应中,反应后化合价升高的元素是
(4)实验中可观察到脱脂棉团
(5)氢氧化钠溶液的作用是
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐2】在一节化学课上,老师为大家演示了如图所示的趣味实验 “魔棒生烟”,用两根玻璃棒分别在浓氨水和浓盐酸中蘸一下,然后将这两根玻璃棒靠近(不要接触,如图),可观察到产生大量白烟。
“魔棒生烟”,用两根玻璃棒分别在浓氨水和浓盐酸中蘸一下,然后将这两根玻璃棒靠近(不要接触,如图),可观察到产生大量白烟。
为了揭秘魔术,化学兴趣小组的同学查阅了大量资料发现:
【查询资料】①浓盐酸会挥发氯化氢(HCl)气体,浓氨水会挥发出氨气(NH3),两种气体反应生成白色固体氯化铵(NH4Cl)
②气体的相对分子质量越小,分子运动速率快
然后化学兴趣小组的同学进一步设计了如图2所示的实验,试回答以下问题:

(1)图1中“魔棒生烟”魔术中,两根玻璃棒无需接触,就可看见白烟产生,说明分子具有的性质是:______ 。
(2)“魔棒生烟”涉及的反应符号表达式:______ ,关于该反应中各元素的化合价说法正确的是______ (填字母)
A所有元素的化合价都不变
B有一种元素的化合价改变
C有两种元素的化合价改变
D所有元素化合价都发生了改变
(3)图2同时打开开关a、b,玻璃管c中出现白烟,白烟最浓的地方是:______ (选填”e”f”或g),理由是:______ 。
(4)看到产生白烟后,立即关闭开关a、b,并向烧瓶B中滴加5-6滴无色酚酞溶液,可观察到的现象是:______ ,图2相比图1实验的优点是:______ 。
 “魔棒生烟”,用两根玻璃棒分别在浓氨水和浓盐酸中蘸一下,然后将这两根玻璃棒靠近(不要接触,如图),可观察到产生大量白烟。
“魔棒生烟”,用两根玻璃棒分别在浓氨水和浓盐酸中蘸一下,然后将这两根玻璃棒靠近(不要接触,如图),可观察到产生大量白烟。为了揭秘魔术,化学兴趣小组的同学查阅了大量资料发现:
【查询资料】①浓盐酸会挥发氯化氢(HCl)气体,浓氨水会挥发出氨气(NH3),两种气体反应生成白色固体氯化铵(NH4Cl)
②气体的相对分子质量越小,分子运动速率快
然后化学兴趣小组的同学进一步设计了如图2所示的实验,试回答以下问题:

(1)图1中“魔棒生烟”魔术中,两根玻璃棒无需接触,就可看见白烟产生,说明分子具有的性质是:
(2)“魔棒生烟”涉及的反应符号表达式:
A所有元素的化合价都不变
B有一种元素的化合价改变
C有两种元素的化合价改变
D所有元素化合价都发生了改变
(3)图2同时打开开关a、b,玻璃管c中出现白烟,白烟最浓的地方是:
(4)看到产生白烟后,立即关闭开关a、b,并向烧瓶B中滴加5-6滴无色酚酞溶液,可观察到的现象是:
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】结合如图实验常用装置(铁架台、夹持和连接装置略),回答有关问题:

(1)实验室将一定量氯酸钾和二氧化锰混合制取氧气的化学方程式为______ ,下列图象能正确表示对应变化关系的是_______ 。
A B
B C
C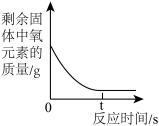 D
D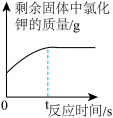
(2)若用I装置收集并测量氧气的体积,应在______ (填“m”或“n”)处连接量筒。
(3)氯气是一种黄绿色、有剧烈刺激性气味的有毒气体,密度比空气大,能溶于水,并与水反应生成盐酸和次氯酸。实验室制备氯气通常用浓盐酸与二氧化锰反应制得: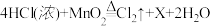 。
。
①组装制取氯气的发生装置所需的玻璃仪器是______ (填编号,下同),干燥氯气可用装置______ 。
②上述反应中X的化学式为______ ,该反应中化合价发生改变的元素为______ (填元素符号)

(1)实验室将一定量氯酸钾和二氧化锰混合制取氧气的化学方程式为
A
 B
B C
C D
D
(2)若用I装置收集并测量氧气的体积,应在
(3)氯气是一种黄绿色、有剧烈刺激性气味的有毒气体,密度比空气大,能溶于水,并与水反应生成盐酸和次氯酸。实验室制备氯气通常用浓盐酸与二氧化锰反应制得:
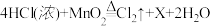 。
。①组装制取氯气的发生装置所需的玻璃仪器是
②上述反应中X的化学式为
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
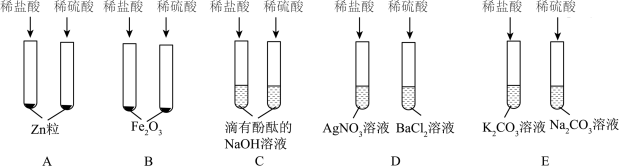
【推荐1】电动自行车常用的蓄铅电池中的电解液一般为稀硫酸,利用稀硫酸进行以下实验:

(1)写出图A实验中发生的化学方程式_____ 。
(2)图B实验中有_____ 现象,其反应的化学方程式为_____ 。
(3)由图A、C实验可知,稀硫酸能与_____ 、_____ (填物质类别)反应。
(4)稀硫酸和稀盐酸具有相似的化学性质,这是因为它们在组成上都有_____ ,鉴别两种酸可以选用的化学试剂是_____ 。

(1)写出图A实验中发生的化学方程式
(2)图B实验中有
(3)由图A、C实验可知,稀硫酸能与
(4)稀硫酸和稀盐酸具有相似的化学性质,这是因为它们在组成上都有
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐2】小明为探究酸、碱、盐的化学性质,做了如下实验:

(1)实验后液体颜色变红的是_____ ,变为黄色的是_____ (填试管编号)。
(2)反应后试管C溶液中一定有的阳离子是_____ (写离子符号)。
(3)小明把试管D、E反应后的液体倒入一个洁净的烧杯中,观察到只有白色沉淀生成,过滤后得到白色沉淀和无色滤液,小明分别对试管D、E反应时的反应物用量有如下描述,正确的是_____
A 试管D:氢氧化钙溶液一定过量 B 试管D:稀盐酸一定不足
C 试管E:碳酸钠溶液一定过量 D 试管E:稀盐酸一定不足

(1)实验后液体颜色变红的是
(2)反应后试管C溶液中一定有的阳离子是
(3)小明把试管D、E反应后的液体倒入一个洁净的烧杯中,观察到只有白色沉淀生成,过滤后得到白色沉淀和无色滤液,小明分别对试管D、E反应时的反应物用量有如下描述,正确的是
A 试管D:氢氧化钙溶液一定过量 B 试管D:稀盐酸一定不足
C 试管E:碳酸钠溶液一定过量 D 试管E:稀盐酸一定不足
您最近一年使用:0次