水是生命之源,也是日常生活、工农业生产必不可少的。
(1)清澈的温泉水是________ (填“纯净物”或“混合物”)。
(2)净化温泉水的过程中,活性炭的主要作用是________________ 。
(3)鉴别生活用水是硬水还是软水,方法是取样滴加等质量的肥皂水,有大量泡沫产生的为________________ 。
(4)如图是硝酸钾和氯化钠在水中的溶解度曲线。

①两种物质中,溶解度受温度影响较小的是______________ 。
②使接近饱和的氯化钠溶液变为饱和溶液的一种方法是______________ 。
③60℃时,硝酸钾饱和溶液中溶质、溶剂的质量比是______________ 。
④60℃时,硝酸钾饱和溶液中溶有少量的氯化钠,提纯硝酸钾应采用的方法是______________ 。
(1)清澈的温泉水是
(2)净化温泉水的过程中,活性炭的主要作用是
(3)鉴别生活用水是硬水还是软水,方法是取样滴加等质量的肥皂水,有大量泡沫产生的为
(4)如图是硝酸钾和氯化钠在水中的溶解度曲线。

①两种物质中,溶解度受温度影响较小的是
②使接近饱和的氯化钠溶液变为饱和溶液的一种方法是
③60℃时,硝酸钾饱和溶液中溶质、溶剂的质量比是
④60℃时,硝酸钾饱和溶液中溶有少量的氯化钠,提纯硝酸钾应采用的方法是
2016·天津·一模 查看更多[1]
更新时间:2020-04-23 18:07:06
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】2017年3月22日是第25届世界水日,宣传主题是“Wastewater”(废水),请回答下列与水有关的问题:
(1)废水中常含有难溶性杂质,除去这些杂质的操作是___________ (填“过滤”、“吸附”或“蒸馏”),实验完成该操作所需的玻璃仪器除玻璃棒外还有___________ (填序号),其中玻璃棒的作用是___________ 。
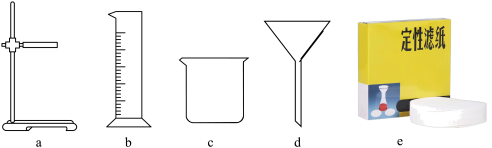
(2)除去难溶性杂质后,可利用活性炭___________ (填“过滤 ”、“吸附 ”或“蒸馏 ”)废水中的异味和色素,污水经物理、化学或生化方法进行分级处理后得到中水,中水不可饮用,请列举中水的一项用途:___________ 。
(3)硬水给生活和生产带来很多麻烦,生活中可用________ 来区分硬水和软水,生活中常用_________ 的方法来降低水的硬度;
(4)以下是有关爱护水资源的一些具体做法:属于防治水体污染措施的是________(填字母)
(1)废水中常含有难溶性杂质,除去这些杂质的操作是

(2)除去难溶性杂质后,可利用活性炭
(3)硬水给生活和生产带来很多麻烦,生活中可用
(4)以下是有关爱护水资源的一些具体做法:属于防治水体污染措施的是________(填字母)
| A.洗手洗脸时随时关闭水龙头 |
| B.工业上应用新技术、新工艺减少污染物的产生 |
| C.农业上合理使用化肥和农药 |
| D.用淘米水浇花 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】水是生命之源,是“永远值得探究的物质”,人类从未停止过对水的研究和保护。

(1)2023年8月24日,日本将福岛核污水排入大海,激起全世界人民的抗议和谴责。核污水中有H-3等难以去除的放射性原子,3是相对原子质量,该原子的中子数为_____ 。
(2)水的电解实验如图1所示,反应的符号表达式为_____ ,其中分析正确的是_____ 。
A.生成2mL氧气
B.产生1mL气体的为电源负极
C.该实验可证明水是由氢元素和氧元素组成
(3)目前许多学校安装了直饮水机,其主要工作流程如图2.其中①中炭罐的作用是_____ 。要检验所得的直饮水是硬水还是软水,可向其中加入适量的_____ 。

(1)2023年8月24日,日本将福岛核污水排入大海,激起全世界人民的抗议和谴责。核污水中有H-3等难以去除的放射性原子,3是相对原子质量,该原子的中子数为
(2)水的电解实验如图1所示,反应的符号表达式为
A.生成2mL氧气
B.产生1mL气体的为电源负极
C.该实验可证明水是由氢元素和氧元素组成
(3)目前许多学校安装了直饮水机,其主要工作流程如图2.其中①中炭罐的作用是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】水是生活中最常见的物质之一,也是实验室常用的试剂。
(1)长期饮用硬水会影响人体健康,检验自来水是否为硬水常用的物质是______ 。
(2)某工厂用电解水的方法制取氧气,发现氧气的产量略小于理论值,且所得氧气中有淡淡的鱼腥气味(每个具有鱼腥气味的气体分子由三个原子构成)。从元素守恒角度分析,该鱼腥气味的气体是______ (填化学式)。
(3)硫酸钠溶于水能离解出自由移动的______ 、______ (填符号),因此硫酸钠溶液能导电。
(4)电解水时,在水中加入少量硫酸钠可增强导电性。某兴趣小组把4.0g硫酸钠固体加入86.8g水中,充分溶解后进行电解。一段时间后停止通电,在试管A中收集到1.2g气体(装置如图)。回答下列问题:
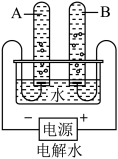
①B管中收集到的气体是______ ,其质量是______ g。
②电解后溶液中硫酸钠的质量分数为______ 。
(1)长期饮用硬水会影响人体健康,检验自来水是否为硬水常用的物质是
(2)某工厂用电解水的方法制取氧气,发现氧气的产量略小于理论值,且所得氧气中有淡淡的鱼腥气味(每个具有鱼腥气味的气体分子由三个原子构成)。从元素守恒角度分析,该鱼腥气味的气体是
(3)硫酸钠溶于水能离解出自由移动的
(4)电解水时,在水中加入少量硫酸钠可增强导电性。某兴趣小组把4.0g硫酸钠固体加入86.8g水中,充分溶解后进行电解。一段时间后停止通电,在试管A中收集到1.2g气体(装置如图)。回答下列问题:

①B管中收集到的气体是
②电解后溶液中硫酸钠的质量分数为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】化学源于生活,也服务于生活。

(1)水是生命之源。净化水的主要操作步骤:加入明矾---沉淀----过滤------吸附----杀菌消毒等。净化水时加入明矾的作用是:___________ 。然后进行过滤,请指出如图所示操作中的一处明显错误___________ .若过滤所得滤液仍然浑浊,写出两点原因_____________ ,
(2)经过以上操作后,所得到的水并不是纯水,若想进一步得到纯水,还需进行的操作是___________ 。硬水和软水可以用__________ 区别,生活中常用________ 方法降低水的硬度。
(3)生活离不开水,我们还可以从组成、结构等角度认识水。

①组成:如图所示电解水的实验中,试管a、b中产生气体的体积为_______ ,该实验证明水是由_______ 组成的。
②结构:每个水分子是由______ 构成。
③请写出电解水的文字表达式:________
④在电解水实验中加入少量稀硫酸的作用是________

(1)水是生命之源。净化水的主要操作步骤:加入明矾---沉淀----过滤------吸附----杀菌消毒等。净化水时加入明矾的作用是:
(2)经过以上操作后,所得到的水并不是纯水,若想进一步得到纯水,还需进行的操作是
(3)生活离不开水,我们还可以从组成、结构等角度认识水。

①组成:如图所示电解水的实验中,试管a、b中产生气体的体积为
②结构:每个水分子是由
③请写出电解水的文字表达式:
④在电解水实验中加入少量稀硫酸的作用是
您最近一年使用:0次
【推荐3】水是重要的自然资源。合理开发利用水资源,推进社会发展与进步。
(1)自然界中的水含有较多杂质,净化过程中加入活性炭,是利用其_____ 性。
(2)天然水具有一定的硬度,日常区分硬水和软水可选用的物质是_____ 。
(3)请举一例生活中节约用水的具体措施_____ 。
(4)水作为原料,可获得多种产品。
①工业上常用水制取水煤气,原理为: ,该反应过程中,还原剂是
,该反应过程中,还原剂是_____ ;
②利用CO和H2制取二甲醚的微观过程如图所示:

该变化过程中,X分子的化学式为_____ ,参加反应的CO和H2的分子个数比是_____ 。
(1)自然界中的水含有较多杂质,净化过程中加入活性炭,是利用其
(2)天然水具有一定的硬度,日常区分硬水和软水可选用的物质是
(3)请举一例生活中节约用水的具体措施
(4)水作为原料,可获得多种产品。
①工业上常用水制取水煤气,原理为:
 ,该反应过程中,还原剂是
,该反应过程中,还原剂是②利用CO和H2制取二甲醚的微观过程如图所示:

该变化过程中,X分子的化学式为
您最近一年使用:0次
【推荐1】溶液在生产生活中都有重要的应用。
(1)在市场上有一种叫做“摇摇冰”的即冷即饮型饮料。所谓“摇摇冰”是指吸食前将饮料罐隔离层中的制冷物质和水混合摇动一段时间后,就能使罐中饮料冷却。请根据所学知识猜测该制冷物质可能是 。
(2)如图一是甲、乙、丙三种固体物质的溶解度曲线。能同时使甲、乙、丙三种物质的饱和溶液变为不饱和溶液的方法是_________ 。
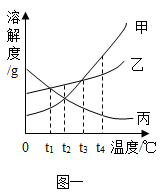
(3)将等质量的乙、丙两种物质分别加水配成t1℃时的饱和溶液,所得溶液的质量乙_________ 丙(选填“>”、“=”或“<”)。
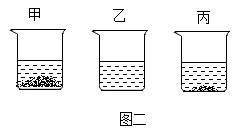
(4)20℃时,把等质量的甲、乙、丙三种固体分别加入到盛有50g水的烧杯中充分溶解后,观察到现象如图二。分析可知,20℃所处的温度范围是 (填字母序号)。
(5)将等质量甲、丙的饱和溶液从t4℃降温到t2℃,对于所得溶液下列叙述正确的是 。
(1)在市场上有一种叫做“摇摇冰”的即冷即饮型饮料。所谓“摇摇冰”是指吸食前将饮料罐隔离层中的制冷物质和水混合摇动一段时间后,就能使罐中饮料冷却。请根据所学知识猜测该制冷物质可能是 。
| A.氢氧化钠固体 | B.硝酸铵固体 | C.氯化钠固体 | D.蔗糖固体 |

(3)将等质量的乙、丙两种物质分别加水配成t1℃时的饱和溶液,所得溶液的质量乙
(4)20℃时,把等质量的甲、乙、丙三种固体分别加入到盛有50g水的烧杯中充分溶解后,观察到现象如图二。分析可知,20℃所处的温度范围是 (填字母序号)。

| A.0<20<t1 | B.t1<20<t2 | C.t2<20<t3 | D.t3<20<t4 |
| A.甲、丙都是饱和溶液 | B.溶液的质量甲>丙 |
| C.溶剂的质量甲<丙 | D.溶质的质量分数甲=丙 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:

(1)在t1℃时,甲、乙、丙三种物质的溶解度由小到大的顺序为_______ 。
(2)在t3℃时,等质量的甲、乙、丙三种物质的饱和溶液中,溶剂质量最小的是______ 。
(3)降温结晶过程中,甲、乙两物质的溶解度都________ (填“增大”、“减小”或“不变”)。
(4)若将接近饱和的丙溶液在保持溶质的质量不变的情况下变成饱和溶液的方法是________ 。
(5)在t1℃时,将三种物质饱和溶液升温至t2℃时溶质的质量分数由大到小顺序是________ 。

(1)在t1℃时,甲、乙、丙三种物质的溶解度由小到大的顺序为
(2)在t3℃时,等质量的甲、乙、丙三种物质的饱和溶液中,溶剂质量最小的是
(3)降温结晶过程中,甲、乙两物质的溶解度都
(4)若将接近饱和的丙溶液在保持溶质的质量不变的情况下变成饱和溶液的方法是
(5)在t1℃时,将三种物质饱和溶液升温至t2℃时溶质的质量分数由大到小顺序是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】如图是甲、乙、丙三种物质的溶解度曲线,请回答下列问题:

(1)图中___________ 物质的溶解度曲线受温度影响较小。
(2)t1℃时甲和丙的溶解度为___________ g。
(3)t2℃时若要将N点的甲溶液转变为M点的甲溶液,可采用___________ 的方法。
(4)将t2℃时的甲、乙、丙三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质量分数由大到小的顺序是___________ 。
(5)现有t1℃时100g含溶质质量为5%的甲溶液,要变成t2℃时的饱和溶液,还需要加入___________ 克甲物质。

(1)图中
(2)t1℃时甲和丙的溶解度为
(3)t2℃时若要将N点的甲溶液转变为M点的甲溶液,可采用
(4)将t2℃时的甲、乙、丙三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质量分数由大到小的顺序是
(5)现有t1℃时100g含溶质质量为5%的甲溶液,要变成t2℃时的饱和溶液,还需要加入
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】如图所示,依据甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:

(1)t1℃时,甲、乙、丙三种物质的溶解度的大小关系是_______________ 。
(2)t3℃时,将30g甲物质加入到50g水中,所得溶液的质量为_______________ 。
(3)t1℃时,将甲、乙、丙的饱和溶液都升温到t3℃,溶液仍然饱和的是________ (填“甲”、“乙”或“丙”)
(4)t2℃时,甲、乙、丙三种物质的饱和溶液各100g,分别降温到t1℃时,所得溶液质量的大小关系是_______________ 。

(1)t1℃时,甲、乙、丙三种物质的溶解度的大小关系是
(2)t3℃时,将30g甲物质加入到50g水中,所得溶液的质量为
(3)t1℃时,将甲、乙、丙的饱和溶液都升温到t3℃,溶液仍然饱和的是
(4)t2℃时,甲、乙、丙三种物质的饱和溶液各100g,分别降温到t1℃时,所得溶液质量的大小关系是
您最近一年使用:0次
【推荐2】溶液在生产、生活中有着重要的作用。
(1)生活中常用______ 的方法降低水的硬度。
(2)a、b、c.三种固体物质在水中的溶解度曲线如图所示。

①P点的意义是______ 。
②当a中混有少量b时,可用______ 的方法提纯a。
③t1℃时物质a的饱和溶液中,溶质与溶液质量比为______ (填最简比)。
④t2℃时,分别在100g水中加入等质量的a、b、c,充分搅拌后,所得溶液质量的大小关系不可能是______ (填标号)。
A.a>b=c B.a=b>c C.a=b=c D.a>b>c
(3)科学家们发现,大气中的CO2增加会导致海水的pH下降,使海水酸化。海水酸化对海洋生态系统的影响非常大,例如对珊瑚礁的破坏、对贝类的影响等。请回答以下问题:
①CO2能使海水酸化的原因是______ (用化学方程式表示)。
②目前,科学家们正在研究如何利用海洋生物来减缓海水酸化的发生。请简要说明这种方法:______ 。
(1)生活中常用
(2)a、b、c.三种固体物质在水中的溶解度曲线如图所示。

①P点的意义是
②当a中混有少量b时,可用
③t1℃时物质a的饱和溶液中,溶质与溶液质量比为
④t2℃时,分别在100g水中加入等质量的a、b、c,充分搅拌后,所得溶液质量的大小关系不可能是
A.a>b=c B.a=b>c C.a=b=c D.a>b>c
(3)科学家们发现,大气中的CO2增加会导致海水的pH下降,使海水酸化。海水酸化对海洋生态系统的影响非常大,例如对珊瑚礁的破坏、对贝类的影响等。请回答以下问题:
①CO2能使海水酸化的原因是
②目前,科学家们正在研究如何利用海洋生物来减缓海水酸化的发生。请简要说明这种方法:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】下表是KNO3、NaC1在不同温度下的溶解度(单位:g)
(1)60℃时,50g水中溶解32g硝酸钾形成不饱和溶液,欲使该溶液恰好达到饱和,可以恒温蒸发水的质量______ g(精确到1g);当其它条件不变时,也可以降温到_____ ℃恰好饱和。
(2)KNO3溶液中含有少量NaCl时,可通过_____ 方法提纯。析出的晶体和剩余溶液描述正确的是______ (填写编号)。
A.剩余溶液一定是当时KNO3的饱和溶液
B.剩余溶液一定是当时NaCl的不饱和溶液
C.上述方法无法将两者完全分离
D.析出的晶体中一定不含有NaCl
(3)t℃时,将一定量KNO3的不饱和溶液平均分为三份,分别恒温蒸发出水的质量为5g、10g、15g,析出KNO3晶体的质量依次为ag、bg、cg,则a、b、c三者的关系为_____。
| 温度(℃) | 0 | 10 | 20 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
(2)KNO3溶液中含有少量NaCl时,可通过
A.剩余溶液一定是当时KNO3的饱和溶液
B.剩余溶液一定是当时NaCl的不饱和溶液
C.上述方法无法将两者完全分离
D.析出的晶体中一定不含有NaCl
(3)t℃时,将一定量KNO3的不饱和溶液平均分为三份,分别恒温蒸发出水的质量为5g、10g、15g,析出KNO3晶体的质量依次为ag、bg、cg,则a、b、c三者的关系为_____。
| A.c=a+b | B.c=2b-a | C.c=a+2b | D.c=2a-b |
您最近一年使用:0次




