有一包不纯的NaOH粉末,可能含有Na2SO4、NaCl、CuCl2、NH4Cl、Na2CO3、MgCl2中的一种或几种,为分析含有的杂质,现进行如下实验。
(1)取样溶于水,无固体残留,得无色溶液X。则此粉末中一定不含_________ 。
(2)取溶液X适量,微热,无氨味。则此粉末中一定不含______
(3)另取溶液X适量,滴加BaCl溶液,有白色沉淀,再加入足量稀HNO,沉淀全部溶解,则此粉末中一定不含__ ,沉淀溶解的反应方程式为______
(4)为进一步探究该粉末的成分,可另取溶液X适量,滴加过量M溶液,再滴加N溶液,观察现象。M、N分别为______ (选填序号)。
a 硝酸钡、硝酸银 b 稀硝酸、硝酸银 c 氯化钡、硝酸银
(1)取样溶于水,无固体残留,得无色溶液X。则此粉末中一定不含
(2)取溶液X适量,微热,无氨味。则此粉末中一定不含
(3)另取溶液X适量,滴加BaCl溶液,有白色沉淀,再加入足量稀HNO,沉淀全部溶解,则此粉末中一定不含
(4)为进一步探究该粉末的成分,可另取溶液X适量,滴加过量M溶液,再滴加N溶液,观察现象。M、N分别为
a 硝酸钡、硝酸银 b 稀硝酸、硝酸银 c 氯化钡、硝酸银
2020·江苏镇江·二模 查看更多[4]
2023年江苏省镇江市句容市华阳中学中考模拟化学试题2021年贵州省安顺市乐平中学中考模拟化学试题8(已下线)必刷卷04-2021年中考化学考前信息必刷卷(镇江专用)2020年江苏省镇江市中考二模化学试题
更新时间:2020-07-18 07:20:14
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)小杰在一个玻璃瓶中装了半瓶液体,从另一个玻璃瓶中用镊子取出了一些固体颗粒,他把固体的小颗粒用镊子投入瓶中,立即将瘪气球的开口端套住瓶口,再用橡皮筋拉紧,如图1所示,不久,大家看到气球膨胀起来了,如图2,要产生这种现象,则可能的物质组合是:

(2)小明在塑料瓶里装了液体后,充入了一种气体,立即拧紧瓶盖,一会儿,瓶子变瘪了,如图2,要产生这种现象,则可能的物质组合是:

| 液体 | 固体 | |
| 可能1 | ||
| 可能2 |
| 液体 | 固体 | |
| 可能1 | ||
| 可能2 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐2】以纯碱和石灰石为原料制备烧碱的工艺流程如下图所示。请回答下列问题。

(1)下列物质中均能与石灰石、生石灰、熟石灰发生反应的是_____ (填序号)。
A.水 B.盐酸 C.二氧化碳
(2)步骤④发生反应的化学方程式是____________ 。
(3)如果要检验上述产品中的烧碱溶液里是否含有纯碱,可用的试剂为_____ (填一种试剂的化学式)写出有关化学方程式_______________

(1)下列物质中均能与石灰石、生石灰、熟石灰发生反应的是
A.水 B.盐酸 C.二氧化碳
(2)步骤④发生反应的化学方程式是
(3)如果要检验上述产品中的烧碱溶液里是否含有纯碱,可用的试剂为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】酸、碱、盐是我们身边重要的化合物。请根据所学知识回答相关问题:
(1)舞蹈《只此青绿》创作灵感来自名画《千里江山图》。画作以石青、石绿、赭石、炭黑等矿石为主要颜料。
①“石绿”为孔雀石,其主要成分是碱式碳酸铜(Cu2(OH)2CO3)。碱式碳酸铜由_______ 种元素组成。“石绿”可与稀盐酸反应,根据“石绿”的组成推测与稀盐酸反应的实验现象是_______ 。
②矿物颜料用于画作能避免虫蛀的主要原因是_______ (选填字母)。
A.炭黑有吸附性
B.赭石(氧化铁)有吸水性
C.孔雀石有毒性
(2)完成下列实验报告。
(1)舞蹈《只此青绿》创作灵感来自名画《千里江山图》。画作以石青、石绿、赭石、炭黑等矿石为主要颜料。
①“石绿”为孔雀石,其主要成分是碱式碳酸铜(Cu2(OH)2CO3)。碱式碳酸铜由
②矿物颜料用于画作能避免虫蛀的主要原因是
A.炭黑有吸附性
B.赭石(氧化铁)有吸水性
C.孔雀石有毒性
(2)完成下列实验报告。
| 装置及操作 | 现象 | 解释或结论 | |
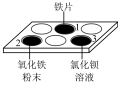 | ①向1中滴加 | 铁片上附着红色周体,溶液颜色变浅 | Fe的金属活动性比Cu的强 |
| ②向2中滴加盐酸 | 固体减少,得到 | 化学方程式: | |
| ③向3中滴加足量稀硫酸 | 氯化钡能与硫酸反应 | ||
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐1】A~G是初中化学常见的七种物质,且A、B、C、D、E属于单质、氧化物、酸、碱、盐五种不同类别的物质,它们之间的关系如图所示。(“—”表示相连的物质能相互反应;“→”表示物质间的转化关系,部分反应物、生成物及反应条件未标出)。已知A物质中含有三种元素;B是单质,其组成元素在地壳中的含量位居第四;物质C的溶液呈蓝色;反应①②的现象相同,都产生白色沉淀;D、G两种物质类别相同,且都易溶于水。试回答:

(1)写出B的化学式:______ ;
(2)物质C在农业生产中的一种用途是______ ;
(3)D与E反应的化学方程式是______ ;
(4)图中反应与转化关系中,涉及______ 种基本反应类型。

(1)写出B的化学式:
(2)物质C在农业生产中的一种用途是
(3)D与E反应的化学方程式是
(4)图中反应与转化关系中,涉及
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】化学就在我们身边,人类的衣、食、住、行都离不开化学。

(1)图1是某服装标签的部分内容。面料和里料中属于合成材料的是___________ 。
(2)某学校的早餐饼配料表见图2,其中富含蛋白质的物质是___________ ;当衣服上沾有花生油时,可用洗涤剂除去,是由于洗涤剂对花生油有___________ 作用。
(3)饮食过量,胃酸会大量分泌,以致消化不良。为缓减该症状,可服用碳酸氢钠片或胃舒平(主要成分为Al(OH)3)治疗,请写出其中任意一个化学反应方程式_______ ,其反应的基本类型均为________ 反应。

(1)图1是某服装标签的部分内容。面料和里料中属于合成材料的是
(2)某学校的早餐饼配料表见图2,其中富含蛋白质的物质是
(3)饮食过量,胃酸会大量分泌,以致消化不良。为缓减该症状,可服用碳酸氢钠片或胃舒平(主要成分为Al(OH)3)治疗,请写出其中任意一个化学反应方程式
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
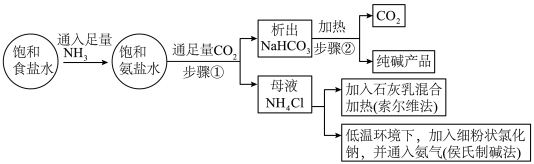
【推荐3】学习以下资料,了解纯碱工业制备历程。
材料1:1791年,法国人吕布兰发明了第一个工业制纯碱的方法,以食盐、硫酸为原料,设备腐蚀严重并且纯度不高。
材料2:1862年,比利时化学家索尔维发明了——索尔维法(又称氨碱法),以食盐、石灰石和氨为原料。氨碱法实现了连续性生产,产品也较为纯净。
材料3:1943年,侯德榜成功揭秘索尔维制碱法,创立了中国人自己的制碱工艺——侯氏制碱法,开创了世界制碱工业的新纪元。侯德榜被称为我国纯碱之父。 NH3↑+HCl↑
NH3↑+HCl↑
(1)饱和食盐水中先通入氨气形成饱和氨盐水,再加压通入二氧化碳,这样操作的目的是_______ ,步骤①过滤后所得滤液是碳酸氢钠的_______ (填“饱和”或者“不饱和”)溶液。
(2)“侯氏制碱法”是在氨碱法基础上,向滤出碳酸氢钠晶体后的氯化铵溶液中加入食盐,使其中的氯化铵单独结晶析出用作_______ (填一种农业上的用途),不采用蒸发结晶的方法得到氯化铵晶体的原因是_______ 。
(3)索尔维法向母液中加入石灰乳混合加热,生成NH3也可回收利用,反应的化学方程式为__________ 。
(4)相比“氨碱法制纯碱”,“侯氏制碱法”的优点有__________ (填字母序号)。
a.侯氏制碱法保留了氨碱法的优点,减少了环境污染,提高了原料利用率
b.不产生用途不大且难处理的CaCl2,对环境更加友好
c.侯氏制碱法中CO2可以循环使用,后续无须补充CO2
(5)写出步骤②中发生反应的化学方程式__________ 。
材料1:1791年,法国人吕布兰发明了第一个工业制纯碱的方法,以食盐、硫酸为原料,设备腐蚀严重并且纯度不高。
材料2:1862年,比利时化学家索尔维发明了——索尔维法(又称氨碱法),以食盐、石灰石和氨为原料。氨碱法实现了连续性生产,产品也较为纯净。
材料3:1943年,侯德榜成功揭秘索尔维制碱法,创立了中国人自己的制碱工艺——侯氏制碱法,开创了世界制碱工业的新纪元。侯德榜被称为我国纯碱之父。
 NH3↑+HCl↑
NH3↑+HCl↑(1)饱和食盐水中先通入氨气形成饱和氨盐水,再加压通入二氧化碳,这样操作的目的是
(2)“侯氏制碱法”是在氨碱法基础上,向滤出碳酸氢钠晶体后的氯化铵溶液中加入食盐,使其中的氯化铵单独结晶析出用作
(3)索尔维法向母液中加入石灰乳混合加热,生成NH3也可回收利用,反应的化学方程式为
(4)相比“氨碱法制纯碱”,“侯氏制碱法”的优点有
a.侯氏制碱法保留了氨碱法的优点,减少了环境污染,提高了原料利用率
b.不产生用途不大且难处理的CaCl2,对环境更加友好
c.侯氏制碱法中CO2可以循环使用,后续无须补充CO2
(5)写出步骤②中发生反应的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
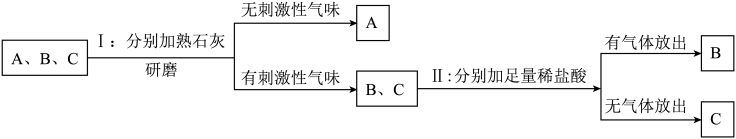
【推荐1】实验室有三瓶化肥未贴标签,只知道它们分别是碳酸氢铵(NH4HCO3)、氯化铵(NH4Cl)和尿素[CO(NH2)2]中的一种,为鉴别三种化肥,某同学分别取少量样品编号为A、B、C,并进行如下实验:(此处箭头表示得出实验结论)
(1)写出三种化肥的名称:A______ ;B______ ;C______ 。
(2)实验I中C与熟石灰反应的化学方程式为______ 。
(3)实验Ⅱ中有气体放出,反应的化学方程式为______ 。
(1)写出三种化肥的名称:A
(2)实验I中C与熟石灰反应的化学方程式为
(3)实验Ⅱ中有气体放出,反应的化学方程式为
您最近一年使用:0次
【推荐2】海洋是一个巨大的资源宝库,可以从海水中制得粗盐,以粗盐水为原料综合利用的部分途径如图所示:
(2)按加入试剂的正确顺序,过滤后的滤液A中溶质有_______ (填化学式);在该流程中,是先向饱和食盐水中通入过量的氨气,然后再通入过量的二氧化碳,先通入过量氨气的目的是_______ 。
(3)若向分离出NaHCO3晶体后的母液B(含有NH4Cl)中加入过量Ca(OH)2,则可获得一种可以循环使用的物质,其化学式是_______ 。
(4)上述流程涉及到的基本反应类型有_______ 。

| A.Na2CO3、NaOH、BaCl2 |
| B.BaCl2、Na2CO3、NaOH |
| C.NaOH、BaCl2、Na2CO3 |
(2)按加入试剂的正确顺序,过滤后的滤液A中溶质有
(3)若向分离出NaHCO3晶体后的母液B(含有NH4Cl)中加入过量Ca(OH)2,则可获得一种可以循环使用的物质,其化学式是
(4)上述流程涉及到的基本反应类型有
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐3】现有一包固体混合物A,其中可能含有硝酸铵、硫酸钾、硝酸铜、氯化钠四种物质中的一种或多种.现按图所示进行检验,出现的现象如图中所述(假设过程中所有发生的反应都恰好完全反应).请你依据实验过程和产生的现象做出分析与判断:

(1)气体B的化学式是________ .
(2)步骤④发生反应的化学方程式______________________________ .
(3)通过上述现象判断,该固体混合物A中一定含有的物质是______________________________ ;不能确定是否含有的物质是______ ,如果要证明混合物A中确实含有该物质,可用滤液F继续实验.请简要说出继续实验的操作步骤和现象______________________________________ .

(1)气体B的化学式是
(2)步骤④发生反应的化学方程式
(3)通过上述现象判断,该固体混合物A中一定含有的物质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】在“宏观-微观-符号”之间建立联系,是化学学科特有的思维方式,能帮助我们更好地认识物质变化的本质。请完成下列问题:

(其中“ ”表示碳原子,“
”表示碳原子,“ ”表示氧原子,“
”表示氧原子,“ ”表示氢原子)
”表示氢原子)
(1)请写出该反应的化学方程式______ ,上述反应的产物C、D中,与CO2组成元素相同的是(填字母序号)______ 。
(2)由初中学习可知:中和反应的微观实质是氢离子和氢氧根离子结合生成了水分子,即: 。像这种用实际参加反应的离子符号来表示化学反应的式子叫离子方程式。
。像这种用实际参加反应的离子符号来表示化学反应的式子叫离子方程式。
离子方程式的书写一般按以下步骤(以氯化镁溶液与氢氧化钾溶液反应为例):
Ⅰ、写出氯化镁溶液与氢氧化钾溶液反应的化学方程式:______ 。
Ⅱ、把易溶于水、易电离的物质写成离子形式,难溶的物质、气体和水等仍用化学式表示。
上述方程式可改写成: :
:
删去两边不参加反应的离子即得离子方程式: 。
。
请回答:
①写出碳酸钠溶液和稀盐酸反应的离子方程式:______ 。
②写出一个与 相对应的化学方程式:
相对应的化学方程式:______ 。
③下列各组离子,在pH=3的无色水溶液中能大量共存的是______ (填序号)。
A.K+、Fe2+、C1-、 B.Na+、Ca2+、
B.Na+、Ca2+、 、OH-
、OH-
C.Na+、Ca2+、C1-、 D.
D. 、Ba2+、C1-、
、Ba2+、C1-、

(其中“
 ”表示碳原子,“
”表示碳原子,“ ”表示氧原子,“
”表示氧原子,“ ”表示氢原子)
”表示氢原子)(1)请写出该反应的化学方程式
(2)由初中学习可知:中和反应的微观实质是氢离子和氢氧根离子结合生成了水分子,即:
 。像这种用实际参加反应的离子符号来表示化学反应的式子叫离子方程式。
。像这种用实际参加反应的离子符号来表示化学反应的式子叫离子方程式。离子方程式的书写一般按以下步骤(以氯化镁溶液与氢氧化钾溶液反应为例):
Ⅰ、写出氯化镁溶液与氢氧化钾溶液反应的化学方程式:
Ⅱ、把易溶于水、易电离的物质写成离子形式,难溶的物质、气体和水等仍用化学式表示。
上述方程式可改写成:
 :
:删去两边不参加反应的离子即得离子方程式:
 。
。请回答:
①写出碳酸钠溶液和稀盐酸反应的离子方程式:
②写出一个与
 相对应的化学方程式:
相对应的化学方程式:③下列各组离子,在pH=3的无色水溶液中能大量共存的是
A.K+、Fe2+、C1-、
 B.Na+、Ca2+、
B.Na+、Ca2+、 、OH-
、OH-C.Na+、Ca2+、C1-、
 D.
D. 、Ba2+、C1-、
、Ba2+、C1-、
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐2】酸、碱、盐的溶解性表是学习化学的重要工具之一。下表是部分酸、碱、盐在水中的溶解性(20。C),请回答下列问题。
(1)上述阴、阳离子形成不溶性碱的化学式为________ , 形成复合肥料的化学式为_____ 。
(2)KOH溶液和Ba(NO3)2溶液_______ (填“能“或“不能“)反应,理由是_______ 。
(3)下列各组离子在水溶液中能大量共存的是_______________ 。
A. OH-H+Ba2+NO B. OH-Ba2+K+Cl-
B. OH-Ba2+K+Cl-
C. CO K+Ba2+Cl-D. CO
K+Ba2+Cl-D. CO Cu2+NO
Cu2+NO K+
K+
| 阴离子 阳离子 | OH- | NO3- | CO32- | Cl- |
| K+ | 溶 | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 不 | 溶 |
| Cu2+ | 不 | 溶 | 不 | 溶 |
(1)上述阴、阳离子形成不溶性碱的化学式为
(2)KOH溶液和Ba(NO3)2溶液
(3)下列各组离子在水溶液中能大量共存的是
A. OH-H+Ba2+NO
 B. OH-Ba2+K+Cl-
B. OH-Ba2+K+Cl-C. CO
 K+Ba2+Cl-D. CO
K+Ba2+Cl-D. CO Cu2+NO
Cu2+NO K+
K+
您最近一年使用:0次



