孔雀石是冶炼金属铜的主要原料,其主要成分是Cu2(OH)2CO3〔可看成是Cu(OH)2·CuCO3〕,还含少量氧化铁和二氧化硅。以下为“湿法炼铜”并制备其它副产品氯化钠和铁红(氧化铁)的工业流程。
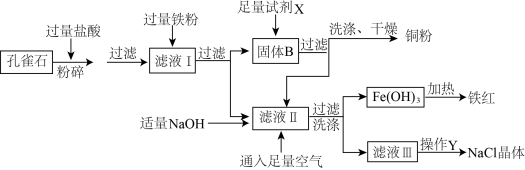
【查阅资料】①二氧化硅不溶于水,也不与酸反应。
②铁能与氯化铁溶液反应,反应方程式为2FeCl3+Fe=3FeCl2。
③氢氧化亚铁(白色固体)易被氧气氧化,反应方程式为4Fe(OH)2+2H2O+O2=4Fe(OH)3。
回答下列问题:
(1)将孔雀石粉碎的目的是____ ;
(2)写出盐酸与Cu2(OH)2CO3反应的化学方程式____ ;
(3)在滤液Ⅰ中加入过量铁粉,搅拌至充分反应,其中发生的置换反应有____ 个;
(4)在洗涤、干燥获取铜粉时,判断洗涤干净的方法是____ ;
(5)滤液Ⅱ的溶质为____ (填化学式);若取少量滤液Ⅱ于试管中,逐滴滴加适量氢氧化钠溶液后静置。该过程中的实验现象为____ ;
(6)操作Y的名称是____ ,该操作中需要使用的仪器有铁架台、坩埚钳、酒精灯、玻璃棒、____ 。

【查阅资料】①二氧化硅不溶于水,也不与酸反应。
②铁能与氯化铁溶液反应,反应方程式为2FeCl3+Fe=3FeCl2。
③氢氧化亚铁(白色固体)易被氧气氧化,反应方程式为4Fe(OH)2+2H2O+O2=4Fe(OH)3。
回答下列问题:
(1)将孔雀石粉碎的目的是
(2)写出盐酸与Cu2(OH)2CO3反应的化学方程式
(3)在滤液Ⅰ中加入过量铁粉,搅拌至充分反应,其中发生的置换反应有
(4)在洗涤、干燥获取铜粉时,判断洗涤干净的方法是
(5)滤液Ⅱ的溶质为
(6)操作Y的名称是
2020·江苏南京·二模 查看更多[3]
2020年江苏省南京市玄武区南京市外国语学校中考二模化学试题(已下线)化学-(苏州卷)【试题猜想】2021年中考考前最后一卷(已下线)第08讲 阶段性测试卷(9-11单元)-【寒假自学课】2024年九年级化学寒假提升学与练(人教版)
更新时间:2020-07-13 08:17:18
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐1】金属钛(Ti)的硬度大、熔点高、常温下耐酸碱,是航海、医疗等不可或缺的材料。钛铁矿(主要成分FeTiO3)是工业上冶炼金属钛的主要原料,制备金属钛的一种工艺流程如图所示(部分产物略):
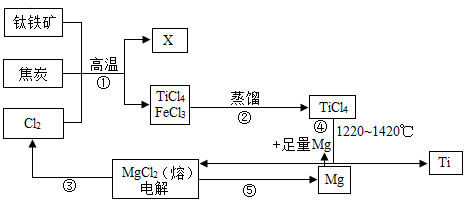
(1)步骤①中要先将钛铁矿和焦炭粉碎,目的是:__________ 。
(2)X为可燃性氧化物,其化学式为__________ 。
(3)步骤④的化学方程式为:___________ ,该反应的基本反应类型是__________ 。
(4)该流程中可以循环利用的物质是___________ 。(答出一种即可)

(1)步骤①中要先将钛铁矿和焦炭粉碎,目的是:
(2)X为可燃性氧化物,其化学式为
(3)步骤④的化学方程式为:
(4)该流程中可以循环利用的物质是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】已知下图中A~K均为初中化学常见的物质,各物质之间的转化关系如图所示(反应条件已略去)。固态C叫做干冰,F和E常用来配制医用酒精溶液,J为浅绿色溶液。
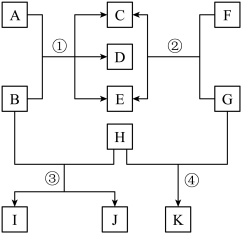
请回答下列问题:
(1)C的化学式为_______ 。
(2)反应①的化学方程式_______ (写出一个即可);
(3)G的一种用途_______ 。
(4)反应③的基本反应类型_______ 。
(5)反应④的实验现象_______ 。

请回答下列问题:
(1)C的化学式为
(2)反应①的化学方程式
(3)G的一种用途
(4)反应③的基本反应类型
(5)反应④的实验现象
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐3】A-G是纯净物且A、B、C、D、E是初中化学中常见的不同类别的物质。它们之间的关系如图所示(“→”表示物质间的转化关系,“—”表示两端的物质能发生化学反应)。A是草木灰的主要成分,B是光合作用不可缺少的物质,D是由两种元素组成的化合物,E是黑色粉末,F是未来最理想的清洁能源,请回答下列问题:
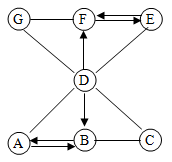
(1)写出物质E的化学式:________ 。
(2)D→F反应的基本类型是________ 。
(3)物质A和物质D反应的化学方程式是_______ 。
(4)古代常将草木灰与C溶液混合,滤取反应后清液作漂洗的洗涤剂。写出此反应的化学方程式________ 。

(1)写出物质E的化学式:
(2)D→F反应的基本类型是
(3)物质A和物质D反应的化学方程式是
(4)古代常将草木灰与C溶液混合,滤取反应后清液作漂洗的洗涤剂。写出此反应的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】图中表示的是几种常见物质的转化关系(部分反应条件、反应物、生成物省略)。已知C为生活中不可缺少的调味品,D是一种常见气体,F为大理石的主要成分,请回答以下问题:
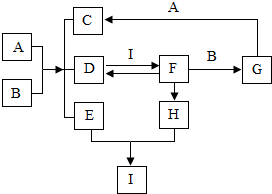
(1)写出E的化学式_____ ;
(2)写出A和B反应的化学方程式_______________ ,属于____ 反应基本类型;
(3)写出D和I的溶液反应的现象_________________ ;
(4)写出I的一种用途__________ 。

(1)写出E的化学式
(2)写出A和B反应的化学方程式
(3)写出D和I的溶液反应的现象
(4)写出I的一种用途
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐2】某兴趣小组利用废镍材料(含有金属Ni及少量Fe、Ag)探究相关物质的性质并回收镍,设计流程如图(小部分产物略去)。
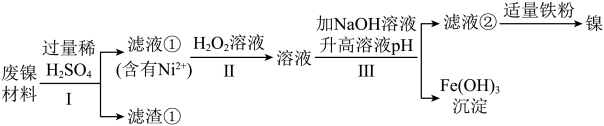
查阅资料:a.H2O2溶液可将Fe2+转化为Fe3+。
b.Fe3+ 、Ni2+转化为对应的氢氧化物沉淀时,溶液pH如图
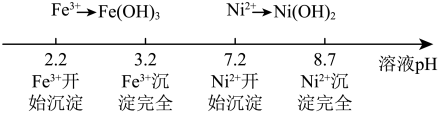
(1)步骤Ⅰ的操作为______ 。
(2)滤渣①的成分为______ 。
(3)单质Fe参与反应的化学方程式为______ 。(任写一个)
(4)滤液②中有Ni2+、无Fe3+,则滤液②pH可能为______ (填序号)。
A.pH=1 B.pH=2 C.pH=6 D.pH=10
(5)Ni、Fe、Ag三种金属的活动性由强到弱的顺序为______ 。

查阅资料:a.H2O2溶液可将Fe2+转化为Fe3+。
b.Fe3+ 、Ni2+转化为对应的氢氧化物沉淀时,溶液pH如图

(1)步骤Ⅰ的操作为
(2)滤渣①的成分为
(3)单质Fe参与反应的化学方程式为
(4)滤液②中有Ni2+、无Fe3+,则滤液②pH可能为
A.pH=1 B.pH=2 C.pH=6 D.pH=10
(5)Ni、Fe、Ag三种金属的活动性由强到弱的顺序为
您最近一年使用:0次
【推荐3】海水晒盐得到粗盐,剩余的母液称为苦卤,粗盐和苦卤用途广泛。
(1)为了除去粗盐溶液中的 Ca2+、Mg2+、 ,可按照下列实验操作进行:①加过量Na2CO3溶液;②加过量NaOH 溶液;③加过量BaCl2溶液;④加入适量盐酸;⑤过滤。请你排出一种合理的操作顺序
,可按照下列实验操作进行:①加过量Na2CO3溶液;②加过量NaOH 溶液;③加过量BaCl2溶液;④加入适量盐酸;⑤过滤。请你排出一种合理的操作顺序________ (用序号表示) ,其中步骤中加过量 BaCl2溶液的目的是________ ,步骤中加入适量盐酸的目的是________ 。
(2)镁广泛应用于火箭、导弹和飞机制造业;利用苦卤制取镁的主要流程如图:
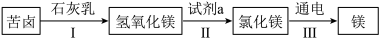
步骤 II 中反应的化学方程式是________ ;上述流程中发生复分解反应的步骤是 ________ ;用苦卤制取镁比直接用海水制取镁的优势是________ 。
(3)请回答海水制碱的相关题目
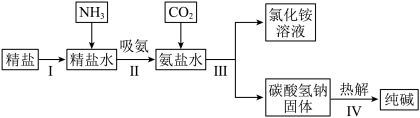
①步骤Ⅲ、步骤Ⅳ反应的化学方程式为:________ 、________ 。
②如果不将氯化铵作为目标产品,即加入氨气不是为了生产出氯化铵,那么,氨气在制碱过程中的作用是________ 。
③工业生产纯碱的流程中,碳酸化时溶液中析出碳酸氢钠而没有析出氯化铵的原因是________ 。
(1)为了除去粗盐溶液中的 Ca2+、Mg2+、
 ,可按照下列实验操作进行:①加过量Na2CO3溶液;②加过量NaOH 溶液;③加过量BaCl2溶液;④加入适量盐酸;⑤过滤。请你排出一种合理的操作顺序
,可按照下列实验操作进行:①加过量Na2CO3溶液;②加过量NaOH 溶液;③加过量BaCl2溶液;④加入适量盐酸;⑤过滤。请你排出一种合理的操作顺序(2)镁广泛应用于火箭、导弹和飞机制造业;利用苦卤制取镁的主要流程如图:

步骤 II 中反应的化学方程式是
(3)请回答海水制碱的相关题目

①步骤Ⅲ、步骤Ⅳ反应的化学方程式为:
②如果不将氯化铵作为目标产品,即加入氨气不是为了生产出氯化铵,那么,氨气在制碱过程中的作用是
③工业生产纯碱的流程中,碳酸化时溶液中析出碳酸氢钠而没有析出氯化铵的原因是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】已知A、B、C、D是初中化学常见的物质,其中C属于碱,A与D的物质类别不同,它们存在如下反应关系和转化关系。“一” 表示相连的物质能发生反应,“→”表示一 种物质能生成另一种物质(部分反应物、生成物及反应条件已省略)。请回答下列问题:
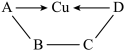
(1)A的化学式为____________ 。
(2)D物质的水溶液呈__________ 色;D→Cu的反应属于__________ (填基本反应类型)。
(3)B与C反应的化学方程式为___________ (写一个);C与D能够发生反应的原因是_______ 。

(1)A的化学式为
(2)D物质的水溶液呈
(3)B与C反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】粗盐的提纯
粗盐经过溶解、过滤操作得到的盐溶液含有可溶性杂质(Na2SO4、CaCl2、MgCl2),这些杂质可利用化学方法除去。
(1)仪器的选择:在过滤操作过程中,使用的玻璃仪器有______
(2)试剂的选择:按下表所示顺序,完成实验。
(3)依次加入选择的试剂后,过滤得到澄清的溶液,还需要加入过量的试剂______ ,然后进行______ 操作,可以得到比较纯净的氯化钠晶体。
(4)在实验过程中只加入一种试剂,也可以同时除去Na2SO4、MgCl2这两种杂质,该试剂是______ (填化学式)
粗盐经过溶解、过滤操作得到的盐溶液含有可溶性杂质(Na2SO4、CaCl2、MgCl2),这些杂质可利用化学方法除去。
(1)仪器的选择:在过滤操作过程中,使用的玻璃仪器有
(2)试剂的选择:按下表所示顺序,完成实验。
| 顺序 | 杂质 | 加入的试剂(过量) | 化学方程式或实验现象 |
| ① | Na2SO4 | 氯化钡 | 实验现象是 |
| ② | MgCl2 | 氢氧化钠 | 书写化学方程式 |
| ③ | CaCl2 | 实验现象是有白色沉淀生成 |
(4)在实验过程中只加入一种试剂,也可以同时除去Na2SO4、MgCl2这两种杂质,该试剂是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】为探究工业废水的综合利用,某化学小组在实验室中完成了以下实验。
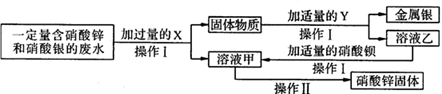
①固体物质的成分有哪些____________ ?
②写出乙与硝酸钡反应的化学方程式_________________ ?
③操作I和操作Ⅱ中都要用到一种玻璃仪器。该仪器在操作Ⅱ中的作用是什么______________ ?

①固体物质的成分有哪些
②写出乙与硝酸钡反应的化学方程式
③操作I和操作Ⅱ中都要用到一种玻璃仪器。该仪器在操作Ⅱ中的作用是什么
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】金属蚀刻加工过程中,常用盐酸对其表面氧化物进行清洗,会产生酸洗废水。pH在1.5左右的某酸洗废水中含铁元素质量分数约3%,其他金属元素如铜、镍浓度较低,工业上综合利用酸洗废水可制备六水合氯化铁。制备过程如下:
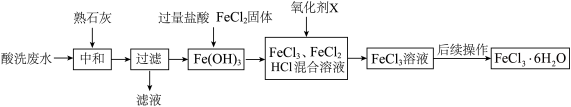
【查阅资料】
I.相关金离子生成氢氧化物沉淀的pH如下表所示:
Ⅱ.已知FeCl3溶液加热过程中会与水反应生成Fe(OH)3
请回答下列问题:
(1)“中和”时,熟石灰与酸洗废水中铁的盐溶液发生的反应方程式为___ 。
(2)加入熟石灰调节溶液pH的范围为:____ pH____ ,有利于将酸洗废水中的铁元素完全沉淀并制备纯度较高的产品。
(3)“氧化”时,利用氧化剂H2O2在酸性条件下将FeCl2氧化成FeCl3和一种常见液体,其反应方程式为_____ 。
(4)将得到的FeCl3溶液在HCl气氛中蒸发浓缩、冷却结晶、过滤、洗涤、干燥得FeCl3 ▪6H2O晶体.其中“蒸发浓缩”时玻璃棒的作用是____ 。FeCl3溶液在HCl气氛中加热的目的是_____ 。

【查阅资料】
I.相关金离子生成氢氧化物沉淀的pH如下表所示:
| 氢氧化物 | Fe(OH)3 | Cu(OH)2 | Ni(OH)2 |
| 开始沉淀pH | 1.5 | 4.2 | 7.1 |
| 沉淀完全pH | 3.7 | 6.7 | 9.2 |
请回答下列问题:
(1)“中和”时,熟石灰与酸洗废水中铁的盐溶液发生的反应方程式为
(2)加入熟石灰调节溶液pH的范围为:
(3)“氧化”时,利用氧化剂H2O2在酸性条件下将FeCl2氧化成FeCl3和一种常见液体,其反应方程式为
(4)将得到的FeCl3溶液在HCl气氛中蒸发浓缩、冷却结晶、过滤、洗涤、干燥得FeCl3 ▪6H2O晶体.其中“蒸发浓缩”时玻璃棒的作用是
您最近一年使用:0次




