某工厂化验室用氢氧化钠溶液中和一定量石油产品中的残余硫酸至中性,共消耗5%的氢氧化钠溶液160g.这一定量石油产品中含H2SO4的质量是多少?
19-20九年级下·安徽合肥·阶段练习 查看更多[3]
(已下线)化学(北京卷)-学易金卷:2024年中考考前押题密卷安徽省合肥市包河区科大附中2019-2020 学年九年级下学期第二次月考化学试题安徽省合肥市中国科技大学附属中学2019-2020学年九年级下学期检测试卷(二)化学试题
更新时间:2020-12-18 18:34:36
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】氢气是一种理想的清洁、高能燃料。实验室常用锌与稀硫酸反应来制取氢气。某同学在实验室用3.25g锌与25.00g稀硫酸充分反应,无固体剩余。
(1)氢气是清洁能源,其燃烧产物是______ (填名称)。
(2)计算制得氢气的质量(写出计算过程)。
(1)氢气是清洁能源,其燃烧产物是
(2)计算制得氢气的质量(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】气体A是一种氮的氧化物,由某些含氮化合物产生,可用于治疗心绞痛。
(1)一种转化为A的方法是:硝化甘油(C3H5O9N3)在人体内氧化,其方程式为4C3H5N3O9+5O2═12A+12CO2+10H2O,则A的化学式为_______。
(2)另一种转化为A的方法是:铜与稀硝酸反应,其化学方程式为3Cu+8HNO3(稀)═3Cu(NO3)2+2A↑+4H2O。现用6.4kg铜与足量的稀硝酸反应,计算理论上能生成A的质量_____。(写出计算过程)
(1)一种转化为A的方法是:硝化甘油(C3H5O9N3)在人体内氧化,其方程式为4C3H5N3O9+5O2═12A+12CO2+10H2O,则A的化学式为_______。
(2)另一种转化为A的方法是:铜与稀硝酸反应,其化学方程式为3Cu+8HNO3(稀)═3Cu(NO3)2+2A↑+4H2O。现用6.4kg铜与足量的稀硝酸反应,计算理论上能生成A的质量_____。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】用盐酸洗钢材会产生“酸洗废液”(主要成分为 FeCl2和H2O,其他杂质忽略不计),工业上用“酸洗废液”经高温氧化制取高纯氧化铁,同时产生的氯化氢可回收使用,主要反应原理为: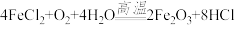 某化工厂有 5 t“酸洗废液”,经过上述反应后可得 0.73t 氯化氢气体。计算:
某化工厂有 5 t“酸洗废液”,经过上述反应后可得 0.73t 氯化氢气体。计算:
(1)产生的氯化氢可以制得 10%的稀盐酸的质量为______t。
(2)计算“酸洗废液”中 FeCl2的质量分数(写出计算过程,结果保留 0.1%)。
(3) “酸洗废液”充分反应后,剩余水的质量为______t。
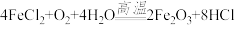 某化工厂有 5 t“酸洗废液”,经过上述反应后可得 0.73t 氯化氢气体。计算:
某化工厂有 5 t“酸洗废液”,经过上述反应后可得 0.73t 氯化氢气体。计算:(1)产生的氯化氢可以制得 10%的稀盐酸的质量为______t。
(2)计算“酸洗废液”中 FeCl2的质量分数(写出计算过程,结果保留 0.1%)。
(3) “酸洗废液”充分反应后,剩余水的质量为______t。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】常温下,向盛有100gNaOH溶液的烧杯中逐滴加入溶质质量分数为3.65%的稀盐酸,测得反应过程中溶液的pH与加入稀盐酸的质量如图所示:

(1)当溶液为中性时,消耗稀盐酸的质量为______ g。
(2)计算恰好完全反应时,所得溶液的溶质质量分数。

(1)当溶液为中性时,消耗稀盐酸的质量为
(2)计算恰好完全反应时,所得溶液的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
名校
【推荐2】某工厂排放的废水中含有亚硫酸钠(Na2SO3)未经处理,会造成污染。化学兴趣小组的同学对废水处理设计了如图所示的实验方案:

试计算:
(l)反应完后生成亚硫酸钙沉淀的质量为_______g。
(2)废水中亚硫酸钠的质量分数为_________(请写出计算过程)。(温馨提示:Na2SO3+CaCl2=CaSO3↓+2NaCl;氯化钙不与废水中的其它杂质反应)

试计算:
(l)反应完后生成亚硫酸钙沉淀的质量为_______g。
(2)废水中亚硫酸钠的质量分数为_________(请写出计算过程)。(温馨提示:Na2SO3+CaCl2=CaSO3↓+2NaCl;氯化钙不与废水中的其它杂质反应)
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
【推荐3】铁铜金属粉末常用于生产机械零件。为测定某铁铜金属粉末中铁粉的含量,取20g样品于烧杯中,逐滴加入稀硫酸充分反应后,测得固体质量随加入稀硫酸的质量关系如图所示。计算:
(2)生成氢气的质量。
(3)所用稀硫酸的溶质质量分数。

(2)生成氢气的质量。
(3)所用稀硫酸的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】实验室欲测定一瓶标签破损的稀硫酸的溶质质量分数。现取10g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液加入,溶液的pH的变化如下图所示。试回答:

(1)b点表示____________________。
(2)当pH=7时,消耗_______________gNaOH溶液,其溶质NaOH的质量为______g。
(3)计算10g稀硫酸中溶质的质量_____。

(1)b点表示____________________。
(2)当pH=7时,消耗_______________gNaOH溶液,其溶质NaOH的质量为______g。
(3)计算10g稀硫酸中溶质的质量_____。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将5%的NaOH溶液逐滴加入到20克稀盐酸中,边加边搅拌,随着NaoH溶液的加入,溶液pH的变化如图所示。试回答:

(1)b点溶液中存在的阴离子有___________ 。(写符号)
(2)当恰好完全反应时,消耗NaOH溶液的质量为___________ 克。
(3)计算稀盐酸中溶质的质量分数(写出计算过程)。

(1)b点溶液中存在的阴离子有
(2)当恰好完全反应时,消耗NaOH溶液的质量为
(3)计算稀盐酸中溶质的质量分数(写出计算过程)。
您最近一年使用:0次




