某化学实验小组利用如图装置探究一氧化碳还原氧化铁的实验:向氧化铁中通入纯净的一氧化碳气体,请回答下列问题。
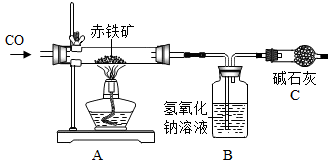
(1)实验过程中观察到装置A中玻璃管内发生的现象_______ ;
(2)写出B装置发生的化学反应方程式是_______ ;
(3)从环境保护的角度看该实验存在的缺陷是_______ ;
(4)实验结束时先撤去酒精灯,继续通入一氧化碳,其目的是_______
(5)实验前称量纯净的Fe2O3质量为20g。通入足量的一氧化碳完全反应后B装置总质量增加了13.2g,则反应后A中玻璃管内剩余物质为_____ (填“纯净物”或“混合物”)。

(1)实验过程中观察到装置A中玻璃管内发生的现象
(2)写出B装置发生的化学反应方程式是
(3)从环境保护的角度看该实验存在的缺陷是
(4)实验结束时先撤去酒精灯,继续通入一氧化碳,其目的是
(5)实验前称量纯净的Fe2O3质量为20g。通入足量的一氧化碳完全反应后B装置总质量增加了13.2g,则反应后A中玻璃管内剩余物质为
20-21九年级上·黑龙江大庆·阶段练习 查看更多[3]
河北省邯郸市2020-2021学年九年级上学期第三次月考化学试题(已下线)练习11 金属矿物 铁的冶炼 金属防护和废金属回收-2020-2021学年【补习教材·寒假作业】九年级化学(沪教版)黑龙江省大庆市让胡路区庆新中学2020-2021学年九年级上学期第一次月考化学试题
更新时间:2020-12-22 12:15:23
|
相似题推荐
实验题
|
较难
(0.4)
【推荐1】某化学学习小组做CO还原Fe2O3实验时,查阅资料发现CO还原Fe2O3的实验中若温度不同、受热不均时,除生成Fe外,还会生成Fe3O4。其中Fe3O4为金属氧化物,可与盐酸反应,不与硫酸铜溶液反应。为定量测定生成物的成分,某同学用下图所示的实验方案进行实验并记录数据:

试回答:
(1)写出CO还原Fe2O3生成Fe的化学方程式_____ ;
(2)过滤操作需要的玻璃仪器是烧杯、玻璃棒和_____ ;方案中加入过量盐酸的目的是_____ ;
(3)根据以上实验数据,计算17.2g生成物中Fe3O4的质量为_____ 。
(4)如得到17.2g生成物,计算参加反应的Fe2O3的质量_____ 。

试回答:
(1)写出CO还原Fe2O3生成Fe的化学方程式
(2)过滤操作需要的玻璃仪器是烧杯、玻璃棒和
(3)根据以上实验数据,计算17.2g生成物中Fe3O4的质量为
(4)如得到17.2g生成物,计算参加反应的Fe2O3的质量
您最近一年使用:0次
实验题
|
较难
(0.4)
名校
【推荐2】金属材料在生产、生活中有广泛的应用。请依据学知识完成下列问题!
(1)下列物质中属于金属材料的有______。
(2)“每金七厘造方寸金一千片”体现了黄金具有良好的______ 。
(3)防止自行车链条生锈的措施是______ 。
(4)奖牌材料选择合金,是利用了合金的______性质。
(5)①小舟同学准备在实验室用如图所示装置模拟工业炼铁。

A 中反应的化学方程式为:______ 。
②某同学实验完成后,发现过量的澄渣石灰水增重 4.4g,则该同学通入装置的 CO 气体质量______ 2.8g(填“大于”“等于”“小于”)。
③某同学认为也可以将上图 B 中澄清石灰水及尾部酒精灯装置换成下图装置,下列装置中你认为最为合理的是______ 。

(1)下列物质中属于金属材料的有______。
| A.象牙 | B.黄金 | C.丝织品 | D.青铜 | E.人造骨 |
(3)防止自行车链条生锈的措施是
(4)奖牌材料选择合金,是利用了合金的______性质。
| A.硬度大 | B.耐磨性好 | C.抗腐蚀性强 | D.色泽美观 |

A 中反应的化学方程式为:
②某同学实验完成后,发现过量的澄渣石灰水增重 4.4g,则该同学通入装置的 CO 气体质量
③某同学认为也可以将上图 B 中澄清石灰水及尾部酒精灯装置换成下图装置,下列装置中你认为最为合理的是

您最近一年使用:0次
实验题
|
较难
(0.4)
【推荐3】化学兴趣小组的同学设计了用一氧化碳还原氧化铁的实验装置,如图所示,请回答下列问题。

(1)实验开始时,应_____ (填“先加热再通CO”或“先通CO再加热”),a管中观察到的现象_____ 。
(2)B装置除了吸收CO2气体外,还_____ 。
(3)为了防止溶液倒吸,本实验停止加热前是否需要先断开A和B的连接处?_____ (填“需要”或“不需要”),理由是_____ 。
(4)若a管中氧化铁全部还原成铁,冷却后称量铁的质量比反应前氧化铁的质量减少了6g,则加入a管中的氧化铁的质量是_____ g

(1)实验开始时,应
(2)B装置除了吸收CO2气体外,还
(3)为了防止溶液倒吸,本实验停止加热前是否需要先断开A和B的连接处?
(4)若a管中氧化铁全部还原成铁,冷却后称量铁的质量比反应前氧化铁的质量减少了6g,则加入a管中的氧化铁的质量是
您最近一年使用:0次
实验题
|
较难
(0.4)
解题方法
【推荐1】重庆地区盛产页岩气(主要成分为CH4),某兴趣小组利用如图所示的装置对CH4与CuO反应的产物进行探究(假设产物都能被相应试剂完全吸收)。

【查阅资料】
①氧化亚铜为红色固体,与稀硫酸反应的化学方程式为Cu2O+H2SO4=Cu+CuSO4+H2O。
②CH4与CuO反应的气体产物可能为CO、CO2、水蒸气中某几种。
③白色无水硫酸铜固体遇水变为蓝色硫酸铜晶体。
【实验】
实验进行一段时间后,发现黑色粉末中产生了红色固体们对红色固体提出了如下猜想。
猜想一:固体为Cu 猜想二:固体为Cu2O 猜想三:固体为Cu和Cu2O
(1)他们将红色固体浸泡在稀硫酸溶液中,无明显现象,则猜想__________ 正确。
(2)装置B中白色固体变蓝,气体产物中有____________ (填化学式)。
(3)装置C中出现浑浊现象,反应的化学方程式为_____________ 。
(4)经装置D干燥后的气体可点燃,但他们认为不能判断一定有CO,原因是_____________ 。
(5)实验结束后,他们发现装置B与装置C增加的质量比为9:11,结合(2)的结论,可判断产物中___ (填 “有”或“无”)CO。装置A中反应的化学方程式为______________ 。

【查阅资料】
①氧化亚铜为红色固体,与稀硫酸反应的化学方程式为Cu2O+H2SO4=Cu+CuSO4+H2O。
②CH4与CuO反应的气体产物可能为CO、CO2、水蒸气中某几种。
③白色无水硫酸铜固体遇水变为蓝色硫酸铜晶体。
【实验】
实验进行一段时间后,发现黑色粉末中产生了红色固体们对红色固体提出了如下猜想。
猜想一:固体为Cu 猜想二:固体为Cu2O 猜想三:固体为Cu和Cu2O
(1)他们将红色固体浸泡在稀硫酸溶液中,无明显现象,则猜想
(2)装置B中白色固体变蓝,气体产物中有
(3)装置C中出现浑浊现象,反应的化学方程式为
(4)经装置D干燥后的气体可点燃,但他们认为不能判断一定有CO,原因是
(5)实验结束后,他们发现装置B与装置C增加的质量比为9:11,结合(2)的结论,可判断产物中
您最近一年使用:0次
实验题
|
较难
(0.4)
【推荐2】金属铁是当今用途最广的金属,现研究铁的冶炼。
【研究一】实验室模拟炼铁(装置如下图)。

已知:B装置中的液体为过量的氢氧化钠与氢氧化钙混合液,氢氧化钠吸收二氧化碳能力比氢氧化钙强。请回答下列问题:
(1)实验过程中A处玻璃管中的实验现象:________ 。
(2)写出B处反应的化学方程式:________ 。
(3)实验装置按图连接,请将以下四步按正确操作步骤排序:________ (填序号)。
A点燃A处酒精喷灯
B通入CO
C停止通入CO
D熄灭酒精喷灯
(4)实验装置图中虚线框内装置起到的作用有_________ (填序号)。
A收集一氧化碳
B吸收二氧化碳
C检验二氧化碳
(5)已知此反应过程中温度不同,可能生成铁的不同的氧化物。原固体Fe2O3质量为48.0g,现用热分析仪记录CO与Fe2O3进行反应时有关数据,得到固体质量与反应温度的关系曲线如下图所示:

根据图象分析,写出B点时固体成分的化学式_________ 。
【研究二】工业炼铁【装置如下图】

(1)焦炭是炼铁的重要原料之一,其作用有___________ 。
(2)炼铁高炉内发生的主要化学反应①的化学方程式为____________ 。
(3)“高炉气体”中除二氧化碳外,体积含量最多的气体是___________ 。
(4)为测定产物生铁中单质铁的质量分数,某兴趣小组取用10g生铁样品,把100g稀硫酸分四次加入样品中(假设样品中除单质铁外,其他成份不与硫酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下:
①从以上数据可知,第_________ 次生铁样品中的单质铁已完全反应。
②生铁样品中单质铁的质量分数=__________ 。
③所用稀硫酸的H2SO4质量分数。(列式计算)_______
【研究一】实验室模拟炼铁(装置如下图)。

已知:B装置中的液体为过量的氢氧化钠与氢氧化钙混合液,氢氧化钠吸收二氧化碳能力比氢氧化钙强。请回答下列问题:
(1)实验过程中A处玻璃管中的实验现象:
(2)写出B处反应的化学方程式:
(3)实验装置按图连接,请将以下四步按正确操作步骤排序:
A点燃A处酒精喷灯
B通入CO
C停止通入CO
D熄灭酒精喷灯
(4)实验装置图中虚线框内装置起到的作用有
A收集一氧化碳
B吸收二氧化碳
C检验二氧化碳
(5)已知此反应过程中温度不同,可能生成铁的不同的氧化物。原固体Fe2O3质量为48.0g,现用热分析仪记录CO与Fe2O3进行反应时有关数据,得到固体质量与反应温度的关系曲线如下图所示:

根据图象分析,写出B点时固体成分的化学式
【研究二】工业炼铁【装置如下图】

(1)焦炭是炼铁的重要原料之一,其作用有
(2)炼铁高炉内发生的主要化学反应①的化学方程式为
(3)“高炉气体”中除二氧化碳外,体积含量最多的气体是
(4)为测定产物生铁中单质铁的质量分数,某兴趣小组取用10g生铁样品,把100g稀硫酸分四次加入样品中(假设样品中除单质铁外,其他成份不与硫酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下:
| 稀硫酸的用量 | 剩余固体的质量 |
| 第一次加入25g | 7.2g |
| 第二次加入25g | 4.4g |
| 第三次加入25g | 1.6g |
| 第四次加入25g | 0.2g |
②生铁样品中单质铁的质量分数=
③所用稀硫酸的H2SO4质量分数。(列式计算)
您最近一年使用:0次
实验题
|
较难
(0.4)
解题方法
【推荐3】老师给了同学们一包红色粉末,该粉末可能是铜粉和氧化铁[Fe2O3]粉末中的一种或两种。同学们对该粉末的成分进行了研究。取该粉末 放入硬质玻璃管中,先通CO然后再用酒精喷灯加热一段时间,停止加热继续通入CO至装置冷却。实验装置如图:
放入硬质玻璃管中,先通CO然后再用酒精喷灯加热一段时间,停止加热继续通入CO至装置冷却。实验装置如图:

(1)实验时,先通CO再加热的目的是______ 。
(2)若该粉末全部是氧化铁,在硬质玻璃管中观察到的实验现象是______ ;其中发生反应的化学方程式为______ 。
(3)B装置是用于吸收二氧化碳并收集CO,其中盛放的试剂应该是______。
(4)若该粉末为铜粉和氧化铁的混合物,待装置完全冷却至室温,称量硬质玻璃管内剩余固体的质量为 。则
。则 的取值范围是
的取值范围是______ 。
(5)如果没有装置B、C,该实验造成的危害是______ 。
 放入硬质玻璃管中,先通CO然后再用酒精喷灯加热一段时间,停止加热继续通入CO至装置冷却。实验装置如图:
放入硬质玻璃管中,先通CO然后再用酒精喷灯加热一段时间,停止加热继续通入CO至装置冷却。实验装置如图:
(1)实验时,先通CO再加热的目的是
(2)若该粉末全部是氧化铁,在硬质玻璃管中观察到的实验现象是
(3)B装置是用于吸收二氧化碳并收集CO,其中盛放的试剂应该是______。
| A.澄清石灰水 | B.稀盐酸 | C.水 |
 。则
。则 的取值范围是
的取值范围是(5)如果没有装置B、C,该实验造成的危害是
您最近一年使用:0次
实验题
|
较难
(0.4)
解题方法
【推荐1】绿矾(FeSO4﹒nH2O)是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。绿矾不稳定,加热时会失去结晶水生成硫酸亚铁,硫酸亚铁在空气中易被氧化。某化学兴趣小组为测定绿矾中结晶水的含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。称重B装置,记为n1g。(已知碱石灰是氧化钙和氢氧化钠的混合物)

实验步骤如下:
Ⅰ.打开K1和K2,缓缓通入N2一段时间后连接好装置,关闭K1
Ⅱ.点燃酒精灯,加热一段时间
Ⅲ.熄灭酒精灯
Ⅳ…………,称量A的质量为m3g,称量B的质量为n2g
回答下列问题:
(1)步骤Ⅳ中“……………。”的具体操作是_______ 。
(2)装置B中发生反应的化学方程式为_______ 。
(3)根据实验记录,如只选择装置A的数据计算绿矾中结晶水的质量分数为_______ (列式表示)。
(4)如选择实验前后B装置数据计算,则装置C的作用是_______ 。若两组数据的计算结果都偏小,则可能的共同原因是_______ 。

实验步骤如下:
Ⅰ.打开K1和K2,缓缓通入N2一段时间后连接好装置,关闭K1
Ⅱ.点燃酒精灯,加热一段时间
Ⅲ.熄灭酒精灯
Ⅳ…………,称量A的质量为m3g,称量B的质量为n2g
回答下列问题:
(1)步骤Ⅳ中“……………。”的具体操作是
(2)装置B中发生反应的化学方程式为
(3)根据实验记录,如只选择装置A的数据计算绿矾中结晶水的质量分数为
(4)如选择实验前后B装置数据计算,则装置C的作用是
您最近一年使用:0次
实验题
|
较难
(0.4)
解题方法
【推荐2】同学们对一包干燥的红色粉末氧化铁的含量进行测定。请你参与并回答有关问题。称取该粉末5.0g装入硬质玻璃管中,按下图在通风橱中进行实验。开始时缓缓通入CO气体,过一段时间后再加热使其充分反应。待反应完全后,停止加热,继续通CO气体至玻璃管冷却。反应前后称量相关装置和物质的总质量,其数据如下表(假定粉末中的杂质不参加反应,也不发生变化):

【交流讨论】
(1)开始实验时,在A装置中应_____ (选序号“a.先通CO,排尽空气”“b.先加热红色粉末”)。
(2)选择①组的实验数据计算来确定红色粉末中氧化铁的质量分数是_____ %,造成②组洗气瓶和瓶中物质的总质量增加量过小的原因是(写一点) _____ 。
(3)实验中观察到A装置反应管中的现象为_____ 。
(4)为了防止溶液倒吸,本实验停止加热前_____ (填“需要”或“不需要”)先断开A和B的连接处。本实验中,为达到测定氧化铁含量的目的,可以用 _____ 代替CO气体。
【反思评价】从环保角度看,该实验装置设计上不足之处是_____ 。

| 反应前 | 反应后 | |
| ①组 | 玻璃管和红色粉末的总质量为37.5g | 玻璃管和固体物质的总质量为36.3g |
| ②组 | 洗气瓶和所盛溶液的总质量为180.0g | 洗气瓶和瓶中物质的总质量为180.1g |
(1)开始实验时,在A装置中应
(2)选择①组的实验数据计算来确定红色粉末中氧化铁的质量分数是
(3)实验中观察到A装置反应管中的现象为
(4)为了防止溶液倒吸,本实验停止加热前
【反思评价】从环保角度看,该实验装置设计上不足之处是
您最近一年使用:0次
实验题
|
较难
(0.4)
【推荐3】我国提出2060年前实现碳中和。体现了构建人类命运共同体的大国担当。实现碳中和人人有责。为了减少CO2排放;同学们决定从我做起,在进行“木炭还原氧化铜”实验时进行了装置设计改进;改进前和改进后装置如下图所示。______ ;装置B用于吸收反应生成的CO2。
(2)同学们通过查阅资料了解到上述实验中还会产生少量的CO,于是同学们按下图所示增加小气球以此完善实验装置。小气球的作用是______ 。______ 处(填“A”或“B”)黑色粉末变红;则说明木炭还原氧化铜实验中产生了CO。
第一步:先用氦气排除装置内的空气(如下图所示);______ (填“只有CO2”“只有CO”或“既有CO2又有CO”)。
(5)由上述结论并结合质量守恒定律分析;木炭还原氧化铜的实验中试管中固体减少的质量______ (填“等于”或“不等于”)澄清石灰水增加的质量。
本实验结束后,同学们在老师的带领下通过查阅大量文献资料,还定量探究了木炭还原氧化铜的实验中生成CO的多少与木炭和氧化铜的质量配比有关系。

(2)同学们通过查阅资料了解到上述实验中还会产生少量的CO,于是同学们按下图所示增加小气球以此完善实验装置。小气球的作用是


第一步:先用氦气排除装置内的空气(如下图所示);



(5)由上述结论并结合质量守恒定律分析;木炭还原氧化铜的实验中试管中固体减少的质量
本实验结束后,同学们在老师的带领下通过查阅大量文献资料,还定量探究了木炭还原氧化铜的实验中生成CO的多少与木炭和氧化铜的质量配比有关系。
您最近一年使用:0次



