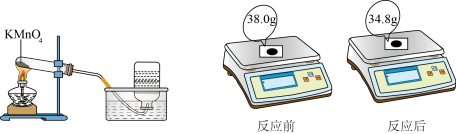
若用分液漏斗替换装置E中的长颈漏斗,则有如下图的氧气发生装置。
取34g过氧化氢溶液于分液漏斗A中,向B中加入一定量的二氧化锰,活塞K保持打开。不同时间电子天平的读数如下表所示(不考虑 逸出):
逸出):
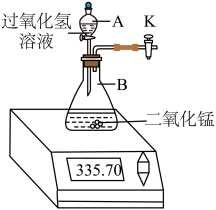
请根据要求回答下列问题:
①生成氧气的物质的量为_______mol;
②完全反应后B中水的质量为_______克;
③根据上述氧气的量计算参加反应的过氧化氢的物质的量(根据化学方程式列式计算)。
取34g过氧化氢溶液于分液漏斗A中,向B中加入一定量的二氧化锰,活塞K保持打开。不同时间电子天平的读数如下表所示(不考虑
 逸出):
逸出):| 反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 装置+过氧化氢溶液+二氧化锰/g | 335.70 | 333.78 | 332.64 | 332.58 | 332.50 | 332.50 | 332.50 |

请根据要求回答下列问题:
①生成氧气的物质的量为_______mol;
②完全反应后B中水的质量为_______克;
③根据上述氧气的量计算参加反应的过氧化氢的物质的量(根据化学方程式列式计算)。
更新时间:2020-12-29 13:26:29
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】为了制作叶脉书签,需要配制125g10%的NaOH溶液。
(l)计算需要称取 NaOH 的质量;
(2)将洗净的树叶放在配制好的溶液中煮沸后取出,称量发现溶液的质量减少了5g,溶质质量分数也有所减小。为了测定剩下溶液中NaOH的质量分数,向溶液中逐渐加入7.3%的稀盐酸,当溶液pH=7时,消耗盐酸50g。计算:
①生成NaCl的质量;
②剩下溶液中NaOH的质量分数;
③刚好完全反应时溶液中溶质的质量分数。(写出计算过程,精确到0.1%)
(l)计算需要称取 NaOH 的质量;
(2)将洗净的树叶放在配制好的溶液中煮沸后取出,称量发现溶液的质量减少了5g,溶质质量分数也有所减小。为了测定剩下溶液中NaOH的质量分数,向溶液中逐渐加入7.3%的稀盐酸,当溶液pH=7时,消耗盐酸50g。计算:
①生成NaCl的质量;
②剩下溶液中NaOH的质量分数;
③刚好完全反应时溶液中溶质的质量分数。(写出计算过程,精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】为测定久置于空气中的氢氧化钠样品的变质程度,某化学活动小组称取该固体样品10g放入锥形瓶中,加水溶解,配成50g溶液,再向锥形瓶中滴加稀硫酸,反应过程中产生气体质量的部分实验数据和锥形瓶中溶液质量变化的如下表所示,求10g样品中碳酸钠的质量分数。
| 加入稀硫酸的质量/g | 40 | 65 | 75 |
| 产生气体的质量/g | 1.1 | 2.2 | 2.2 |
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】宏观和微观相联系是化学认识物质和学习的独特思维方式。
(1)某化合物由碳、氢两种元素组成,这两种元素的质量比为3:1,该化合物的化学式量为16,它的化学式为______ 。
(2)两个微粒的质量比等于其相对质量比。一个碳-12原子的质量为1.993×10-26Kg,一个水分子的相对分子质量为18,则一个水分子的质量为______ Kg(只写出计算式即可)。
(3)宏观物质的质量与微观粒子数存在一定的内在联系,人们发现6.02×1023Kg个C-12原子的质量数值上等于其相对原子质量,单位为克。即6.02×1023个C-12原子的质量为12g。化学上将6.02×1023称为阿伏加德罗常数,而含有阿伏加德罗常数个微粒的物质规定为1摩尔。则1摩尔水的质量为______ g。
(1)某化合物由碳、氢两种元素组成,这两种元素的质量比为3:1,该化合物的化学式量为16,它的化学式为
(2)两个微粒的质量比等于其相对质量比。一个碳-12原子的质量为1.993×10-26Kg,一个水分子的相对分子质量为18,则一个水分子的质量为
(3)宏观物质的质量与微观粒子数存在一定的内在联系,人们发现6.02×1023Kg个C-12原子的质量数值上等于其相对原子质量,单位为克。即6.02×1023个C-12原子的质量为12g。化学上将6.02×1023称为阿伏加德罗常数,而含有阿伏加德罗常数个微粒的物质规定为1摩尔。则1摩尔水的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】过氧乙酸是一种常用的消毒剂,其化学式为CH3COOOH;其摩尔质量为______ ;其中C、H原子的物质的量比为______ ;0.5mol过氧乙酸中约含有______ 个氢原子。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】资料:①水的化学式为 H2O,表示每个水分子由两个氢原子和一个氧原子构成; 二氧化碳的化学式为 CO2;碳、氢、氧原子的相对原子质量分别为 12、1、16。
②化学上有一种能将微观粒子数目与宏观物质质量联系起来的量,叫物质的量,其单位是摩尔。1 摩尔任何物质中含有构成它的微粒个数都是 6.02×1023 个,1 摩尔任何物质的质量是 以克为单位,数值上都等于该物质的化学式中各原子的相对原子质量的总和。例如 1 摩尔水的各种量关系如图。

计算:
(1)1 摩尔水的水分子中氢原子数目是________ 个;
(2)1 摩尔水的水分子中各原子的总数目是___________ 个;
(3)1 摩尔二氧化碳的质量为____________ g。
②化学上有一种能将微观粒子数目与宏观物质质量联系起来的量,叫物质的量,其单位是摩尔。1 摩尔任何物质中含有构成它的微粒个数都是 6.02×1023 个,1 摩尔任何物质的质量是 以克为单位,数值上都等于该物质的化学式中各原子的相对原子质量的总和。例如 1 摩尔水的各种量关系如图。

计算:
(1)1 摩尔水的水分子中氢原子数目是
(2)1 摩尔水的水分子中各原子的总数目是
(3)1 摩尔二氧化碳的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】硫酸铜溶液对过氧化氢的分解有催化作用。实验室里利用如图实验装置制取氧气,锥形瓶中先加入10. 0%的硫酸铜溶液33.6 g,然后将分液漏斗中的溶质质量分数为5. 0%的过氧化氢溶液68.0 g逐滴滴入,使过氧化氢完全分解。
(1)硫酸铜在上述化学反应前后质量______ (填“变”或“不变”)。
(2)求反应后锥形瓶内溶液中溶质的质量分数。(结果精确到0.1%)

(1)硫酸铜在上述化学反应前后质量
(2)求反应后锥形瓶内溶液中溶质的质量分数。(结果精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组为测定实验室中一瓶久置的过氧化氢溶液中溶质的质量分数,实验测得相关数据如下图所示:

(1)剩余的混合物中二氧化锰的质量为 g,二氧化锰在反应中的作用是 ,反应生成氧气的质量为 g。
(2)计算该过氧化氢溶液中溶质的质量。
(3)计算该过氧化氢溶液中溶质的质量分数。

(1)剩余的混合物中二氧化锰的质量为 g,二氧化锰在反应中的作用是 ,反应生成氧气的质量为 g。
(2)计算该过氧化氢溶液中溶质的质量。
(3)计算该过氧化氢溶液中溶质的质量分数。
您最近一年使用:0次