回答下列问题。
(1)从硝酸钾、少量氯化钠和不溶性杂质(泥沙)的混合物中得到硝酸钾的流程如下:
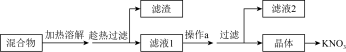
①结合图表分析,趁热过滤的原因是________________ 。
②操作a的名称是___________ 。
③滤液2的溶质是____________ 。
(2)A~D为初中化学常见物质,A、D都是金属,且A的颜色呈紫红色,D为银白色贵重金属,在常温下通过下图所示转化可获取硝酸钾。回答下列问题。
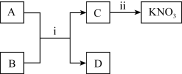
①B物质是_______________ 。
②反应i能发生的原因是_______________ 。
③反应i的化学方程式是________________ ,该反应所属的基本反应类型是____________ 。
④ 若只用一步操作实现反应ii,能否加入氯化钾?_____ (填“能”或“不能”)。说明理由:_________________________ 。
(1)从硝酸钾、少量氯化钠和不溶性杂质(泥沙)的混合物中得到硝酸钾的流程如下:

| 温度/℃ | 0 | 20 | 40 | 60 | 80 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| KN03 | 13.3 | 31.6 | 63.9 | 110 | 169 | |
②操作a的名称是
③滤液2的溶质是
(2)A~D为初中化学常见物质,A、D都是金属,且A的颜色呈紫红色,D为银白色贵重金属,在常温下通过下图所示转化可获取硝酸钾。回答下列问题。

①B物质是
②反应i能发生的原因是
③反应i的化学方程式是
④ 若只用一步操作实现反应ii,能否加入氯化钾?
更新时间:2021-02-03 11:22:25
|
相似题推荐
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】化学兴趣小组的同学在实验室利用硫酸铜溶液、稀硫酸、硝酸钡溶液、碳酸钠溶液、氢氧化钠溶液,将溶液两两混合判断能否发生反应。
(1)写出一个有白色沉淀生成的化学方程式。
(2)写出上述能发生反应但没有明显现象的一组物质的化学式。
(3)写出复分解反应中,生成物应具备的条件。
(1)写出一个有白色沉淀生成的化学方程式。
(2)写出上述能发生反应但没有明显现象的一组物质的化学式。
(3)写出复分解反应中,生成物应具备的条件。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】根据碱的四条化学性质回答下列问题:

(1)X的种类应该属于______ ,③反应的基本类型是______ 。
(2)若碱为氢氧化钙,请写出一个符合④反应的化学方程式______ ,该反应之所以能够发生是因为______ 。
(3)利用性质②,可以选择氢氧化钠溶液来吸收有害气体二氧化硫,请写出发生反应的化学方程式______ 。

(1)X的种类应该属于
(2)若碱为氢氧化钙,请写出一个符合④反应的化学方程式
(3)利用性质②,可以选择氢氧化钠溶液来吸收有害气体二氧化硫,请写出发生反应的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某工厂废液中含有氯化钠,氯化铜和氯化亚铁,某课外小组要从废液中回收铜并得到铁红(主要成分Fe2O3),要求全过程不引入其他金属元素,设计实验方案如图所示:

【查阅资料】不溶性的碱受热时都会分解而且一般都会分解为金属氧化物和水。回答下列问题:
(1)加入过量A溶解后,再进行操作a时玻璃棒的作用是_______ 。
(2)工厂废液中加入过量A反应的化学方程式为_______ 。
(3)溶液甲中的金属离子是_______ (写离子符号)。
(4)步骤①②③中所发生的化学反应,其中属于置换反应的是_______ (填序号)。
(5)写出反应⑤的化学方程式_______ 。

【查阅资料】不溶性的碱受热时都会分解而且一般都会分解为金属氧化物和水。回答下列问题:
(1)加入过量A溶解后,再进行操作a时玻璃棒的作用是
(2)工厂废液中加入过量A反应的化学方程式为
(3)溶液甲中的金属离子是
(4)步骤①②③中所发生的化学反应,其中属于置换反应的是
(5)写出反应⑤的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】Fe(OH)3可用于制造医药、颜料等,其胶体可用于净水。某化学兴趣小组利用废铁屑来制备Fe(OH)3粉末的流程如下:
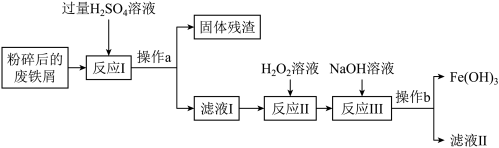
资料:①废铁屑主要为表面附有大量铁锈的铁。
②Fe(OH)3难溶于水,加热时会分解生成氧化铁和水。
③H2O2溶液可以将Fe2+氧化成Fe3+。
(1)操作a的名称为_______ 。
(2)滤液I中除了 外,还存在着的离子是
外,还存在着的离子是_______ 。(写离子符号)
(3)反应I中,需要_______ g20%的H2SO4溶液才能与5.6g铁恰好完全反应。

资料:①废铁屑主要为表面附有大量铁锈的铁。
②Fe(OH)3难溶于水,加热时会分解生成氧化铁和水。
③H2O2溶液可以将Fe2+氧化成Fe3+。
(1)操作a的名称为
(2)滤液I中除了
 外,还存在着的离子是
外,还存在着的离子是(3)反应I中,需要
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】从废旧手机的某些部件中可以回收银和铜,其操作流程如图所示。

(1)将废旧部件粉碎处理的目的是_______ 。
(2)操作a的名称是_______ 。
(3)步骤①发生反应的化学方程式为___ (写一个即可),步骤②加入硝酸银的目的是___ 。
(4)金属M是从硝酸铜溶液中得到铜,该金属可以是_______ (填化学式,一种即可)

(1)将废旧部件粉碎处理的目的是
(2)操作a的名称是
(3)步骤①发生反应的化学方程式为
(4)金属M是从硝酸铜溶液中得到铜,该金属可以是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】硫酸锌可制备各种含锌材料,在防腐、医学上有很多应用。菱锌矿的主要成分是ZnCO3,还含有少量的二氧化硅和氧化铁。以菱锌矿为原料制备ZnSO4·7H2O的工艺流程如下图所示(二氧化硅难溶于水,也不与稀硫酸反应):____________________ 。
(2)滤液1中含有的阳离子是H+和______ (填离子符号)。
(3)“转化”中加入足量锌粉,反应的化学方程式有Zn+Fe2(SO4)3=ZnSO4+2FeSO4和__________________ (任写一个)。
(4)下列说法正确的是____(填字母)。

(2)滤液1中含有的阳离子是H+和
(3)“转化”中加入足量锌粉,反应的化学方程式有Zn+Fe2(SO4)3=ZnSO4+2FeSO4和
(4)下列说法正确的是____(填字母)。
| A.“粉碎”是为了使菱锌矿在“酸浸”中与稀硫酸充分反应 |
| B.滤渣甲、滤渣乙均能与稀硫酸反应产生气体 |
| C.滤液2的质量一定比滤液1的质量大 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】下表是硝酸钾和氯化铵在不同温度时的溶解度。分析表中数据,回答问题。
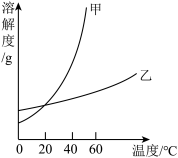
(1)上图中,甲可表示___ (填化学式)的溶解度曲线。
(2)40℃时,两种物质的饱和溶液中,溶质质量分数较小的是__ (填化学式)。
(3)20℃时,按下图所示操作,B中溶液的溶质与溶剂质量比为_____ (填最简整数比);C中的溶液是__ (填“饱和”或“不饱和”)溶液。

(4)60℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到60℃,剩余溶液的质量:硝酸钾溶液__ (填“>”“<”或“=”)氯化铵溶液。
(5)室温下,将盛有硝酸钾的饱和溶液的试管放入盛有水的烧杯中,再向烧杯内的水中加入一定量的硝酸铵并搅拌,试管内可以观察到的现象是____ 。
| 温度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | 硝酸钾 | 13.3 | 31.6 | 63.9 | 110 |
| 氯化铵 | 29.4 | 37.2 | 45.8 | 55.2 | |

(1)上图中,甲可表示
(2)40℃时,两种物质的饱和溶液中,溶质质量分数较小的是
(3)20℃时,按下图所示操作,B中溶液的溶质与溶剂质量比为

(4)60℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到60℃,剩余溶液的质量:硝酸钾溶液
(5)室温下,将盛有硝酸钾的饱和溶液的试管放入盛有水的烧杯中,再向烧杯内的水中加入一定量的硝酸铵并搅拌,试管内可以观察到的现象是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】下列数据是硝酸钾固体在不同温度时的溶解度。
(1)硝酸钾溶液中的溶剂是__ 。
(2)20℃时,向100克水中加入31.6克硝酸钾,充分溶解后得到__ (填“饱和”或“不饱和”)溶液。
(3)如图所示,小烧杯中盛放的是述(2)中所得到的硝酸钾溶液。若将少量的下列物质分别小心地加入到大烧杯的水中。不断搅拌,一定能够使小烧杯中有固体析出的是__ (填字母)

A 冰 B 浓硫酸 C 硝酸铵 D 冰 E 氢氧化钠 F 氧化钙
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(1)硝酸钾溶液中的溶剂是
(2)20℃时,向100克水中加入31.6克硝酸钾,充分溶解后得到
(3)如图所示,小烧杯中盛放的是述(2)中所得到的硝酸钾溶液。若将少量的下列物质分别小心地加入到大烧杯的水中。不断搅拌,一定能够使小烧杯中有固体析出的是

A 冰 B 浓硫酸 C 硝酸铵 D 冰 E 氢氧化钠 F 氧化钙
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】葡萄糖(C6H12O6)是生命活动中不可缺少的物质,它在人体内能直接参与新陈代谢过程。某化学小组的同学对葡萄糖进行以下研究。
(1)葡萄糖由______ 种元素组成,各元素的质量之比为_______ 。
(2)小组的同学分别对葡萄糖在水和乙醇中的溶解性进行探究,实验结果如图。说明葡萄糖的溶解性与______ 有关。

(3)甲同学对某样品中葡萄糖的含量进行测定,原理: 。则X的化学式为
。则X的化学式为_____ 。
实验一 配制葡萄糖溶液
(4)临床发现,用10%的葡萄糖溶液与10~20 mL25%的硫酸镁溶液混合配成药水可以治疗支气管哮喘。

①正确的实验操作顺序是______ (填序号)。
Aebacd B. eabcd C. ecbda D. ecadb
②配制500mL溶质质量分数为10%的葡萄糖溶液(密度1.04g/mL),需要葡萄糖的质量___ g。
实验二 配制硫酸镁溶液
(5)下表为硫酸镁的部分溶解度数据。配制硫酸镁溶液时温度要控制在20°C以上。请结合表中数据分析原因______ 。
(1)葡萄糖由
(2)小组的同学分别对葡萄糖在水和乙醇中的溶解性进行探究,实验结果如图。说明葡萄糖的溶解性与

(3)甲同学对某样品中葡萄糖的含量进行测定,原理:
 。则X的化学式为
。则X的化学式为实验一 配制葡萄糖溶液
(4)临床发现,用10%的葡萄糖溶液与10~20 mL25%的硫酸镁溶液混合配成药水可以治疗支气管哮喘。

①正确的实验操作顺序是
Aebacd B. eabcd C. ecbda D. ecadb
②配制500mL溶质质量分数为10%的葡萄糖溶液(密度1.04g/mL),需要葡萄糖的质量
实验二 配制硫酸镁溶液
(5)下表为硫酸镁的部分溶解度数据。配制硫酸镁溶液时温度要控制在20°C以上。请结合表中数据分析原因
| 温度l℃ | 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 |
| 溶解度/g | 22 | 24.8 | 27.7 | 30.5 | 33.3 | 36.4 | 39.3 | 41.8 |
您最近一年使用:0次



