氧化钠和硝酸钾两种物质的溶解度曲线如下图所示,回答下列问题:

(1)由图可知,氯化钠___________(填“易”、“可”、“微”或“难”)溶于水。
(2)图中两种物质的溶解度曲线有一个交点A,点A的含义是___________。
(3)22℃时,向50.0g水中加入15.0g硝酸钾,充分溶解后,所得溶液是___________(填“饱和”或“不饱和”)溶液,当温度升高到60℃时(不考虑水分蒸发),溶液的溶质量分数___________(填“变大”、“变小”或“不变”)。
(4)22℃时,100.0g10%的氯化钠溶液中加入多少克氯化钠恰好可以形成饱和溶液(计算结果保留至0.1g)?
(5)硝酸钾溶液可作为无土栽培的营养液。已知12%的硝酸钾溶液的密度为1.12g/cm3,若要配制224.0g溶质质量分数为3%的硝酸钾溶液,需要量取12%的硝酸钾溶液多少毫升(计算结果保留至0.1mL)?

(1)由图可知,氯化钠___________(填“易”、“可”、“微”或“难”)溶于水。
(2)图中两种物质的溶解度曲线有一个交点A,点A的含义是___________。
(3)22℃时,向50.0g水中加入15.0g硝酸钾,充分溶解后,所得溶液是___________(填“饱和”或“不饱和”)溶液,当温度升高到60℃时(不考虑水分蒸发),溶液的溶质量分数___________(填“变大”、“变小”或“不变”)。
(4)22℃时,100.0g10%的氯化钠溶液中加入多少克氯化钠恰好可以形成饱和溶液(计算结果保留至0.1g)?
(5)硝酸钾溶液可作为无土栽培的营养液。已知12%的硝酸钾溶液的密度为1.12g/cm3,若要配制224.0g溶质质量分数为3%的硝酸钾溶液,需要量取12%的硝酸钾溶液多少毫升(计算结果保留至0.1mL)?
更新时间:2021-03-21 08:48:27
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】如图是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线。请回答下列问题。

(1)若将丙的饱和溶液从t3 ℃降温到t2 ℃时,一定会发生改变的是_____(填序号)。
a.溶解度 b.溶质的质量 c.溶质的质量分数
(2)分别将甲、乙、丙三种物质的饱和溶液各100 g从t3 ℃降到t2 ℃,降温后甲、乙、丙三种溶液的溶剂质量由大到小的顺序是__________________。
(3)t3 ℃时甲的饱和溶液的溶质质量分数是_____________(计算结果精确到0.1%)。

(1)若将丙的饱和溶液从t3 ℃降温到t2 ℃时,一定会发生改变的是_____(填序号)。
a.溶解度 b.溶质的质量 c.溶质的质量分数
(2)分别将甲、乙、丙三种物质的饱和溶液各100 g从t3 ℃降到t2 ℃,降温后甲、乙、丙三种溶液的溶剂质量由大到小的顺序是__________________。
(3)t3 ℃时甲的饱和溶液的溶质质量分数是_____________(计算结果精确到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】住在华北地区盐碱湖边的人们常常“冬天捞碱(碳酸钠),夏天晒盐(氯化钠)”。实验小组的同学们想测出捞出的“碱”中碳酸钠的质量分数,于是称取6g样品于烧杯中,并取稀盐酸200g,平均分成4份,依次加入样品中(样品中的其他成分不与稀盐酸反应),充分反应后,称取了剩余混合物的总质量,结果如下:
请完成下列分析及计算:
(1)“冬天捞碱”的原理是_____ (选填“降温”或“蒸发”)结晶。
(2)m=_____ 。
(3)计算捞出的“碱”中碳酸钠的质量分数。(写出解答过程,结果精确到0.1%)
| 实验次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| 剩余混合物的总质量/g | 55 | 104 | 153.8 | m |
(1)“冬天捞碱”的原理是
(2)m=
(3)计算捞出的“碱”中碳酸钠的质量分数。(写出解答过程,结果精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】人类的生活和生产也离不开水。
(一)某同学配制60g溶质质量分数为5%的NaCl溶液,准备了下列实验用品,回答下列问题:

(1)配制溶液过程中还缺少了一种玻仪器是_________(填名称)
(2)计算配制60g溶质质量分数为5%的NaCl溶液所需氯化钠的质量是______。
(3)用量筒来量取所需的水(水的密度为1g/cm),量筒的规格_____(从下列中选用10mL、25mL、50mL、100mL);该同学如果采用如下图中观察方式___量取液体(填A、B、C),会导致配制的溶液中溶质的反量分数偏大。

(二)请根据下图中a、b、c三种物质的溶解度曲线,回答下列问题:

(1)t1℃时,a、h、c三种物溶解度的的大小关系是______;
(2t2℃时,30ga物厉力入到50g水中不断搅拌,溶液的质量是_______g;
(3)现有接近饱和的c的溶液,要使它变成饱和溶液,可以采用的方法是________(填一种即可)
(4)将t2℃时的a、b、c二种物质的饱和溶液降温到t1℃,溶液中溶质质量分数最小的是_(填物质序号)
(一)某同学配制60g溶质质量分数为5%的NaCl溶液,准备了下列实验用品,回答下列问题:

(1)配制溶液过程中还缺少了一种玻仪器是_________(填名称)
(2)计算配制60g溶质质量分数为5%的NaCl溶液所需氯化钠的质量是______。
(3)用量筒来量取所需的水(水的密度为1g/cm),量筒的规格_____(从下列中选用10mL、25mL、50mL、100mL);该同学如果采用如下图中观察方式___量取液体(填A、B、C),会导致配制的溶液中溶质的反量分数偏大。

(二)请根据下图中a、b、c三种物质的溶解度曲线,回答下列问题:

(1)t1℃时,a、h、c三种物溶解度的的大小关系是______;
(2t2℃时,30ga物厉力入到50g水中不断搅拌,溶液的质量是_______g;
(3)现有接近饱和的c的溶液,要使它变成饱和溶液,可以采用的方法是________(填一种即可)
(4)将t2℃时的a、b、c二种物质的饱和溶液降温到t1℃,溶液中溶质质量分数最小的是_(填物质序号)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】硝酸钾在不同温度下的溶解度如表:
(1)30℃时,把15.8g硝酸钾完全溶解在50g水中,所得硝酸钾溶液的质量分数为_____。
(2)步骤(1)所得的溶液中至少需要加入_____克硝酸钾才能饱和。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
| 溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.8 |
(2)步骤(1)所得的溶液中至少需要加入_____克硝酸钾才能饱和。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
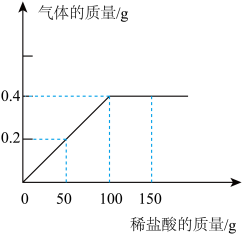
【推荐2】在一定温度下,向100g水中依次加入一定质量的KC1固体,充分溶解,加入KCl固体的质量与所得溶液质量的关系如图所示:_______ 溶液(填“饱和”或“不饱和”)。
(2)实验③所得溶液中溶质的质量分数是_______ (写出计算过程)
(3)现有溶质质量分数为10%的KC1的溶液300g,若配制成溶质质量分数为3%的KCl的溶液,问需要加水的质量是多少。(写出计算过程)

(2)实验③所得溶液中溶质的质量分数是
(3)现有溶质质量分数为10%的KC1的溶液300g,若配制成溶质质量分数为3%的KCl的溶液,问需要加水的质量是多少。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】现有300g溶质质量分数为10%的氯化钠溶液,
(1)若蒸发掉150克水,溶液中溶质质量分数为___________?
(2)若要使此溶液的溶质质量分数变成20% ,需向溶液中加入___________氯化钠?
(3)若要使此溶液的溶质质量分数变成5% ,需向溶液中加入___________水?
(1)若蒸发掉150克水,溶液中溶质质量分数为___________?
(2)若要使此溶液的溶质质量分数变成20% ,需向溶液中加入___________氯化钠?
(3)若要使此溶液的溶质质量分数变成5% ,需向溶液中加入___________水?
您最近一年使用:0次
【推荐2】如图为某品牌过氧化氢溶液说明书,,用该品牌过氧化氢溶液配制600g10%的过氧化氢溶液用于消毒,请回答下列问题:
(1)溶质(H2O2)的相对分子质量_____________。
(2)溶质(H2O2)中氢、氧元素质量比为_____________。
(3)600g10%的过氧化氢溶液中含有_____________g溶质,配置时需要加入__________g水进行稀释。
过氧化氢溶液说明书 【药品名称】过氧化氢溶液 【成分】化学式:H2O2 【注意事项】本品遇光、热易分解变质 【溶质质量分数】30% 【净含量】500mL 【贮藏】遮光、密闭、在阴凉处(不超过20℃)保存。 |
(2)溶质(H2O2)中氢、氧元素质量比为_____________。
(3)600g10%的过氧化氢溶液中含有_____________g溶质,配置时需要加入__________g水进行稀释。
您最近一年使用:0次

 。
。

