下图1是实验室模拟炼铁的装置图,试回答:
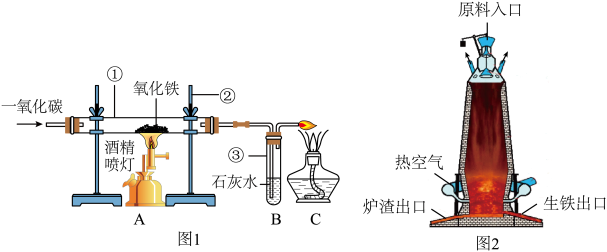
(1)实验过程玻璃管中发生反应的现象是______ ,发生反应的化学方程式是______ 。
(2)在实验过程中,先要通入一氧化碳气体一段时间,其目的是______ 。
(3)该实验装置存在问题,请指出问题之处:______ 。
(4)图2是工业生产中炼铁高炉的结构图。实际生产中炼铁的原料铁矿石、焦炭、石灰石是从原料入口加入,其中焦炭在高炉炼铁时的作用是______ 。
(5)取少量高炉中炼出的生铁放入烧杯中,加入足量稀盐酸,当反应停止后,还可观察到烧杯底部有黑色不溶物,该物质主要是______ (填化学式)。
(6)某钢铁公司用490万吨含氧化铁60%的赤铁矿石炼铁,所得到的生铁中最多含铁多少万吨?______ (写出计算过程)

(1)实验过程玻璃管中发生反应的现象是
(2)在实验过程中,先要通入一氧化碳气体一段时间,其目的是
(3)该实验装置存在问题,请指出问题之处:
(4)图2是工业生产中炼铁高炉的结构图。实际生产中炼铁的原料铁矿石、焦炭、石灰石是从原料入口加入,其中焦炭在高炉炼铁时的作用是
(5)取少量高炉中炼出的生铁放入烧杯中,加入足量稀盐酸,当反应停止后,还可观察到烧杯底部有黑色不溶物,该物质主要是
(6)某钢铁公司用490万吨含氧化铁60%的赤铁矿石炼铁,所得到的生铁中最多含铁多少万吨?
更新时间:2021-04-04 21:19:33
|
相似题推荐
综合应用题
|
适中
(0.65)
解题方法
【推荐1】人类历史发展的不同阶段曾以不同金属材料的使用作为标志。

(1)金、银在自然界有单质形式存在,说明他们的化学性质都_________ (填“不活泼”或“活泼”)。
(2)工业上常以赤铁矿石(主要成分是氧化铁)为原料炼铁,请写出一氧化碳与氧化铁反应的化学方程式:______________ 。
(3)钛和钛合金是21世纪的重要的金属材料。钛合金制品放在海水中数年,取出后仍光亮如新,是因为其_______________ (填字母序号)非常好。
A可塑性 B机械性能 C抗腐蚀性能
(4)利用“活泼金属”可以制得H2,H2可用作汽车能源。若推广应用于汽车产业,则需综合考虑的因素有________________ (填字母序号)。
A金属原料的成本 B生成过程中的能耗和污染 C金属的回收利用
(5)黄铜是铜和锌的合金。某化学兴趣小组的同学为了测定某黄铜样品中铜的质量分数,取20g该黄铜样品粉末放入烧杯中,向其中加入100g稀硫酸,恰好完全反应。反应后烧杯中剩余物的总质量为119.8g。试求:
①反应产生氢气的质量是___________ g。
②该黄铜样品中铜的质量分数。(写出计算过程)____

(1)金、银在自然界有单质形式存在,说明他们的化学性质都
(2)工业上常以赤铁矿石(主要成分是氧化铁)为原料炼铁,请写出一氧化碳与氧化铁反应的化学方程式:
(3)钛和钛合金是21世纪的重要的金属材料。钛合金制品放在海水中数年,取出后仍光亮如新,是因为其
A可塑性 B机械性能 C抗腐蚀性能
(4)利用“活泼金属”可以制得H2,H2可用作汽车能源。若推广应用于汽车产业,则需综合考虑的因素有
A金属原料的成本 B生成过程中的能耗和污染 C金属的回收利用
(5)黄铜是铜和锌的合金。某化学兴趣小组的同学为了测定某黄铜样品中铜的质量分数,取20g该黄铜样品粉末放入烧杯中,向其中加入100g稀硫酸,恰好完全反应。反应后烧杯中剩余物的总质量为119.8g。试求:
①反应产生氢气的质量是
②该黄铜样品中铜的质量分数。(写出计算过程)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】现有以下三个实验,请回答问题

(1)图中实验A是探究二氧化碳的溶解性实验。二氧化碳是否可以溶于水,很难直接观察到现象,可以通过______________ 的现象来间接感知。
(2)图中实验B探究铁锈蚀条件的装置。调节L端与R端的液面高度一致,塞紧木塞,一周后观察,L端液面_________ 填“高于”、“低于”或者“等于”)R端液面,说明铁生锈与_____ 、_________ 等物质有关。
(3)图中实验C是实验室用“一氧化碳还原氧化铁”的实验,实验结束后称得石灰水增重4.4g,则整个实验过程中实际消耗CO的量_____ (填“大于”、“小于”或者“等于”)2.8g,尾气处理方法为______ 。

(1)图中实验A是探究二氧化碳的溶解性实验。二氧化碳是否可以溶于水,很难直接观察到现象,可以通过
(2)图中实验B探究铁锈蚀条件的装置。调节L端与R端的液面高度一致,塞紧木塞,一周后观察,L端液面
(3)图中实验C是实验室用“一氧化碳还原氧化铁”的实验,实验结束后称得石灰水增重4.4g,则整个实验过程中实际消耗CO的量
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】2021年3月2日C919大型客机全球首单“落地”东航,迈出商业成功重要一步。先进材料首次在国产客机大规模使用,其中第三代铝锂合金材料在C919机体结构中的用量达到8.8%。
(1)下列客机上使用的物品中,属于合成材料的是______(填序号)。
(2)客机上常提供以下食物:瘦肉、青菜、面包、米饭、鱼排、饮用水等,其中富含蛋白质的是______ 。客机上提供的饮用水可用______ 判断它是硬水还是软水。
(3)铁铜等其他金属材料在飞机上也有应用。已知工业上炼铁炼钢和轧制钢材的主要流程如下图:

①写出高炉用磁铁矿炼铁的化学反应方程式______ 。
②炼铁的固体原料需经过粉碎,其目的是______ 。
③热空气和高炉气体的主要成分有一种相同,这种气体的名称是______ 。
④生铁转化为钢的过程中纯氧的作用是______ 。
(1)下列客机上使用的物品中,属于合成材料的是______(填序号)。
| A.合金门把手 | B.塑料桌板 | C.涤沦窗帘 | D.羊毛毯子 |
(2)客机上常提供以下食物:瘦肉、青菜、面包、米饭、鱼排、饮用水等,其中富含蛋白质的是
(3)铁铜等其他金属材料在飞机上也有应用。已知工业上炼铁炼钢和轧制钢材的主要流程如下图:

①写出高炉用磁铁矿炼铁的化学反应方程式
②炼铁的固体原料需经过粉碎,其目的是
③热空气和高炉气体的主要成分有一种相同,这种气体的名称是
④生铁转化为钢的过程中纯氧的作用是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】金属与人类的生产、生活密切相关,牢记掌握金属的知识非常重要。
(1)下列用途是利用金属导电性的是______ (填字母)。
A作导线 B金作戒指 C铝合金做门窗 D铁锅做炊具
(2)如图是化学小组探究铁钉锈蚀条件的实验,要达到实验目的还需补充__________ 实验?
(3)在实验室里,可以利用如图装置制得铁。
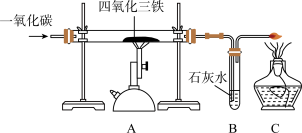
①A处玻璃管内所发生反应的化学方程为________________ 。
②B处可观察到的现象是____________ ;C处酒精灯的作用是_____________ 。
(4)向一定量的硝酸银、硝酸铝和硝酸铜的混合溶液中加入一定量的锌,溶液质量与加入锌的质量关系如图。请回答:

①写出a点所发生反应的化学方程式__________ 。
②d 点对应的溶液中的金属离子有哪些__________ ?
(5)为了测定铜锌合金样品中锌的含量,称取样品20g于烧杯中,向其中加入100g稀硫酸至恰好完全反应,反应后烧杯中物质的总质量为119.6g。请计算:样品中锌的质量分数__________ 。
(1)下列用途是利用金属导电性的是
A作导线 B金作戒指 C铝合金做门窗 D铁锅做炊具
(2)如图是化学小组探究铁钉锈蚀条件的实验,要达到实验目的还需补充

(3)在实验室里,可以利用如图装置制得铁。

①A处玻璃管内所发生反应的化学方程为
②B处可观察到的现象是
(4)向一定量的硝酸银、硝酸铝和硝酸铜的混合溶液中加入一定量的锌,溶液质量与加入锌的质量关系如图。请回答:

①写出a点所发生反应的化学方程式
②d 点对应的溶液中的金属离子有哪些
(5)为了测定铜锌合金样品中锌的含量,称取样品20g于烧杯中,向其中加入100g稀硫酸至恰好完全反应,反应后烧杯中物质的总质量为119.6g。请计算:样品中锌的质量分数
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】金属及合金有广泛的用途。请运用所学知识回答下列问题:
(1)铝的利用比铜和铁晚。金属大规模开发和利用的先后顺序与下列___________ 有关。
甲、金属的活动性 乙、金属的导电性 丙、金属在地壳中的含量
(2)Al在高温条件下可以与Fe3O4发生置换反应,其反应的化学方程式为___________ ;单质铁可以和硫酸铁溶液反应生成硫酸亚铁,化学反应方程式为___________ 。
(3)取一定量的Al放入Cu(NO3)2和AgNO3的混合溶液中充分反应后过滤,得到固体和蓝色滤液。则固体中可能存在的金属是___________ ;该过程中一定发生的化学方程式为___________ 。
(4)实验室可通过以下简单实验模拟工业炼铁的基本原理:
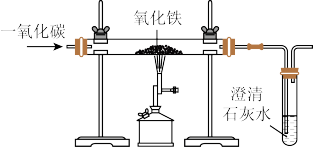
①请写出玻璃管中出现的现象:___________ 。
②从环保角度分析,该装置有明显的缺陷,你认为应该如何改进?___________
③某同学用一氧化碳还原氧化铁的实验装置以赤铁矿为原料来冶炼生铁。试计算冶炼2000t含杂质2%的生铁,需要含氧化铁80%的赤铁矿石的质量是多少___________ ?
(1)铝的利用比铜和铁晚。金属大规模开发和利用的先后顺序与下列
甲、金属的活动性 乙、金属的导电性 丙、金属在地壳中的含量
(2)Al在高温条件下可以与Fe3O4发生置换反应,其反应的化学方程式为
(3)取一定量的Al放入Cu(NO3)2和AgNO3的混合溶液中充分反应后过滤,得到固体和蓝色滤液。则固体中可能存在的金属是
(4)实验室可通过以下简单实验模拟工业炼铁的基本原理:

①请写出玻璃管中出现的现象:
②从环保角度分析,该装置有明显的缺陷,你认为应该如何改进?
③某同学用一氧化碳还原氧化铁的实验装置以赤铁矿为原料来冶炼生铁。试计算冶炼2000t含杂质2%的生铁,需要含氧化铁80%的赤铁矿石的质量是多少
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】金属与人类的生产、生活密切相关,牢固掌握金属的知识非常重要。
(1)铝和铁都是我们生活中常见的金属,铝耐腐蚀性能比铁好的原因是_____ 。
(2)如图是一氧化碳还原氧化铁的实验装置,请回答下列问题。

①玻璃管A中的实验现象是_____ 。
②实验开始时,先通入一氧化碳的原因是_____ 。
③从环保角度考虑,还需对以上装置进行改进,请简述改进措施_______ 。
(3)为了验证Fe、Cu、Ag三种金属的活动性顺序,请你写出两种可行方案所需的物质。
方案一:_______
方案二:_______
(4)若除去FeCl2溶液中杂质CuCl2,请写出有关的化学方程式。_____
(5)实验室在高温条件下,用足量一氧化碳还原10g赤铁矿,充分反应后,测得生成的纯铁的质量为5.6g。则该赤铁矿中氧化铁的质量分数是_____ 。
(1)铝和铁都是我们生活中常见的金属,铝耐腐蚀性能比铁好的原因是
(2)如图是一氧化碳还原氧化铁的实验装置,请回答下列问题。

①玻璃管A中的实验现象是
②实验开始时,先通入一氧化碳的原因是
③从环保角度考虑,还需对以上装置进行改进,请简述改进措施
(3)为了验证Fe、Cu、Ag三种金属的活动性顺序,请你写出两种可行方案所需的物质。
方案一:
方案二:
(4)若除去FeCl2溶液中杂质CuCl2,请写出有关的化学方程式。
(5)实验室在高温条件下,用足量一氧化碳还原10g赤铁矿,充分反应后,测得生成的纯铁的质量为5.6g。则该赤铁矿中氧化铁的质量分数是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】金属和金属材料与人类的生产和生活密切相关。
(1)制作USB数据线要用到铁、制等材料。这主要是利用了铁、钢的_____ 性(填“导电”或“导热”)。
(2)铝合金中主要含有铝、镁、铁三种金属,为验证这三种金属的活动性瓶序,某同学设计如图3个实验。请你写出能发生反应的化学方程式:_____ 。

另一位同学认为实验乙和丙都可以省去。你的看法是_____ (填字母)。
A 乙、丙都可以省去
B 乙、丙都不能省去
C 内可以省去,乙不能省
D 乙可以省去,丙不能省
(3)高铁的高速运行离不开铁轨,建造铁轨所需要的钢铁通常用还原铁矿石制得。工业上用赤铁矿(主要成分为Fe2O3)与一氧化碳反应来炼铁。若制得5.6t铁,理论上需要含氧化铁80%的赤铁矿石_____ 。
实验室利用一氧化碳还原氧化铁的装置中,a处看到的现象_____ ,澄清清石灰水的作用是_____ 。
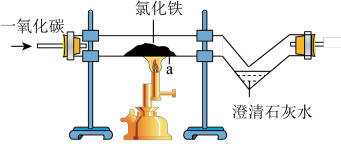
请从环境保护角度指出此实验存在的缺陷:_____ 。
(4)某废弃物只含铜和氧化铜。查阅资料知道,氧化铜能与稀盐酸反应生成氯化铜和水,某生设计了如下实验流程回收金属铜。
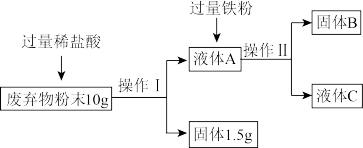
请回答下列问题:
①操作1的名称是_____ 。液体C由H2O和_____ (填化学式)组成。
②将过量铁粉加到液体A中,会发生的反应的化学方程式:_____ 。
③理论上,这个实验能回收到铜粉_____ g。
(1)制作USB数据线要用到铁、制等材料。这主要是利用了铁、钢的
(2)铝合金中主要含有铝、镁、铁三种金属,为验证这三种金属的活动性瓶序,某同学设计如图3个实验。请你写出能发生反应的化学方程式:

另一位同学认为实验乙和丙都可以省去。你的看法是
A 乙、丙都可以省去
B 乙、丙都不能省去
C 内可以省去,乙不能省
D 乙可以省去,丙不能省
(3)高铁的高速运行离不开铁轨,建造铁轨所需要的钢铁通常用还原铁矿石制得。工业上用赤铁矿(主要成分为Fe2O3)与一氧化碳反应来炼铁。若制得5.6t铁,理论上需要含氧化铁80%的赤铁矿石
实验室利用一氧化碳还原氧化铁的装置中,a处看到的现象

请从环境保护角度指出此实验存在的缺陷:
(4)某废弃物只含铜和氧化铜。查阅资料知道,氧化铜能与稀盐酸反应生成氯化铜和水,某生设计了如下实验流程回收金属铜。

请回答下列问题:
①操作1的名称是
②将过量铁粉加到液体A中,会发生的反应的化学方程式:
③理论上,这个实验能回收到铜粉
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】化学是以实验为基础的科学。
(1)如图,将注射器中的溶液缓缓推入V形管,反应的化学方程式为______ ;用80℃的热水加热盛有红磷和白磷的W形管时,发现白磷燃烧而红磷不燃烧,由此可说明燃烧需要的条件是______ 。

(2)请根据下列各图中有关信息回答问题:
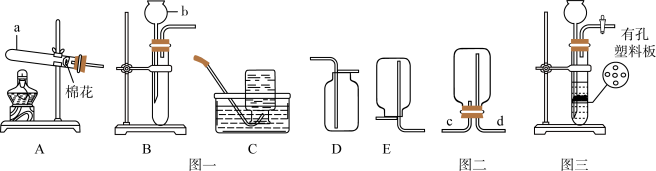
①从图一A到E中选择实验室制取二氧化碳的装置______ (填标号);若将其改为图三的发生装置,与原装置相比,其优点是______ ;若将其改为如图二的收集装置,气体应从______ (填“c”或“d”)端通入。
②写出用A装置制取氧气的化学方程式______ ;酒精灯内酒精完全燃烧的化学方程式______ 。
(3)某炼铁厂要得到2240t铁,请你根据化学方程式计算:理论上需要含氧化铁80%的赤铁矿的质量是多少?
(1)如图,将注射器中的溶液缓缓推入V形管,反应的化学方程式为

(2)请根据下列各图中有关信息回答问题:

①从图一A到E中选择实验室制取二氧化碳的装置
②写出用A装置制取氧气的化学方程式
(3)某炼铁厂要得到2240t铁,请你根据化学方程式计算:理论上需要含氧化铁80%的赤铁矿的质量是多少?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】如图甲是实验室模拟炼铁的装置图,试回答:

(1)按如图连接实验装置、检查装置气密性、装药品、固定实验装置后,主要实验步骤有:①通入一氧化碳;②停止通入一氧化碳;③点燃酒精喷灯;④熄灭酒精喷灯;⑤验纯。正确的操作顺序是__________ (填序号)。
(2)实验过程中仪器①中发生的反应的现象是____________ ,反应的化学方程式是___________ 。
(3)实验过程中产生的尾气不能直接排放的原因是____________________ 。
(4)图乙是工业生产中炼铁高炉的结构图。实际生产中炼铁的原料铁矿石、焦炭、石灰石是从原料入口加入的,其中焦炭在高炉炼铁时的作用是____________________ 。
(5)若用1440t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是__________ t。

(1)按如图连接实验装置、检查装置气密性、装药品、固定实验装置后,主要实验步骤有:①通入一氧化碳;②停止通入一氧化碳;③点燃酒精喷灯;④熄灭酒精喷灯;⑤验纯。正确的操作顺序是
(2)实验过程中仪器①中发生的反应的现象是
(3)实验过程中产生的尾气不能直接排放的原因是
(4)图乙是工业生产中炼铁高炉的结构图。实际生产中炼铁的原料铁矿石、焦炭、石灰石是从原料入口加入的,其中焦炭在高炉炼铁时的作用是
(5)若用1440t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】某校课外活动小组的同学在老师的帮助下,探究用赤铁矿(主要成分是Fe2O3)炼铁的主要反应原理。他们设计的实验装置如下图所示。
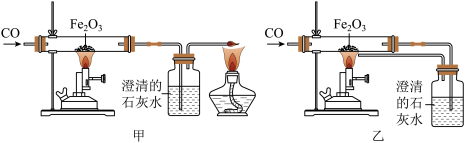
(1)写出一氧化碳还原氧化铁的化学方程式___________ 。
(2)实验中在甲装置中观察到的实验现象___________ 。
(3)甲装置中,设置酒精灯的目的___________ ,实验时应先点燃___________ 灯。
(4)乙装置与甲装置相比,它的主要优点是___________ 。
(5)为测定某生铁(铁碳合金)样品中碳的质量分数,小军同学取5.8g生铁样品盛放在烧杯中,并向其中加入100g稀盐酸,恰好完全反应后烧杯内剩余物质的总质量为105.6g。请分析并计算:
①生成氢气的质量为___________ g;
②生铁样品中碳的质量分数。_______ (结果精确到0.1%)

(1)写出一氧化碳还原氧化铁的化学方程式
(2)实验中在甲装置中观察到的实验现象
(3)甲装置中,设置酒精灯的目的
(4)乙装置与甲装置相比,它的主要优点是
(5)为测定某生铁(铁碳合金)样品中碳的质量分数,小军同学取5.8g生铁样品盛放在烧杯中,并向其中加入100g稀盐酸,恰好完全反应后烧杯内剩余物质的总质量为105.6g。请分析并计算:
①生成氢气的质量为
②生铁样品中碳的质量分数。
您最近一年使用:0次
【推荐2】通过对有机物的学习,我们知道甲烷密度小于空气,难溶于水,具有可燃性。同学们对甲烷继续进行如下探究:

探究I:甲烷的制取
【查阅资料】实验室加热无水醋酸钠和碱石灰(NaOH和CaO)固体混合物制取甲烷。
(1)仪器a的名称______ 。
(2)制取甲烷的发生装置应选______ (填大写字母),选用装置C收集甲烷时气体应从______ (填小写字母,后同)端进入,如果选择装置D收集,其中装满水,气体应从______ 端进入。
探究Ⅱ:甲烷的组成元素
(3)验纯后点燃甲烷,在火焰上方罩一冷而干燥的烧杯(见装置E),烧杯内壁有______ 生成,向烧杯中倒入少量澄清石灰水,振荡,现象为______ 。由此推断,甲烷中一定含C、H两种元素。
(4)点燃甲烷先将甲烷气体通过盛有______ 的洗气瓶,目的是______ 。
(5)隔绝空气对甲烷加强热得到两种单质,请写出该反应的化学方程式______ 。
探究Ⅲ:甲烷的化学性质
【提出问题】通过以上探究,甲烷除了具有可燃性、能分解外,还具有什么化学性质?
【查阅资料】①无水硫酸铜粉末遇水由白色变蓝色,②甲烷具有还原性。
【进行实验】该同学按如图装置进行实验:
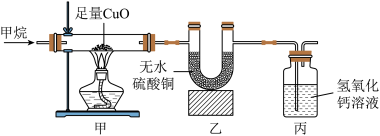
【现象与结论】
现象:甲中黑色固体变为红色,乙中无水硫酸铜变为蓝色,丙中澄清石灰水变浑浊。
结论:甲烷具有还原性。
(6)根据实验现象,写出甲烷还原氧化铜的化学方程式:______ 。
【反思与评价】
(7)加热前,要先向装置中通入一段时间的氮气,再通入甲烷。其目的是______ 。
(8)考虑到甲烷在甲装置中难以完全反应,应该在丙装置后加装尾气处理装置,你的建议是______ (写一点即可)

探究I:甲烷的制取
【查阅资料】实验室加热无水醋酸钠和碱石灰(NaOH和CaO)固体混合物制取甲烷。
(1)仪器a的名称
(2)制取甲烷的发生装置应选
探究Ⅱ:甲烷的组成元素
(3)验纯后点燃甲烷,在火焰上方罩一冷而干燥的烧杯(见装置E),烧杯内壁有
(4)点燃甲烷先将甲烷气体通过盛有
(5)隔绝空气对甲烷加强热得到两种单质,请写出该反应的化学方程式
探究Ⅲ:甲烷的化学性质
【提出问题】通过以上探究,甲烷除了具有可燃性、能分解外,还具有什么化学性质?
【查阅资料】①无水硫酸铜粉末遇水由白色变蓝色,②甲烷具有还原性。
【进行实验】该同学按如图装置进行实验:

【现象与结论】
现象:甲中黑色固体变为红色,乙中无水硫酸铜变为蓝色,丙中澄清石灰水变浑浊。
结论:甲烷具有还原性。
(6)根据实验现象,写出甲烷还原氧化铜的化学方程式:
【反思与评价】
(7)加热前,要先向装置中通入一段时间的氮气,再通入甲烷。其目的是
(8)考虑到甲烷在甲装置中难以完全反应,应该在丙装置后加装尾气处理装置,你的建议是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】钢铁在生产生活中有广泛应用。
I.实验室模拟炼铁
(1)实验室模拟炼铁的装置如图所示。

①仪器 a 的名称是______ 。
②实验中澄清石灰水出现白色浑浊的原因是______ (用化学方程式表示)。
③尾气的处理方法是______ 。
II.工业炼铁方式
(2)一种工业炼铁方法如图所示。
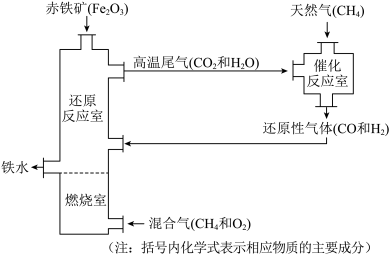
①催化反应室中,CH4与 CO2 或 H2O 在高温下均能发生反应,产物相同,写出相应的化学方程式:______ 。
②流程中 CH4除产生还原性气体外,还有的作用是______ 。
③某钢铁公司用 800 万吨含氧化铁 60%的赤铁矿炼铁,最多能得到含杂质 4%的生铁多少万吨?(写出计算过程)______ 。
I.实验室模拟炼铁
(1)实验室模拟炼铁的装置如图所示。

①仪器 a 的名称是
②实验中澄清石灰水出现白色浑浊的原因是
③尾气的处理方法是
II.工业炼铁方式
(2)一种工业炼铁方法如图所示。

①催化反应室中,CH4与 CO2 或 H2O 在高温下均能发生反应,产物相同,写出相应的化学方程式:
②流程中 CH4除产生还原性气体外,还有的作用是
③某钢铁公司用 800 万吨含氧化铁 60%的赤铁矿炼铁,最多能得到含杂质 4%的生铁多少万吨?(写出计算过程)
您最近一年使用:0次



