研究“水”可从多角度展开。
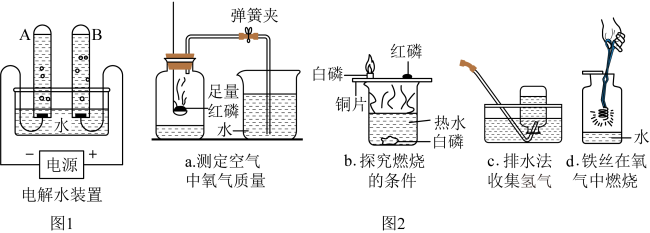
(1)水的电解
按图1所示装置,通电一段时间后,试管A和B中产生气体的体积比约为___________ 。
(2)水的性质:将黄豆大小的金属钾放入盛有水的烧杯中,在反应后的溶液中摘入酚酞试液,溶液变红。
(3)水的用途
①碘与锌在常温下反应速度很慢,若滴入几滴水则反应剧烈,水在此的作用是___________ 。
②图2实验中,对水的主要作用分析不全面的是___________ (填字母)。
A a图中的水通过水体积的变化得出空气中氧气的体积
B b图中的水提供热量
C c图集气瓶中的水排尽空气且便于观察H2何时集满
D d图中的水防止熔融物炸裂集气瓶
③写出图2中d图的化学方程式___________ 。
(4)水与溶液
根据所给氯化钠和碳酸钠的溶解度及溶解度曲线的信息,回答下列问题:
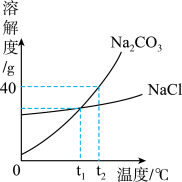
①20℃时,NaCl的溶解度是___________ g。
②t2℃时,将40g Na2CO3固体加入50g水中,充分溶解后所得Na2CO3溶液中溶质与溶剂的质量比为___________ 。
③若Na2CO3中混有少量的NaCl,提纯Na2CO3应采取的方法是___________ (填“降温结晶”或“蒸发结晶”)。

(1)水的电解
按图1所示装置,通电一段时间后,试管A和B中产生气体的体积比约为
(2)水的性质:将黄豆大小的金属钾放入盛有水的烧杯中,在反应后的溶液中摘入酚酞试液,溶液变红。
(3)水的用途
①碘与锌在常温下反应速度很慢,若滴入几滴水则反应剧烈,水在此的作用是
②图2实验中,对水的主要作用分析不全面的是
A a图中的水通过水体积的变化得出空气中氧气的体积
B b图中的水提供热量
C c图集气瓶中的水排尽空气且便于观察H2何时集满
D d图中的水防止熔融物炸裂集气瓶
③写出图2中d图的化学方程式
(4)水与溶液
根据所给氯化钠和碳酸钠的溶解度及溶解度曲线的信息,回答下列问题:

| 温度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| 氯化钠溶解度/g | 35 | 35.5 | 36 | 36.5 | 37 |
| 碳酸钠溶解度/g | 6 | 10 | 18 | 36.5 | 50 |
②t2℃时,将40g Na2CO3固体加入50g水中,充分溶解后所得Na2CO3溶液中溶质与溶剂的质量比为
③若Na2CO3中混有少量的NaCl,提纯Na2CO3应采取的方法是
更新时间:2021-03-15 18:16:23
|
相似题推荐
【推荐1】2022 年世界水日的主题是“珍惜地下水,珍惜隐藏的资源”,生活生产中我们都离不开水。
(1)地下水不可直接饮用,需要经过自来水厂的处理。自来水厂常用______ 来除去色素和异味。
(2)纯水导电能力很弱,电解水时常加入一些 NaOH 增强导电性,以加快电解速率。
①如图是电解水一段时间后的实验示意图:将水槽内液体中及试管内a、b处物质中一定存在的微观粒子的种类在图中画出______ (需画出粒子的数目比关系,水分子不用画)。

②电解过程中,水槽内液体的 pH______ (填“不变”或“变大”或“变小”)。
(3)某实验小组为研究影响电解水速率的因素做了如下实验,实验记录结果如下:
① 比较实验 a、c 可得出结论:______ 。
② 根据对实验 a、b、c 数据的分析,实验 d 的时间 t 最有可能是______ (填序号)。
A.35.4 B.37.8 C.50.2 D.55.6
(4)硬水在加热或长久放置时会形成水垢。水垢的主要成分是 CaCO3和 Mg(OH)2。某同学取水垢样品进行加热,加热过程中剩余固体的质量随加热时间的变化如图所示:

【查阅资料】氢氧化镁受热易分解,生成两种氧化物;碳酸钙则需要更高的温度才可以分解。
① 根据水垢的成分可知,水垢的产生是因为水中含有较多______ (填离子符号)等金属离子。
② b 点剩余固体成分为______ (填化学式)。
③ 根据图中数据计算在 d 点分解的物质的分解百分率=______ 。(分解百分率=已分解的物质的质量/分解前该物质的总质量×100%)
(1)地下水不可直接饮用,需要经过自来水厂的处理。自来水厂常用
(2)纯水导电能力很弱,电解水时常加入一些 NaOH 增强导电性,以加快电解速率。
①如图是电解水一段时间后的实验示意图:将水槽内液体中及试管内a、b处物质中一定存在的微观粒子的种类在图中画出

②电解过程中,水槽内液体的 pH
(3)某实验小组为研究影响电解水速率的因素做了如下实验,实验记录结果如下:
| 实验编号 | 电压(V) | 温度(℃) | NaOH溶液浓度 | H2体积(mL) | O2体积(mL) | 时间(s) |
| a | 6 | 15 | 2% | 20 | 9.8 | 54.0 |
| b | 6 | 15 | 5% | 20 | 9.8 | 36.2 |
| c | 6 | 30 | 2% | 20 | 9.6 | 46.2 |
| d | 6 | 30 | 5% | 20 | 9.7 | t |
② 根据对实验 a、b、c 数据的分析,实验 d 的时间 t 最有可能是
A.35.4 B.37.8 C.50.2 D.55.6
(4)硬水在加热或长久放置时会形成水垢。水垢的主要成分是 CaCO3和 Mg(OH)2。某同学取水垢样品进行加热,加热过程中剩余固体的质量随加热时间的变化如图所示:

【查阅资料】氢氧化镁受热易分解,生成两种氧化物;碳酸钙则需要更高的温度才可以分解。
① 根据水垢的成分可知,水垢的产生是因为水中含有较多
② b 点剩余固体成分为
③ 根据图中数据计算在 d 点分解的物质的分解百分率=
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】水是生命之源,是“永远值得探究的物质”,人类从未停止过对水的研究。
(1)水曾被误认为是一种“元素”。1766年,英国化学家卡文迪许用锌和稀硫酸制得“可燃空气”,他所说的“可燃空气”成分是___________ (填化学式),得出“水是一个结合物而不是简单元素”的结论。
(2)1785年,拉瓦锡将水蒸气通过高温铁制枪管,将水转化为氢气,同时生成一种黑色物质(Fe3O4),上述反应的化学方程式为_________ 。
(3)水在实验室中应用也很广泛。

①下列实验中,对水的主要作用分析错误的是________ (填字母)
A. a 图中的水封住试管及导管中的空气,便于观察气泡冒出
B. b图的水排尽集气瓶中的空气且便于观察O2何时集满
C. c图中的水防止高温熔融物炸裂集气瓶
D. d图中的水加快集气瓶中气体冷却,缓冲集气瓶内的气压骤然升高
②e图试管A、B中收集到的气体质量比约为____________ ,课本上安排电解水实验的目的是____________ 。
(1)水曾被误认为是一种“元素”。1766年,英国化学家卡文迪许用锌和稀硫酸制得“可燃空气”,他所说的“可燃空气”成分是
(2)1785年,拉瓦锡将水蒸气通过高温铁制枪管,将水转化为氢气,同时生成一种黑色物质(Fe3O4),上述反应的化学方程式为
(3)水在实验室中应用也很广泛。

①下列实验中,对水的主要作用分析错误的是
A. a 图中的水封住试管及导管中的空气,便于观察气泡冒出
B. b图的水排尽集气瓶中的空气且便于观察O2何时集满
C. c图中的水防止高温熔融物炸裂集气瓶
D. d图中的水加快集气瓶中气体冷却,缓冲集气瓶内的气压骤然升高
②e图试管A、B中收集到的气体质量比约为
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐3】全方位认识水
(1)水的组成。某兴趣小组的同学对此进行了实验探究。

(提出问题)水是由什么组成的?
(查阅资料)通过电解水和点燃氢气证明燃烧产物的方法均可证明水的组成。
(设计实验)兴趣小组的同学设计了如图所示的实验来探究水的组成,其中图甲是电解水的实验装置,图乙实验是将电解水产生的氢气直接缓缓地通过装有足量碱石灰(可吸收水份干燥气体)的仪器c,并在导管口d处将气体点燃,然后把盛有冷水的烧杯置于如图乙所示的位置。
(实验与结论)
①图甲中玻璃管a和玻璃管b得到气体的体积比为____________ ;检验b管中产物的方法是_____________ 。
②图乙所示的实验过程中可以观察到的实验现象:导管口d处_____________ ;烧杯底部有_________________ 。
③写出实验甲中反应的文字表达式_____________ ;该反应属于________________ (填反应的基本类型) .
④实验甲中没有发生变化的微粒是____________ 和________________ (填微粒符号)。
⑤由以上探究可以得到的有关水的组成的结论是__________________ 。反思提升:由此,你还能得出的微观结论是_________________ (写一个) 。
⑥通过实验甲可以得出水具有的化学性质是:___________ ,保持这种性质的微粒是______________ (用模型表示) ;通过实验乙,可以得出氢气具有的化学性质是:_____________ ,保持这种性质的微粒是______________ (用模型表示)。空气中的氧气仍然保持其原来_____________ 的化学性质,从微观上看是因为____________ 。
(2)水的净化。传统水处理工艺------经典 “三部曲”(a过滤b消毒c沉降),被列为人类20世纪最重要的发明之一。为了提高水质,有些水厂增加了活性炭处理工序。《生活饮用水卫生标准》中,允许使用的消毒剂有Cl2,NH2Cl(一氯胺的化学式),O3,C1O2,水的总硬度(以CaCO3计)不超过450mg/L。
①“三部曲”正确的工艺顺序为___________ (填字母)。
②活性炭处理工艺中,活性炭的作用是__________________ 。
③若水中其他成分不含钙元素,根据水的总硬度可计算出水中钙元素不超过____________________ mg/L。人工沉降常用的絮凝剂有明矾[ ],明矾作絮凝剂是因为与水反应生成氢氧化铝(含有氢氧根离子OH-)胶状物。OH-与SO42-都是原子团,参考明矾化学式,写出氢氧化铝的化学式
],明矾作絮凝剂是因为与水反应生成氢氧化铝(含有氢氧根离子OH-)胶状物。OH-与SO42-都是原子团,参考明矾化学式,写出氢氧化铝的化学式_____________ 。
④一氯胺是国家新版生活饮用水卫生标准中新增的一种消毒剂,请你写出NH2Cl所代表的的宏观和微观的意义。
宏观:_____________________ ,_____________________ ;
微观:_____________________ ,_____________________ ;
自来水厂的净水过程___________________ (填“能”或“不能”)将硬水软化成软水。检验清水池中水是硬水还是软水可用的物质是____________________ 。
(3)水的拓展资料。
①在科研中,水也是一种常用的试剂。水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是______________ (填序号)。
A微粒的构成发生了改变
B微粒的化学性质发生了改变
C元素种类发生了改变
D与水分子比,水合离子的电子数发生了改变
②重水在核反应中作减速剂。一个重水分子由两个重氢原子和一个氧原子构成,一个重氢原子中有一个质子,相对原子量为2。则下列叙述正确的是____________ (填序号)。
A一个重水分子的相对分子质量是20
B重水和水的组成元素不同
C一个重氢原子核外有2个电子
D一个重氢原子核中有1个中子
(1)水的组成。某兴趣小组的同学对此进行了实验探究。

(提出问题)水是由什么组成的?
(查阅资料)通过电解水和点燃氢气证明燃烧产物的方法均可证明水的组成。
(设计实验)兴趣小组的同学设计了如图所示的实验来探究水的组成,其中图甲是电解水的实验装置,图乙实验是将电解水产生的氢气直接缓缓地通过装有足量碱石灰(可吸收水份干燥气体)的仪器c,并在导管口d处将气体点燃,然后把盛有冷水的烧杯置于如图乙所示的位置。
(实验与结论)
①图甲中玻璃管a和玻璃管b得到气体的体积比为
②图乙所示的实验过程中可以观察到的实验现象:导管口d处
③写出实验甲中反应的文字表达式
④实验甲中没有发生变化的微粒是
⑤由以上探究可以得到的有关水的组成的结论是
⑥通过实验甲可以得出水具有的化学性质是:
(2)水的净化。传统水处理工艺------经典 “三部曲”(a过滤b消毒c沉降),被列为人类20世纪最重要的发明之一。为了提高水质,有些水厂增加了活性炭处理工序。《生活饮用水卫生标准》中,允许使用的消毒剂有Cl2,NH2Cl(一氯胺的化学式),O3,C1O2,水的总硬度(以CaCO3计)不超过450mg/L。
①“三部曲”正确的工艺顺序为
②活性炭处理工艺中,活性炭的作用是
③若水中其他成分不含钙元素,根据水的总硬度可计算出水中钙元素不超过
 ],明矾作絮凝剂是因为与水反应生成氢氧化铝(含有氢氧根离子OH-)胶状物。OH-与SO42-都是原子团,参考明矾化学式,写出氢氧化铝的化学式
],明矾作絮凝剂是因为与水反应生成氢氧化铝(含有氢氧根离子OH-)胶状物。OH-与SO42-都是原子团,参考明矾化学式,写出氢氧化铝的化学式④一氯胺是国家新版生活饮用水卫生标准中新增的一种消毒剂,请你写出NH2Cl所代表的的宏观和微观的意义。
宏观:
微观:
自来水厂的净水过程
(3)水的拓展资料。
①在科研中,水也是一种常用的试剂。水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是
A微粒的构成发生了改变
B微粒的化学性质发生了改变
C元素种类发生了改变
D与水分子比,水合离子的电子数发生了改变
②重水在核反应中作减速剂。一个重水分子由两个重氢原子和一个氧原子构成,一个重氢原子中有一个质子,相对原子量为2。则下列叙述正确的是
A一个重水分子的相对分子质量是20
B重水和水的组成元素不同
C一个重氢原子核外有2个电子
D一个重氢原子核中有1个中子
您最近一年使用:0次
综合应用题
|
较难
(0.4)
名校
解题方法
【推荐1】磷酸二氢钾(KH2PO4)为白色粉末,置于空气中易潮解,常作为无土栽培营养液成分之一。如图1是KH2PO4(用A表示)的溶解度曲线图。图2是M、N两点代表的溶液相互转化的途径路线图(“ ”表示转化方向)。
”表示转化方向)。

(1)图1中M点的溶解度为______ 。
(2)图1中t3℃时,N点对应的溶液为______ (填“饱和溶液”或“不饱和溶液”)。图2中,采取“先加水至N点对应的溶质质量分数再升温到t3℃”这一措施来实现M→N转化的途径路线是______ (填序号)。
(3)磷酸二氢钾可以提高果实的结果率,磷酸二氢钾属于______ 肥料。
(4)实验室要配制图1中M点的饱和溶液100g,需磷酸二氢钾的质量为______ 。在配制过程中有同学提议,将称量和量取步骤对调,同学经讨论后认为该建议合理,理由是______ 。
(5)经检测,同学配制的溶液溶质质量分数偏小,可能的原因是______(填序号)。
 ”表示转化方向)。
”表示转化方向)。
(1)图1中M点的溶解度为
(2)图1中t3℃时,N点对应的溶液为
(3)磷酸二氢钾可以提高果实的结果率,磷酸二氢钾属于
(4)实验室要配制图1中M点的饱和溶液100g,需磷酸二氢钾的质量为
(5)经检测,同学配制的溶液溶质质量分数偏小,可能的原因是______(填序号)。
| A.溶解时烧杯内壁有水珠 |
| B.量取溶剂时,仰视读数 |
| C.装瓶时有少量溶液洒出 |
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】固体物质X饱和溶液的质量分数随温度的变化曲线如下图所示。

请回答下列问题:
(1)若将E点的溶液降温至30℃,所得溶液为____ (填“饱和”或“不饱和”)溶液。
(2)若将D点的溶液恒温蒸发溶剂时,D点将向____ 点移动(选填A~E)。
(3)若将50gA点的溶液降温至20℃,则溶液中析出X的质量为_____ 。
(4)30℃时,若要使mg质量分数为30%的X溶液变为36%,采用的方法可以是_____ (填序号)。
a 蒸发掉m/6g水
b 蒸发掉原溶液中溶剂质量的1/2
c 再溶解0.05mg的X粉末
d 加入1.2mg40%的X溶液

请回答下列问题:
(1)若将E点的溶液降温至30℃,所得溶液为
(2)若将D点的溶液恒温蒸发溶剂时,D点将向
(3)若将50gA点的溶液降温至20℃,则溶液中析出X的质量为
(4)30℃时,若要使mg质量分数为30%的X溶液变为36%,采用的方法可以是
a 蒸发掉m/6g水
b 蒸发掉原溶液中溶剂质量的1/2
c 再溶解0.05mg的X粉末
d 加入1.2mg40%的X溶液
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】“感知宇宙奥秘,放飞航天梦想”。中国空间站“天宫课堂”分别于2021年12月9日和2022年3月22日开讲,请回答下列问题。

(1)在空间站的建设中使用了钛和钛合金。钛元素在元素周期表中的相关信息如图1所示。
①钛元素的相对原子质量是_________ 。
②钛合金具有许多优良性能,其硬度_________ (填“大于”或“小于”)金属钛的硬度。
③空间站的太阳能电池在充电过程中的能量转化:太阳能→电能→_________ 。
(2)如图2“泡腾片实验”:航天员将半片泡腾片(含某种酸和碳酸氢钠)塞入一个蓝色水球里,水球里立即产生很多气泡。
①该气体的化学式是_________ 。
②碳酸氢钠俗称小苏打,生活中可用作_________ (举一例)。
(3)如图3“太空冰雪’实验”:实验中用到了过饱和醋酸钠溶液,它在太空中形成液体球态,用带有结晶核的绳子接触液球,它就会瞬间结冰,变成“冰球”,这个“冰球”其实是“热球”。

①过饱和醋酸钠溶液结晶过程_________ (填“放热”或“吸热”)。
②如图4是醋酸钠的溶解度曲线,下列说法正确的是_________ (填字母)。
A.常温下,醋酸钠易溶于水
B.40℃时,饱和醋酸钠溶液的溶质质量分数是65.6%
C.加水能使醋酸钠溶液从饱和变成不饱和
D.将A点的饱和溶液升温到60℃,溶质质量分数增大
(4)“在空间站里,氧气和二氧化碳是怎么循环的呢?”地面分课堂的同学问。空间站中的水、气整合循环系统利用“萨巴蒂尔反应”,将CO2转化为H2O,配合氧气生成系统实现O2的再生,流程如图5所示。

①在氧气生成系统中,运用电解水的方法制氧气,反应的化学方程式为_________ 。
②在萨巴蒂尔反应系统中,发生的反应为 ,则X的化学式为
,则X的化学式为_________ 。
③在流程图所示的物质转化中,进入氧气生成系统发生电解的水的质量_________ (填“大于”、“等于”或“小于”)萨巴蒂尔反应系统中生成水的质量。

(1)在空间站的建设中使用了钛和钛合金。钛元素在元素周期表中的相关信息如图1所示。
①钛元素的相对原子质量是
②钛合金具有许多优良性能,其硬度
③空间站的太阳能电池在充电过程中的能量转化:太阳能→电能→
(2)如图2“泡腾片实验”:航天员将半片泡腾片(含某种酸和碳酸氢钠)塞入一个蓝色水球里,水球里立即产生很多气泡。
①该气体的化学式是
②碳酸氢钠俗称小苏打,生活中可用作
(3)如图3“太空冰雪’实验”:实验中用到了过饱和醋酸钠溶液,它在太空中形成液体球态,用带有结晶核的绳子接触液球,它就会瞬间结冰,变成“冰球”,这个“冰球”其实是“热球”。

①过饱和醋酸钠溶液结晶过程
②如图4是醋酸钠的溶解度曲线,下列说法正确的是
A.常温下,醋酸钠易溶于水
B.40℃时,饱和醋酸钠溶液的溶质质量分数是65.6%
C.加水能使醋酸钠溶液从饱和变成不饱和
D.将A点的饱和溶液升温到60℃,溶质质量分数增大
(4)“在空间站里,氧气和二氧化碳是怎么循环的呢?”地面分课堂的同学问。空间站中的水、气整合循环系统利用“萨巴蒂尔反应”,将CO2转化为H2O,配合氧气生成系统实现O2的再生,流程如图5所示。

①在氧气生成系统中,运用电解水的方法制氧气,反应的化学方程式为
②在萨巴蒂尔反应系统中,发生的反应为
 ,则X的化学式为
,则X的化学式为③在流程图所示的物质转化中,进入氧气生成系统发生电解的水的质量
您最近一年使用:0次



