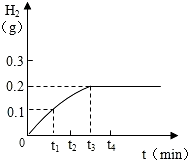
取Cu-Zn合金10g,将该合金放入烧杯中,向其中逐渐加入一定溶质质量分数的稀硫酸,所加稀硫酸与产生气体的质量关系如图所示。请计算:
(1)反应产生氢气的总质量 g。
(2)计算合金中铜的质量。
(3)计算稀硫酸的溶质质量分数。

(1)反应产生氢气的总质量 g。
(2)计算合金中铜的质量。
(3)计算稀硫酸的溶质质量分数。
更新时间:2021/04/12 11:10:15
|
相似题推荐
计算题
|
较易
(0.85)
解题方法
【推荐1】把5g Cu、Zn 混合物加入到盛有50g稀硫酸的烧杯中,恰好完全反应,反应后烧杯内物质的总质量为54.8g,求
(1)加入稀硫酸的过程中会看到什么现象_________________________
(2)产生H2_______ g?
(3)最后所得溶液中溶质的质量为多少?________
(1)加入稀硫酸的过程中会看到什么现象
(2)产生H2
(3)最后所得溶液中溶质的质量为多少?
您最近一年使用:0次
计算题
|
较易
(0.85)
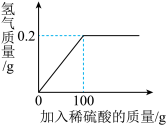
【推荐2】“黄铜”是铜锌合金,可塑性好,耐腐蚀,许多“金色”饰品就是用它来制作的。现称取20.0g黄铜样品置于烧杯中,慢慢加入稀硫酸使其充分反应,直至没有气泡产生为止,请结合下列图示计算。

(1)该20.0g黄铜样品中含锌的质量为____g。
(2)完全反应时生成硫酸锌的质量是______克。

(1)该20.0g黄铜样品中含锌的质量为____g。
(2)完全反应时生成硫酸锌的质量是______克。
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐1】工业上可以用黄铁矿(主要含FeS2,杂质不溶于水和酸)与稀硝酸反应来制取硫酸铁,作为净水剂。发生的化学反应方程式为: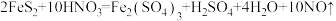 。为测定某黄铁矿中FeS2的含量,现取80g黄铁矿粉末于大烧杯,加入溶质质量分数为18%的稀硝酸至恰好完全反应,消耗700g稀硝酸。
。为测定某黄铁矿中FeS2的含量,现取80g黄铁矿粉末于大烧杯,加入溶质质量分数为18%的稀硝酸至恰好完全反应,消耗700g稀硝酸。
请回答下列问题:
(1)硫酸铁中铁元素的质量分数为________ ;
(2)若要配制上述浓度的稀硝酸1000g,需要60%的浓硝酸________ g来稀释。
(3)计算上述黄铁矿中FeS2的质量分数,大烧杯中所得溶液的质量。(写出计算过程)
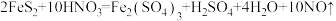 。为测定某黄铁矿中FeS2的含量,现取80g黄铁矿粉末于大烧杯,加入溶质质量分数为18%的稀硝酸至恰好完全反应,消耗700g稀硝酸。
。为测定某黄铁矿中FeS2的含量,现取80g黄铁矿粉末于大烧杯,加入溶质质量分数为18%的稀硝酸至恰好完全反应,消耗700g稀硝酸。请回答下列问题:
(1)硫酸铁中铁元素的质量分数为
(2)若要配制上述浓度的稀硝酸1000g,需要60%的浓硝酸
(3)计算上述黄铁矿中FeS2的质量分数,大烧杯中所得溶液的质量。(写出计算过程)
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】某化学兴趣小组的同学采集了一些大理石样品,为测定该样品中碳酸钙的质量分数,取样品6g粉碎成粉末状置于烧杯中,向其中加入10%的稀盐酸并不断搅拌,恰好不再有气泡产生时(已知杂质不与稀盐酸反应),共用去稀盐酸36.5g。
(1)计算样品中碳酸钙的质量分数。
(2)计算反应后所得溶液中溶质的质量分数?(结果保留到0.1%)
(1)计算样品中碳酸钙的质量分数。
(2)计算反应后所得溶液中溶质的质量分数?(结果保留到0.1%)
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐3】向 133.4 克稀盐酸中加入锌粉(杂质不溶于水也不溶于酸),所加锌粉的质量与产生气体的 质量的关系如下图所示。求:
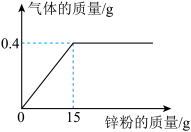
(1)该反应中化合价改变的元素是______ (填名称)。
(2)原稀盐酸中溶质的质量分数为多少?(结果精确到 0.1%)

(1)该反应中化合价改变的元素是
(2)原稀盐酸中溶质的质量分数为多少?(结果精确到 0.1%)
您最近一年使用:0次