海水是种宝贵资源.
(1)“海水晒盐”所采用的方法是________ .
A 冷却结晶 B 蒸发结晶 C 过滤
(2)海上航行缺乏饮用水时可用蒸馏法获得淡水.用该装置将2000g含氯化钠3%的海水暴晒4小时后,剩余海水中氯化钠的质量分数为4%,则收集到的可饮用水为________ g.
(3)海水中的硼酸(化学式为H3BO3)可用于玻璃工业,下表为硼酸的部分溶解度数据.
①60˚C时,100g硼酸饱和溶液中含有硼酸________ g(保留整数).
②某同学设计如下实验探究“温度”及“固体溶质的形态”对溶解速率的影响.三个烧杯中,所得溶液浓度的大小关系是________ (用“①”、“②”、“③”表示);
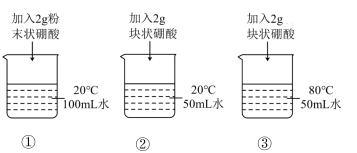
③若要达到实验目的,需改变实验①中的一个条件是________ (从以下选项中选择)
A 将20˚C的水改为80˚C B 将水的体积改为50mL C 将粉末状固体改为块状.
(1)“海水晒盐”所采用的方法是
A 冷却结晶 B 蒸发结晶 C 过滤
(2)海上航行缺乏饮用水时可用蒸馏法获得淡水.用该装置将2000g含氯化钠3%的海水暴晒4小时后,剩余海水中氯化钠的质量分数为4%,则收集到的可饮用水为
(3)海水中的硼酸(化学式为H3BO3)可用于玻璃工业,下表为硼酸的部分溶解度数据.
| 温度(˚C) | 0 | 20 | 40 | 60 | 80 |
| 溶解度(g/100g水) | 3 | 5 | 9 | 15 | 23 |
②某同学设计如下实验探究“温度”及“固体溶质的形态”对溶解速率的影响.三个烧杯中,所得溶液浓度的大小关系是

③若要达到实验目的,需改变实验①中的一个条件是
A 将20˚C的水改为80˚C B 将水的体积改为50mL C 将粉末状固体改为块状.
更新时间:2020-05-20 11:36:29
|
相似题推荐
【推荐1】甲、乙两种固体物质的溶解度曲线如下图所示。
(1)图中P点的含义是____________________________ 。
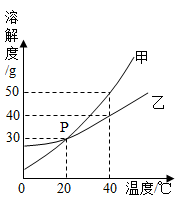
(2)40℃时,饱和溶液中溶质的质量分数:甲____ 乙(填“>”、“=”或“<”)。若将40℃的甲、乙的饱和溶液降温至15℃,则饱和溶液中溶质的质量分数:甲____ 乙(填“>”、“=”或“<”)。20℃时,将60 g乙物质放入100 g水中,升温至40℃,溶液中溶解的溶质与溶剂的质量比为__________ (用最简整数比表示)。
(3)20℃时,进行了如下图所示的实验:
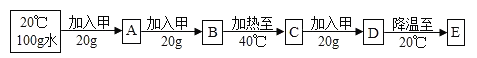
上述实验过程中所得的溶液,属于不饱和溶液的是________ (填序号,下同),________ 溶液与B溶液中溶质的质量分数相同。
(1)图中P点的含义是

(2)40℃时,饱和溶液中溶质的质量分数:甲
(3)20℃时,进行了如下图所示的实验:

上述实验过程中所得的溶液,属于不饱和溶液的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】请根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
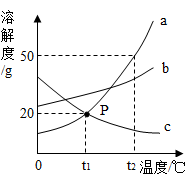
(1)P点的含义是_____ 。
(2)t2℃时,30g物质a加入到50g水中不断搅拌,得到物质a的_____ (填“饱和”或“不饱和”)溶液;此时溶液中溶质的质量分数是 _____ (精确到0.1%)。
(3)将t2℃时的a、b、c三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质量分数最小的是_____ 。
(4)物质a中含有少量的物质b,可采取_____ 的方法提纯a物质。

(1)P点的含义是
(2)t2℃时,30g物质a加入到50g水中不断搅拌,得到物质a的
(3)将t2℃时的a、b、c三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质量分数最小的是
(4)物质a中含有少量的物质b,可采取
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】如图是MgCl2、KCl、MgSO4的溶解度曲线。请回答:
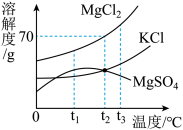
(1)t1℃时,三种物质溶解度的大小关系是____________ 。
(2)将t2℃时KCl和MgSO4的饱和溶液升温至t3℃时,所得溶液中溶质质量分数的关系是____________ 。
(3)t2℃时将100 g MgCl2加入150g水中充分溶解,欲得到t2℃时MgC12饱和溶液,可采取的方法有____________ (写一种)。
(4)将t3℃MgSO4的饱和溶液降温至t1℃时,实验现象为____________ 。

(1)t1℃时,三种物质溶解度的大小关系是
(2)将t2℃时KCl和MgSO4的饱和溶液升温至t3℃时,所得溶液中溶质质量分数的关系是
(3)t2℃时将100 g MgCl2加入150g水中充分溶解,欲得到t2℃时MgC12饱和溶液,可采取的方法有
(4)将t3℃MgSO4的饱和溶液降温至t1℃时,实验现象为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】(1)水是生命的源泉,为了人类社会的可持续发展,我们应该了解水的有关知识.
①节约用水是每个公民的义务,日常生活中你的节水措施是______________ 。
②天然水中含有许多杂质,自来水厂通常对天然水进行:沉淀、过滤、_______ 、消毒等处理,使之达到饮用水标准。
③鉴别软水和硬水常用的试剂是_________ 。
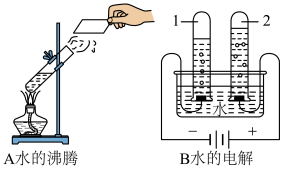
④如图所示的两个实验,探究结论:“水由氢元素和氧元素组成”的是实验_____ ;(填A或B)
(2)下列有关水的说法正确的是___________
①蒸馏能净化水,也能将水软化
②二氧化碳能溶于水,也能与水反应
③氧化钙能吸收空气中的水,也能与水反应
④水是最常用的溶剂,也是与生命密不可分的物质
(3)小红同学在实验室欲配制一定质量分数的食盐溶液。配制的步骤可以概括为计算、称量和量取、____ 、装瓶贴签。
(4)汽车、电动车一般使用铅酸蓄电池。某铅酸蓄电池使用的酸溶液是质量分数为20%的稀硫酸。
①用100g质量分数为98%的浓硫酸配制质量分数为20%的稀硫酸,需要水的质量是________ g。
②配制该稀硫酸时,一定要将浓硫酸沿器壁缓慢注入水里,并且用__________ 不断的搅拌,让产生的热量迅速散失。
①节约用水是每个公民的义务,日常生活中你的节水措施是
②天然水中含有许多杂质,自来水厂通常对天然水进行:沉淀、过滤、
③鉴别软水和硬水常用的试剂是
④如图所示的两个实验,探究结论:“水由氢元素和氧元素组成”的是实验

(2)下列有关水的说法正确的是
①蒸馏能净化水,也能将水软化
②二氧化碳能溶于水,也能与水反应
③氧化钙能吸收空气中的水,也能与水反应
④水是最常用的溶剂,也是与生命密不可分的物质
(3)小红同学在实验室欲配制一定质量分数的食盐溶液。配制的步骤可以概括为计算、称量和量取、
(4)汽车、电动车一般使用铅酸蓄电池。某铅酸蓄电池使用的酸溶液是质量分数为20%的稀硫酸。
①用100g质量分数为98%的浓硫酸配制质量分数为20%的稀硫酸,需要水的质量是
②配制该稀硫酸时,一定要将浓硫酸沿器壁缓慢注入水里,并且用
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】t2℃时,向盛有10mL水的A、B两试管中分别加入等质量的甲、乙两种可溶性固体,使其充分溶解后,观察到如图一所示的现象,请回答:
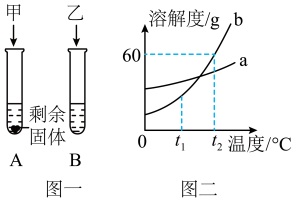
(1)t2℃时,_______ 试管中的溶液一定是饱和溶液。
(2)t2℃时,将80g乙的饱和溶液稀释为溶质质量分数10%的溶液,需加水_______ g。

(1)t2℃时,
(2)t2℃时,将80g乙的饱和溶液稀释为溶质质量分数10%的溶液,需加水
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】“人间烟火,抚慰凡心”。疫情来袭,中国人仍可“医食无忧”,岁月静好,是因为祖国的繁荣富强,国士的负重前行!

(1)“粮稳民心安。”袁隆平院士一辈子都在向他的杂交水稻梦奔跑。他的眼界很小,只在一粒小小的稻种上倾注了所有的精力;他的贡献很大,他让这粒稻种解决了14亿中国人吃饭的问题。
①水稻的主要成分为淀粉【化学式(C6H10O5)n】,淀粉是我们每天摄入较多的营养物质,它在人体内经淀粉酶和水的作用转化为葡萄糖(化学式C6H12O6),并溶解在血液里,通过呼吸作用提供营养和能量,呼吸作用是葡萄糖在酶和氧气的共同作用下发生的,生成两种常见的氧化物,请写出该反应的化学方程式______ 。
②农民种植水稻科学施加尿素【CO(NH2)2】等肥料,其中氮元素的质量分数为______ ;(精确到0.1%)
③青少年正处在生长发育期,应注意营养均衡,膳食合理。有些青少年不爱吃蔬菜、水果,影响生长发育,这主要是由于摄入______ 不足而引起的(填一种常见营养素)。
(2)钟南山院士准确判断,指导战“疫”。
①疫情期间,外出一定要戴口罩。一次性医用口罩阻隔病毒的关键材料熔喷布,是以聚丙烯为原料生产的。聚丙烯属于______ 材料。佩戴活性炭口罩有防毒、除臭、滤菌等功效,这是利用活性炭的______ 性;
②过氧乙酸(CH3COOOH)也是有效的消毒剂,某医疗小组欲用溶质质量分数为0.5%的过氧乙酸溶液200kg对环境进行消毒,需要溶质质量分数为20%的过氧乙酸溶液______ kg。

(1)“粮稳民心安。”袁隆平院士一辈子都在向他的杂交水稻梦奔跑。他的眼界很小,只在一粒小小的稻种上倾注了所有的精力;他的贡献很大,他让这粒稻种解决了14亿中国人吃饭的问题。
①水稻的主要成分为淀粉【化学式(C6H10O5)n】,淀粉是我们每天摄入较多的营养物质,它在人体内经淀粉酶和水的作用转化为葡萄糖(化学式C6H12O6),并溶解在血液里,通过呼吸作用提供营养和能量,呼吸作用是葡萄糖在酶和氧气的共同作用下发生的,生成两种常见的氧化物,请写出该反应的化学方程式
②农民种植水稻科学施加尿素【CO(NH2)2】等肥料,其中氮元素的质量分数为
③青少年正处在生长发育期,应注意营养均衡,膳食合理。有些青少年不爱吃蔬菜、水果,影响生长发育,这主要是由于摄入
(2)钟南山院士准确判断,指导战“疫”。
①疫情期间,外出一定要戴口罩。一次性医用口罩阻隔病毒的关键材料熔喷布,是以聚丙烯为原料生产的。聚丙烯属于
②过氧乙酸(CH3COOOH)也是有效的消毒剂,某医疗小组欲用溶质质量分数为0.5%的过氧乙酸溶液200kg对环境进行消毒,需要溶质质量分数为20%的过氧乙酸溶液
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】我国海岸线长达3.2万千米,海洋专属经济区幅员辽阔,海洋资源丰富,开发前景十分远大。
(1)我国海盐年产量3千多万吨,居世界第一位,基本流程如下图所示,目前从海水中提取食盐的方法主要为在蒸发池中促进水分蒸发,主要是利用了下列各项中的_________ (填选项序号)。

①潮汐能 ②生物能 ③电能 ④太阳能 ⑤化学能
(2)金属镁广泛应用于生活、生产和国防工业。从卤水中提取镁的过程如下图所示:

在上述转化过程中,①处所发生的反应属于________________ 反应(填“中和”“复分解”“氧化”“化合”“分解”之一)。
(3)海水中除了蕴含大量的钠元素和镁元素外,还含有大量的钾元素。KCl和KNO3的溶解度曲线如右图所示。试回答下列问题:
①t1℃时,KCl饱和溶液的溶质质量分数,____________________ KNO3饱和溶液的溶质质量分数(填“大于”“小于”“等于”之一)。
②已知20℃时,KNO3的溶解度为31.6g;80℃时,KNO3的溶解度为169g。

在20℃时,向盛有200g水的烧杯中加入80g硝酸钾,逐渐升温至80℃,在该温度下,最后所得溶液中溶质与溶剂的质量之比为___________________ (填最筒整数比)。
(4)已知:A、B、C、D、E、F是六种常见的物质,其中A是黑色固体,B是无色无味的剧毒气体,C是紫红色金属单质。它们之间的转化关系如图:

请回答:
①写出下列物质的化学式:B___________ 、C ___________ 、E _________ 。
②写出反应②的化学反应方程式:________________________________ ;该反应属于基本反应类型中的_________ 反应。
(1)我国海盐年产量3千多万吨,居世界第一位,基本流程如下图所示,目前从海水中提取食盐的方法主要为在蒸发池中促进水分蒸发,主要是利用了下列各项中的

①潮汐能 ②生物能 ③电能 ④太阳能 ⑤化学能
(2)金属镁广泛应用于生活、生产和国防工业。从卤水中提取镁的过程如下图所示:

在上述转化过程中,①处所发生的反应属于
(3)海水中除了蕴含大量的钠元素和镁元素外,还含有大量的钾元素。KCl和KNO3的溶解度曲线如右图所示。试回答下列问题:
①t1℃时,KCl饱和溶液的溶质质量分数,
②已知20℃时,KNO3的溶解度为31.6g;80℃时,KNO3的溶解度为169g。

在20℃时,向盛有200g水的烧杯中加入80g硝酸钾,逐渐升温至80℃,在该温度下,最后所得溶液中溶质与溶剂的质量之比为
(4)已知:A、B、C、D、E、F是六种常见的物质,其中A是黑色固体,B是无色无味的剧毒气体,C是紫红色金属单质。它们之间的转化关系如图:

请回答:
①写出下列物质的化学式:B
②写出反应②的化学反应方程式:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】海洋是巨大的资源宝库,人类应合理开发并加以保护。
(1)人类正运用各种方法开采、提取多种海洋资源,下列有关说法错误的是_______ (填序号)
A 海底蕴藏的“可燃冰”被誉为“21世纪能源”
B 利用海水涨落推动水轮机转动,从而可以发电
C 海水淡化、“晒盐”、“制碱”、“提镁”过程中,均主要涉及化学变化
D 建立海洋自然保护区,加强海洋环境监测,提高消除污染的技术水平等是保护海洋的必要措施
(2)海水晒盐得到的粗盐,常含泥沙等难溶性杂质和Ca2+、Mg2+、 等可溶性杂质离子,下列有关粗盐提纯的叙述中,错误的是
等可溶性杂质离子,下列有关粗盐提纯的叙述中,错误的是_______ (填序号)
A 除去食盐水中的可溶性杂质,可采用化学方法
B 除去食盐水中可溶性杂质的化学原理为:使杂质离子以沉淀或气体的形式从食盐中分离出来
C 除去食盐中难溶性杂质的方法,属于化学方法
D 粗盐提纯过程中,既有化学方法,又有物理方法
(3)如图是A、B两种固体物质的溶解度曲线:

①将t2℃时A物质的50g饱和溶液蒸干,理论上可以得到A物质_______ g;
②将t1℃时两种物质的饱和溶液同时升温到t2℃,所得溶液的溶质质量分数:A%_______ B%。(填“>”“=”“<”之一);
③若将B物质的不饱和溶液变为饱和溶液,下列有关说法正确的是_______ (填序号)。
A 溶质的质量一定变大
B 溶剂的质量一定变小
C 溶质的质量分数可能不变
D 溶液的温度一定升高
(1)人类正运用各种方法开采、提取多种海洋资源,下列有关说法错误的是
A 海底蕴藏的“可燃冰”被誉为“21世纪能源”
B 利用海水涨落推动水轮机转动,从而可以发电
C 海水淡化、“晒盐”、“制碱”、“提镁”过程中,均主要涉及化学变化
D 建立海洋自然保护区,加强海洋环境监测,提高消除污染的技术水平等是保护海洋的必要措施
(2)海水晒盐得到的粗盐,常含泥沙等难溶性杂质和Ca2+、Mg2+、
 等可溶性杂质离子,下列有关粗盐提纯的叙述中,错误的是
等可溶性杂质离子,下列有关粗盐提纯的叙述中,错误的是A 除去食盐水中的可溶性杂质,可采用化学方法
B 除去食盐水中可溶性杂质的化学原理为:使杂质离子以沉淀或气体的形式从食盐中分离出来
C 除去食盐中难溶性杂质的方法,属于化学方法
D 粗盐提纯过程中,既有化学方法,又有物理方法
(3)如图是A、B两种固体物质的溶解度曲线:

①将t2℃时A物质的50g饱和溶液蒸干,理论上可以得到A物质
②将t1℃时两种物质的饱和溶液同时升温到t2℃,所得溶液的溶质质量分数:A%
③若将B物质的不饱和溶液变为饱和溶液,下列有关说法正确的是
A 溶质的质量一定变大
B 溶剂的质量一定变小
C 溶质的质量分数可能不变
D 溶液的温度一定升高
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】海水综合利用的主要流程如下图。
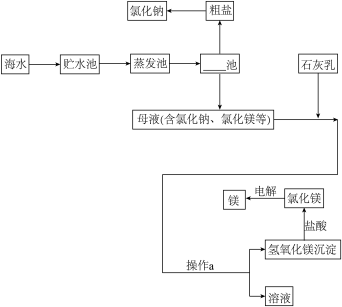
(1)上述工业生产流程图中横线上应该填写_____ 。
(2)操作a的名称是_____ ,在实验室中进行此项操作要用到的金属仪器是_____ 。
(3)根据海水晒盐的工业流程,下列说法中不正确的是_____ (填字母)
a、海水进入贮水池,海水的浓度基本不变
b、蒸发池中,海水中氯化钠的质量逐渐增加
c、母液一定是氯化钠的饱和溶液
(4)制取金属镁,需要在高温熔化状态下电解氯化镁,该反应要在氩气环境中而不能在空气中进行,理由是_____ 。(用化学方程式表示)

(1)上述工业生产流程图中横线上应该填写
(2)操作a的名称是
(3)根据海水晒盐的工业流程,下列说法中不正确的是
a、海水进入贮水池,海水的浓度基本不变
b、蒸发池中,海水中氯化钠的质量逐渐增加
c、母液一定是氯化钠的饱和溶液
(4)制取金属镁,需要在高温熔化状态下电解氯化镁,该反应要在氩气环境中而不能在空气中进行,理由是
您最近一年使用:0次



