如图为 A、B、C 三种固体物质的溶解度曲线。

(1)溶解度随温度升高而降低的物质是______ 。
(2)温度为______ ℃时,A、C两种物质的溶解度相等。
(3)t2 ℃时,把 50g的 A、B分别加到 100g水中,能形成饱和溶液的物质是______ ,所得溶液的溶质质量分数为______ (计算结果精确到 0.1%)。
(4)当B中含有少量 A,可采用______ 的方法提纯 B。

(1)溶解度随温度升高而降低的物质是
(2)温度为
(3)t2 ℃时,把 50g的 A、B分别加到 100g水中,能形成饱和溶液的物质是
(4)当B中含有少量 A,可采用
更新时间:2021-06-06 16:43:06
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】化学知识在生产和生活中有重要作用。请根据图表回答以下问题。
【资料】两种物质在不同温度时的溶解度
生活在盐碱湖附近的人们习惯“夏天晒盐、冬天捞碱〞。
(1)“夏天晒盐〞是利用了氯化钠的溶解度___________ 的特点,氯化钠属于_________ (填“易溶”或“可溶”)物质。
(2)“冬天捞碱”,这里的碱指的是纯碱,主要成分是碳酸钠。30℃时,50g碳酸钠加入100g水形成溶液中溶质与溶剂的质量比为________ 。碳酸钠与氯化钠溶解度相等的温度范围是______ 。
【实验一】粗碱初步提纯
“冬天捞碱”中获得粗碱中含可溶性的氯化钠和泥沙的少量杂质,提纯流程如下:

(3)溶解中玻璃棒的作用是________ 。操作B名称是______ 。
(4)流程中获得碳酸钠样品为__________ (填“混合物”或“纯净物”)。
【实验二】将实验一所得碳酸钠样品提纯
(5)碳酸钠样品中混有氯化钠杂质,经过多步操作后可获得纯净的碳酸钠,其中的操作依次为:溶解、蒸发浓缩、_____ 、_____ 、洗涤、烘干。
【实验三】测定实验一所得样品中碳酸钠的质量分数。
称取50g碳酸钠样品,进行如下实验

(6)步骤Ⅱ所得滤液B为碳酸钠的__________ (填“饱和”或“不饱和”)溶液。
(7)样品中碳酸钠的质量分数为__________ 。
【资料】两种物质在不同温度时的溶解度
| 温度/℃ | 0 | 20 | 30 | 40 | 60 | 80 | |
| 溶解度(g/100g水) | NaCl | 35.7 | 36 | 36.3 | 36.6 | 37.1 | 38.4 |
| Na2CO3 | 7 | 22 | 40 | 49 | 46 | 43.6 | |
(1)“夏天晒盐〞是利用了氯化钠的溶解度
(2)“冬天捞碱”,这里的碱指的是纯碱,主要成分是碳酸钠。30℃时,50g碳酸钠加入100g水形成溶液中溶质与溶剂的质量比为
【实验一】粗碱初步提纯
“冬天捞碱”中获得粗碱中含可溶性的氯化钠和泥沙的少量杂质,提纯流程如下:

(3)溶解中玻璃棒的作用是
(4)流程中获得碳酸钠样品为
【实验二】将实验一所得碳酸钠样品提纯
(5)碳酸钠样品中混有氯化钠杂质,经过多步操作后可获得纯净的碳酸钠,其中的操作依次为:溶解、蒸发浓缩、
【实验三】测定实验一所得样品中碳酸钠的质量分数。
称取50g碳酸钠样品,进行如下实验

(6)步骤Ⅱ所得滤液B为碳酸钠的
(7)样品中碳酸钠的质量分数为
您最近一年使用:0次
【推荐2】生命必需的水在化学中用途广泛。
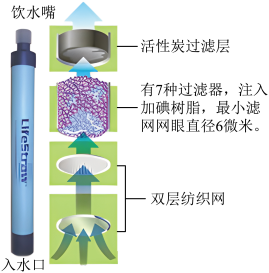
(1)电视节目《荒野求生》中的生命吸管(如下图所示),是一 种将污水净化为饮用水的吸管装置,可以除去 99.3%的细菌和病毒,但难以除去汞等金属离子。野外环境中很多地下水含较多_______ 称为硬水;生命吸管中活性炭___ (“能”或“不能”)使硬水软化。家庭中使硬水软化一般采取______ 方法。
(2)配制 1000g 质量分数是 16%的氯化钠溶液,所需氯化钠 的质量为______ ,水的体积为_______ mL(水的密度近似看 作 1g/mL)。
﹙3﹚下图是甲、乙、丙三种固体物质(均不含结晶水)的溶解 度曲线。
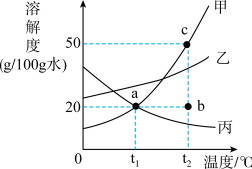
①t1℃时,甲、乙、丙三种物质的溶解度大小关系_______ 。
②t1℃时,完全溶解 5g 丙物质至少需要水_______ g。
③t2℃时,将 20g 甲加入 100g 水中,充分搅拌后所得溶液是 甲的_______ 溶液(填“饱和”或“不饱和”),可以用上图中_______ 点(填“a”“b”“c”)表示。
④将甲、丙的饱和溶液从 t2℃降温到 t1℃,对所得溶液的叙述不 正确的是________
A.都是饱和溶液 B.溶剂质量:甲<丙
C.析出固体质量:甲>丙 D.溶质质量分数:甲=丙
(1)电视节目《荒野求生》中的生命吸管(如下图所示),是一 种将污水净化为饮用水的吸管装置,可以除去 99.3%的细菌和病毒,但难以除去汞等金属离子。野外环境中很多地下水含较多

(2)配制 1000g 质量分数是 16%的氯化钠溶液,所需氯化钠 的质量为
﹙3﹚下图是甲、乙、丙三种固体物质(均不含结晶水)的溶解 度曲线。

①t1℃时,甲、乙、丙三种物质的溶解度大小关系
②t1℃时,完全溶解 5g 丙物质至少需要水
③t2℃时,将 20g 甲加入 100g 水中,充分搅拌后所得溶液是 甲的
④将甲、丙的饱和溶液从 t2℃降温到 t1℃,对所得溶液的叙述不 正确的是
A.都是饱和溶液 B.溶剂质量:甲<丙
C.析出固体质量:甲>丙 D.溶质质量分数:甲=丙
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:

(1)t3℃时,甲的溶解度为____________ g;
(2)t1℃时,甲、乙的饱和溶液各100g,分别蒸发掉10g水,析出固体的质量:甲____ (填“<”“>”或“=”)乙;
(3)t2℃时,在各盛有甲、乙、丙25g固体的三个烧杯中,分别加入100g水,充分搅拌后,能形成饱和溶液的是__________ ;将三个烧杯中的物质均升温至t3℃,此时,溶液中溶质的质量分数的大小关系为_______ 。

(1)t3℃时,甲的溶解度为
(2)t1℃时,甲、乙的饱和溶液各100g,分别蒸发掉10g水,析出固体的质量:甲
(3)t2℃时,在各盛有甲、乙、丙25g固体的三个烧杯中,分别加入100g水,充分搅拌后,能形成饱和溶液的是
您最近一年使用:0次
【推荐1】铈元素属于稀土元素,稀土元素又称“21世纪黄金”,广泛应用于电子、军事、石油化工等领域。下表是硫酸铈[Ce(SO4)2]和硝酸钾两种固体物质在不同温度时的溶解度。
根据数据,绘制出二者的溶解度曲线如图所示,回答下列问题。________ 。
(2)不改变硫酸铈不饱和溶液的溶质质量分数,将其变成饱和溶液可采取________ 的方法。
(3)下列关于两种物质的说法中正确的是 。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | |
| 溶解度/g | 硝酸钾 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
| 硫酸铈 | 24.1 | 20 | 17.2 | 14 | 10 | 8.9 | 8.3 | 7.1 | 6.0 | |
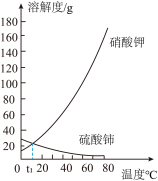
(2)不改变硫酸铈不饱和溶液的溶质质量分数,将其变成饱和溶液可采取
(3)下列关于两种物质的说法中正确的是 。
| A.硫酸铈属于易溶物质 |
| B.t1℃时两种物质的溶液中溶质质量分数相等 |
| C.20℃时,饱和硫酸铈溶液中含有少量的硝酸钾,可采用蒸发结晶的方法提纯硫酸铈 |
| D.0℃<t<t1℃时,硝酸钾的溶解度大于硫酸铈的溶解度 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】如图是a、b、c三种物质的溶解度曲线,请你回答:

(1)t2℃时,a、b、c三种物质的饱和溶液降温时无晶体析出的是______
(2)t2℃时,a、b、c三种物质的饱和溶液中溶质的质量分数由大到小的排列顺序为____ 。
(3)若a中混有少量b,提纯a的方法是___________ 。
(4)t2℃时,向30 ga物质中加入50 g水,充分溶解后,所得溶液质量为___________
(5)配置150kg10%的a溶液,需用30%的a溶液_____ kg需加水______ kg

(1)t2℃时,a、b、c三种物质的饱和溶液降温时无晶体析出的是
(2)t2℃时,a、b、c三种物质的饱和溶液中溶质的质量分数由大到小的排列顺序为
(3)若a中混有少量b,提纯a的方法是
(4)t2℃时,向30 ga物质中加入50 g水,充分溶解后,所得溶液质量为
(5)配置150kg10%的a溶液,需用30%的a溶液
您最近一年使用:0次
【推荐3】溶液与人类生产、生活密切相关。
(1)把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是____(填字母)。
(2)下列不是影响物质溶解度的因素的是____(填字母)。
(3)A、B、C三种固体物质(均不含结晶水)的溶解度曲线如图所示。

①t1℃时,三种物质的溶解度由大到小的关系为____ 。
②t1℃时,30g固体A放入50g水中充分溶解,形成饱和溶液的质量为____ g。
③三种物质的饱和溶液从t2℃降到t1℃,所得溶液中溶质的质量分数由大到小的关系为____ 。
(1)把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是____(填字母)。
| A.氯化钠 | B.面粉 | C.蔗糖 | D.香油 |
| A.溶质的种类 | B.溶剂的种类 | C.溶剂的质量 | D.温度 |

①t1℃时,三种物质的溶解度由大到小的关系为
②t1℃时,30g固体A放入50g水中充分溶解,形成饱和溶液的质量为
③三种物质的饱和溶液从t2℃降到t1℃,所得溶液中溶质的质量分数由大到小的关系为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】如图是甲、乙、丙三种物质的溶解度曲线,回答下列问题:

(1)P点表示的意义是________
(2)t3℃时,50g甲物质溶解在50g水中,得到溶液的质量是__________ 。
(3)甲、乙、丙三种物质的饱和溶液从t2℃降低到t1℃时,得到的三种物质的质量分数从大到小的顺序是________ 。
(4)要使丙物质的饱和溶液变为不饱和溶液,在不改变物质的组成条件下,应采取的方法是___________ 。
(5)下列说法正确的是_________ (填序号)
A.P点是表示在t2℃时,甲、乙的质量分数相等
B.t3℃时,在100g水中最多溶解50g的甲物质
C.t1℃时,在50g水中加入15ga物质,得到溶液65g
D.甲的溶解度大于丙的溶解度

(1)P点表示的意义是
(2)t3℃时,50g甲物质溶解在50g水中,得到溶液的质量是
(3)甲、乙、丙三种物质的饱和溶液从t2℃降低到t1℃时,得到的三种物质的质量分数从大到小的顺序是
(4)要使丙物质的饱和溶液变为不饱和溶液,在不改变物质的组成条件下,应采取的方法是
(5)下列说法正确的是
A.P点是表示在t2℃时,甲、乙的质量分数相等
B.t3℃时,在100g水中最多溶解50g的甲物质
C.t1℃时,在50g水中加入15ga物质,得到溶液65g
D.甲的溶解度大于丙的溶解度
您最近一年使用:0次
【推荐2】溶液与人们的生产生活密切相关。如图1为甲、乙两种固体物质的溶解度曲线。
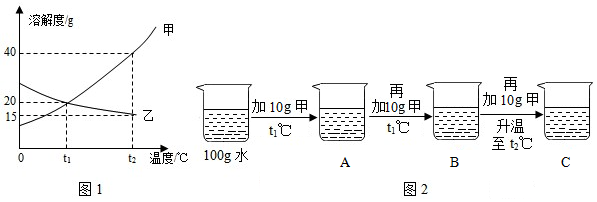
(1)某同学按图2所示进行实验,得到相应温度下的A、B、C溶液,在A、B、C三种溶液中属于不饱和溶液的是_____ (填字母)。
(2)将t2℃时的等质量的甲、乙两种物质的饱和溶液降温至t1℃,所得溶液的质量甲_____ 乙(填“<”、“=”或“>”)。
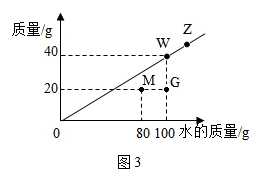
(3)图3是t3℃时,根据W物质在不同质量的水中达到饱和状态时所溶解物质的质量,绘制成的图像。请判断W物质的溶解度随温度的变化关系_____ (填字母)。
a 与图1甲物质相似 b 与图1乙物质相似 c 无法判断
(4)图3中4个点(M、G、W、Z)表示的溶液溶质质量分数的大小关系是_____ 。


(1)某同学按图2所示进行实验,得到相应温度下的A、B、C溶液,在A、B、C三种溶液中属于不饱和溶液的是
(2)将t2℃时的等质量的甲、乙两种物质的饱和溶液降温至t1℃,所得溶液的质量甲
(3)图3是t3℃时,根据W物质在不同质量的水中达到饱和状态时所溶解物质的质量,绘制成的图像。请判断W物质的溶解度随温度的变化关系
a 与图1甲物质相似 b 与图1乙物质相似 c 无法判断
(4)图3中4个点(M、G、W、Z)表示的溶液溶质质量分数的大小关系是
您最近一年使用:0次




