以某菱镁矿石(主要成分是MgCO3,含少量MnCO3、SiO2)制取MgSO4·7H2O,流程如下:______ (写出一种)。此时,MnCO3发生反应的化学方程式是______ 。
(2)“转化”时主要反应是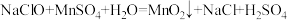 ,氯元素反应前后化合价变化情况是
,氯元素反应前后化合价变化情况是______ (填“升高”或“降低”)。
(3)硫酸镁溶液在不同温度下进行浓缩结晶,可得到不同的晶体:
①“操作1”的具体操作是:蒸发浓缩滤液至表面有晶膜出现(此时MgSO4溶液已饱和)、______ 、过滤、洗涤、低温干燥。
②“操作1”所得滤液中能分离出一种可循环使用的物质,该物质是______ (填化学式)。循环使用的目的是______ 。
(4)已知:MgSO4·7H2O中镁元素质量分数为9.76%,采用热分析法测定所得MgSO4·7H2O样品中镁元素质量分数:
①未加热前,测得样品中镁元素质量分数略大于9.76%,可能的原因是______ 。
②高于900℃后,测得剩余固体中镁元素质量分数大于20%,可能的原因是______ 。
(5)若用100t菱镁矿石可制得246 t MgSO4·7H2O产品,忽略反应过程中镁元素损失,求该菱镁矿石中MgCO3的质量分数。(写出计算过程)______ 。
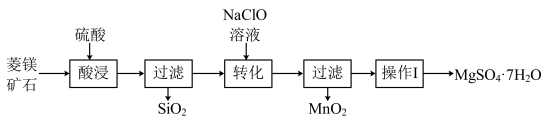
(2)“转化”时主要反应是
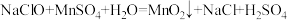 ,氯元素反应前后化合价变化情况是
,氯元素反应前后化合价变化情况是(3)硫酸镁溶液在不同温度下进行浓缩结晶,可得到不同的晶体:
| 温度/℃ | -3.9-1.8 | 1.8-48.1 | 48.1-67.5 | 67.5-200 |
| 析出晶体 | MgSO4·12H2O | MgSO4·7H2O | MgSO4·6H2O | MgSO4·H2O等 |
②“操作1”所得滤液中能分离出一种可循环使用的物质,该物质是
(4)已知:MgSO4·7H2O中镁元素质量分数为9.76%,采用热分析法测定所得MgSO4·7H2O样品中镁元素质量分数:
①未加热前,测得样品中镁元素质量分数略大于9.76%,可能的原因是
②高于900℃后,测得剩余固体中镁元素质量分数大于20%,可能的原因是
(5)若用100t菱镁矿石可制得246 t MgSO4·7H2O产品,忽略反应过程中镁元素损失,求该菱镁矿石中MgCO3的质量分数。(写出计算过程)
2021·江苏扬州·中考真题 查看更多[9]
(已下线)专题10? 工业流程题(六大题型)-2024年中考化学二轮热点题型归纳与变式演练(江苏通用)(已下线)2023年中考风向标-江苏-流程题(已下线)高分突破01 关于实验传感器图像的探究-备战2022年中考化学实验探究题高分突破(已下线)高分突破16 定性定量分析实验的探究-备战2022年中考化学实验探究题高分突破江苏省苏州市姑苏区振华中学2021-2022学年九年级下学期3月月考化学试题(已下线)2022江苏中考风向标-质量守恒定律(已下线)2022江苏中考风向标-流程题(已下线)专题20 流程图题-2021年中考化学真题分项汇编(全国通用)(第01期)江苏省扬州市2021年中考化学试题
更新时间:2021-06-19 17:04:23
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】质量相同的一氧化碳和甲烷在空气中充分燃烧,消耗氧气的质量比为________ 。
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】乙醇常用作燃料,乙醇完全燃烧的化学方程式为______ 。天然气也是常用的燃料,其主要成分是甲烷。当氧气不足时,甲烷燃烧会生成 ,CO和
,CO和 ,若48g甲烷燃烧生成
,若48g甲烷燃烧生成 和CO的质量比为11:14,则参加反应的
和CO的质量比为11:14,则参加反应的 的质量为
的质量为______ g。
 ,CO和
,CO和 ,若48g甲烷燃烧生成
,若48g甲烷燃烧生成 和CO的质量比为11:14,则参加反应的
和CO的质量比为11:14,则参加反应的 的质量为
的质量为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】4.8g的甲醇(CH3OH)在6.4g氧气中燃烧,充分反应后,得到5.4g水、4.4g二氧化碳和一定质量的X,则X的质量为___________ g,此反应的化学方程式为___________ 。
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿空气中易变质。CuCl的制备流程如图:

(1)“滤液1”中除了Na+、 外,还存在较多的离子是
外,还存在较多的离子是___________ (写离子符号)。
(2)“反应”中发生的化学变化是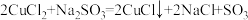 ,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为
,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为___________ 。
(3)“操作a”的名称是___________ ,实验室中溶解和操作a都会用到的一种仪器是___________ 。本流程中可以循环利用的物质(水除外)是___________ (写化学式)。
(4)“醇洗”的目的是___________ 。
(5)320gCuSO4与足量NaCl经上述制备流程,可生成的CuCl最多是___________ g。

(1)“滤液1”中除了Na+、
 外,还存在较多的离子是
外,还存在较多的离子是(2)“反应”中发生的化学变化是
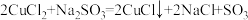 ,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为
,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为(3)“操作a”的名称是
(4)“醇洗”的目的是
(5)320gCuSO4与足量NaCl经上述制备流程,可生成的CuCl最多是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐1】硫酸锌可作为食品锌强化剂的原料.工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3 、MgO、CaO等,生产工艺流程示意如下:
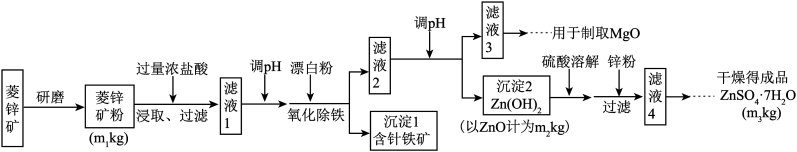
[相关资料]不溶性碱受热分解后生成对应的氧化物。
(1)将菱锌矿研磨成粉的目的是_______
(2)完成“氧化除铁”步骤中反应的化学方程式:2Fe(OH)2+Ca(ClO)2+2H2O=2____ +CaCl2,这个反应中有 ______ 种元素的化合价发生了变化。
(3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,化学式是FeO(OH),组成元素Fe、O、H的质量比是________ ;
(4)根据下表数据,调节“滤液2”的pH范围为_________ ;
(5)工业上从“滤液3”制取MgO过程中,合适的反应物是 _______ (选填序号).
a大理石粉 b石灰乳 c纯碱溶液 d烧碱溶液
(6)“滤液4”之后的操作依次为 :蒸发浓缩、________ 、过滤,洗涤,干燥.
(7)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于_______ .

[相关资料]不溶性碱受热分解后生成对应的氧化物。
(1)将菱锌矿研磨成粉的目的是
(2)完成“氧化除铁”步骤中反应的化学方程式:2Fe(OH)2+Ca(ClO)2+2H2O=2
(3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,化学式是FeO(OH),组成元素Fe、O、H的质量比是
(4)根据下表数据,调节“滤液2”的pH范围为
| Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 | |
| 开始沉淀的pH | 10.4 | 6.4 | - | - |
| 沉淀完全的pH | 12.4 | 8.0 | - | - |
| 开始溶解的pH | - | 10.5 | - | - |
a大理石粉 b石灰乳 c纯碱溶液 d烧碱溶液
(6)“滤液4”之后的操作依次为 :蒸发浓缩、
(7)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于
您最近一年使用:0次
【推荐2】根据图1所示NaCl、KNO3的溶解度曲线和图2所示实验,回答下列问题:


(1)20℃时,将35 g NaCl固体加入50g水中充分溶解,得到的NaCl溶液是___________ (填“饱和”或“不饱和”)溶液。
(2)50℃时,将等质量的氯化钠和硝酸钾两种物质分别加水配成饱和溶液,得到的饱和溶液的质量关系:NaCl溶液___________ (选填“>”、“=”或“<”)KNO3溶液。
(3)当KNO3中混有少量的NaCl,可采用___________ 的方法提纯KNO3。
(4)在20℃时进行了如图2所示的实验,下列有关说法正确的是___________(填字母)。


(1)20℃时,将35 g NaCl固体加入50g水中充分溶解,得到的NaCl溶液是
(2)50℃时,将等质量的氯化钠和硝酸钾两种物质分别加水配成饱和溶液,得到的饱和溶液的质量关系:NaCl溶液
(3)当KNO3中混有少量的NaCl,可采用
(4)在20℃时进行了如图2所示的实验,下列有关说法正确的是___________(填字母)。
| A.向④中加入4.5gKNO3即可达到饱和 | B.②③④中溶质的质量分数相等 |
| C.①③④均为KNO3的不饱和溶液 | D.④→⑤可析出53.9gKNO3晶体 |
您最近一年使用:0次
【推荐3】根据给出的KNO3和NaCl两种物质的溶解度表及溶解度曲线,回答问题。

(1)在20℃时,NaCl的溶解度为______ g;
(2)根据溶解度信息分析,从海水中提取氯化钠采用蒸发结晶的方法,原因是__________ ;
(3)55g硝酸钾和10g氯化钠的混合物,要完全溶解,至少需要加60℃的水______ g;
(4)20℃时,分别将等质量的KNO3和NaCl完全溶解并配成饱和溶液,下列分析中正确的是______。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |

(1)在20℃时,NaCl的溶解度为
(2)根据溶解度信息分析,从海水中提取氯化钠采用蒸发结晶的方法,原因是
(3)55g硝酸钾和10g氯化钠的混合物,要完全溶解,至少需要加60℃的水
(4)20℃时,分别将等质量的KNO3和NaCl完全溶解并配成饱和溶液,下列分析中正确的是______。
| A.硝酸钾溶液中溶质的质量分数大于氯化钠溶液中溶质的质量分数 |
| B.硝酸钾溶液的质量大于氯化钠溶液的质量 |
| C.将两种溶液升温到60℃,溶质的质量分数都变大 |
| D.将两种溶液分别降温到0℃,析出的硝酸钾质量大于析出的氯化钠的质量 |
| E.硝酸钾溶液中水的质量与氯化钠溶液中水的质量比为90:79 |
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐1】A~F是初中化学常见的物质,已知A、B、C、D、E是五种不同类别的物质,A是空气中含有的一种气体,E是地壳中含量最多的金属元素组成的单质,F为蓝色溶液且各元素质量比为2:1:2,六种物质之间的反应与转化关系均为初中化学常见的化学反应,图中“﹣”表示相连的物质能相互反应,“→”表示一种物质转化成另一种物质(部分反应物、生成物及反应条件已略去)请回答下列问题:
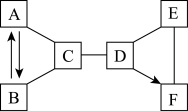
(1)B物质的化学式_____ 。
(2)A和C反应的化学方程式______ 。
(3)E和F反应的化学方程式_______ 。

(1)B物质的化学式
(2)A和C反应的化学方程式
(3)E和F反应的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
名校
解题方法
【推荐2】下图中ABCD分别为不同类别的无机化合物,其中B是一种常见的食品干燥剂,C、 E属于同类物质,F的溶液为黄色且能与硝酸银溶液反应,产生不溶于稀硝酸的白色沉淀。(“→”表示物质之间的相互转化关系,“一”表示两端的物质能发生化学反应)

(1)根据推断写出以下两种物质的化学式:A:____________ ;F: _____________ 。
(2) D与C的反应属于____________ 反应(填基本反应类型)。
(3)写出反应C→E的化学方程式:__________________________ 。
(4)写出D物质的一种用途__________________________ 。
(5) E溶液与F溶液反应的现象是__________________________ 。

(1)根据推断写出以下两种物质的化学式:A:
(2) D与C的反应属于
(3)写出反应C→E的化学方程式:
(4)写出D物质的一种用途
(5) E溶液与F溶液反应的现象是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐3】实验室有100g废液,其中含有硫酸铜、硫酸亚铁、硫酸锌。现对废液进行处理,得到铜和硫酸锌溶液,实验流程如下图所示。

①步骤I、II、III中均包含的操作名称是_____ 。
②滤液B中的溶质是___________________ 。
③当观察到________ 时,说明滤渣A中铁已经完全反应。
④步骤III中加入的X是_________ 。
⑤实验结束后,生成0.1mol铜,请计算原废液中硫酸铜的溶质质量分数。
(根据化学方程式列式计算)___________

①步骤I、II、III中均包含的操作名称是
②滤液B中的溶质是
③当观察到
④步骤III中加入的X是
⑤实验结束后,生成0.1mol铜,请计算原废液中硫酸铜的溶质质量分数。
(根据化学方程式列式计算)
您最近一年使用:0次



