孔雀石主要成分是碱式碳酸铜【Cu2(OH)2CO3】,另外还含有少量的SiO2等杂质(杂质不与硫酸发生反应)。某化学兴趣小组为测定孔雀石中Cu2(OH)2CO3的含量进行如下实验:取30g孔雀石样品,粉碎后放入烧杯中,将200g稀硫酸分成四等份,分四次加入烧杯中,测出每次完全反应后烧杯内物质的总质量,实验数据记录如下:
请完成:(1)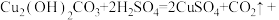 ______。
______。
(2)该反应中生成气体的总质量是______g。
(3)所用稀硫酸的溶质质量分数。(写出计算过程)
| 次数 | 加稀硫酸前 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的质量(g) | 0 | 50 | 50 | 50 | 50 |
| 烧杯内物质的总质量(g) | 30 | 77.8 | 125.6 | 174.5 | 224.5 |
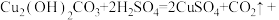 ______。
______。(2)该反应中生成气体的总质量是______g。
(3)所用稀硫酸的溶质质量分数。(写出计算过程)
2021·山东菏泽·中考真题 查看更多[6]
山东省菏泽市2021年中考化学试题(已下线)专题24 化学计算-2021年中考化学真题分项汇编(全国通用)(第02期)河北省部分学校2022-2023学年九年级上学期期末化学试题(已下线)专题10 溶解现象(讲练)-2023年中考化学一轮复习讲练测(沪教版·全国)2023年山东省枣庄市薛城区中考一模(彩虹班)化学试题2024年山东省临沂市莒南县中考一模化学试题
更新时间:2021-06-23 16:19:48
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】实验室用含杂质的锌(也称粗锌)与盐酸反应制取氢气,取8.0g含杂质的锌粒于烧杯中(所含杂质不溶于水,也不与酸反应),向其中加入73.0g稀盐酸,恰好完全反应后烧杯内剩余物质的质量为80.8g。计算:
(1)生成氢气的质量______g。
(2)反应氯化氢和生成氯化锌的质量。
(1)生成氢气的质量______g。
(2)反应氯化氢和生成氯化锌的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】现有H2SO4和CuSO4的混合溶液,为了测定CuSO4的质量分数,小明同学进行如下实验:
取混合溶液于烧杯中,向其中加入铁片至完全反应。反应前后,有关数据如表。
(1)实验中产生氢气的质量为______克。
(2)请根据实验数据计算原混合溶液中CuSO4的质量分数。
(3)小红同学用加入足量BaCl2溶液,通过生成BaSO4沉淀的质量来计算原混合溶液中CuSO4的质量分数,请分析是否合理并说明原因______。
取混合溶液于烧杯中,向其中加入铁片至完全反应。反应前后,有关数据如表。
| 烧杯 | 原混合溶液 | 加入的铁片 | 反应后烧和烧杯内物质的总质量(克) | 剩余铁片 | 析出铜 | |
| 质量(克) | 80 | 100 | 20 | 199.8 | 3.2 | 12.8 |
(1)实验中产生氢气的质量为______克。
(2)请根据实验数据计算原混合溶液中CuSO4的质量分数。
(3)小红同学用加入足量BaCl2溶液,通过生成BaSO4沉淀的质量来计算原混合溶液中CuSO4的质量分数,请分析是否合理并说明原因______。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】化学兴趣小组的同学要测定鸡蛋壳(主要成分是碳酸钙)中含CaCO3的质量分数。取20g鸡蛋壳,捣碎,放入烧杯中,向其中加入80g某质量分数的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其它成分都不溶于水,且不与稀盐酸反应),测得烧杯中反应剩余物的质量(m)与反应时间(t)的关系如图所示,当反应进行到B点时,所用盐酸刚好消耗了加入量的一半。

(1)反应中产生CO2的质量为______ g。
(2)20g该鸡蛋壳中CaCO3的质量分数为多少?(写出计算过程)
(3)请读图分析,B点表示的意义是______ (双选)。
①CaCO3与稀盐酸的反应刚好进行到一半
②CaCO3与稀盐酸反应已结束
③烧杯中剩余液体的质量是93.4g
④CaCO3已全部反应

(1)反应中产生CO2的质量为
(2)20g该鸡蛋壳中CaCO3的质量分数为多少?(写出计算过程)
(3)请读图分析,B点表示的意义是
①CaCO3与稀盐酸的反应刚好进行到一半
②CaCO3与稀盐酸反应已结束
③烧杯中剩余液体的质量是93.4g
④CaCO3已全部反应
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】2024年4月30日,“神舟十七号”载人飞船返回舱在东风着陆场成功着陆。飞船返回着陆时主要靠制动,飞船携带的推进剂是联氨 和四氧化二氮
和四氧化二氮 ,制动时的反应原理是
,制动时的反应原理是 。
。
(1)请写出 的化学式:
的化学式:__________ 。
(2)若飞船返回时携带 联氨,制动时联氨完全反应,求产生氮气的质量是多少?(写出计算过程)
联氨,制动时联氨完全反应,求产生氮气的质量是多少?(写出计算过程)
 和四氧化二氮
和四氧化二氮 ,制动时的反应原理是
,制动时的反应原理是 。
。(1)请写出
 的化学式:
的化学式:(2)若飞船返回时携带
 联氨,制动时联氨完全反应,求产生氮气的质量是多少?(写出计算过程)
联氨,制动时联氨完全反应,求产生氮气的质量是多少?(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】孔雀石主要成分是碱式碳酸铜[Cu2(OH)2CO3],另外还含有少量的SiO2等杂质(杂 质不与硫酸发生反应)。某化学兴趣小组为测定孔雀石中Cu2(OH)2CO3的含量,进行如下实验。取30g孔雀石样品,粉碎后放入烧杯中,将200g稀硫酸分成四等份,分四次加入烧杯中,测 出每次完全反应后烧杯内物质的总质量。实验数据记录如下:
请完成:
(1)
_____ 。
(2)所用稀硫酸的溶质质量分数______ 。(写出计算过程)
| 次数 | 加稀硫酸前 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的质量(g) | 0 | 50 | 50 | 50 | 50 |
| 烧杯内物质的总质量(g) | 30 | 77.8 | 125.6 | 174.5 | 224.5 |
(1)

(2)所用稀硫酸的溶质质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】铁铜金属粉末常用于生产机械零件。为测定某铁铜金属粉末中铁粉的含量,取20g样品于烧杯中,逐滴加入稀硫酸充分反应后,测得固体质量随加入稀硫酸的质量关系如图所示。计算:______ g。
(2)恰好完全反应时,溶液的颜色为_______ 。
(3)所用稀硫酸的溶质质量分数_______ 。(写出计算过程)。

(2)恰好完全反应时,溶液的颜色为
(3)所用稀硫酸的溶质质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】为测定一瓶 溶液中溶质的质量分数,兴趣小组进行如下实验:
溶液中溶质的质量分数,兴趣小组进行如下实验:
(1)生成氢氧化铜沉淀的质量为_____ 。
(2)该瓶 溶液中溶质的质量分数(写出计算过程)。
溶液中溶质的质量分数(写出计算过程)。
 溶液中溶质的质量分数,兴趣小组进行如下实验:
溶液中溶质的质量分数,兴趣小组进行如下实验:
(1)生成氢氧化铜沉淀的质量为
(2)该瓶
 溶液中溶质的质量分数(写出计算过程)。
溶液中溶质的质量分数(写出计算过程)。
您最近一年使用:0次

 4H2O+2CO2↑+3
4H2O+2CO2↑+3


