化学就在我们身边,人类的生活离不开化学。
(1)紫薯营养丰富,具有特殊的保健功能。下表是100 g紫薯粉的营养成分含量表:
①以上营养成分中_______ (填名称)是人体中含有的微量元素。
②紫薯中的花青素能消耗活性氧,具有_______ (填“氧化”或“还原”)性,可用于抗衰老。
③在酶的作用下,淀粉水解为葡萄糖,葡萄糖再转化为乙醇和二氧化碳。写出葡萄糖转化为乙醇的化学方程式:_______ 。
(2)材料的不断发展可以促进社会进步。
①碱式碳酸铝镁[MgaAlb(OH)c(CO3)d·xH2O]常用作塑料阻燃剂。化学式中a、b、c、d的代数关系式为_______ 。
②有机玻璃属于_______ (填字母)。
A 复合材料 B.合成材料 C.金属材料 D.无机非金属材料
(3)水和天然气重整可以得到合成气,其反应的微观示意图如图所示:
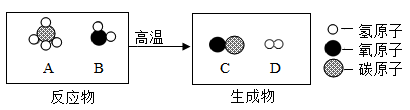
①在微观模型A、B、C、D中,表示水分子的是_______ (填字母代号)。
②生成物中,C和D的质量比为_______ 。
(4)农业生产中,氮肥硫酸铵不能和熟石灰混合使用的原因_______ (用化学方程式表示),检验生成的气体可以使用_______ 试纸。
(1)紫薯营养丰富,具有特殊的保健功能。下表是100 g紫薯粉的营养成分含量表:
| 营养成分 | 含量(每100 g) | 营养成分 | 含量(每100 g) |
| 水分 | 9.9 g | 钙元素 | 23.00 mg |
| 脂肪 | 0.2 g | 铁元素 | 1.10 mg |
| 蛋白质 | 4.8 g | 硒元素 | 0.02 mg |
| 淀粉 | 82.5 g | 花青素 | 0.10 g |
| 纤维素 | 2.7 g | 其他 | …… |
②紫薯中的花青素能消耗活性氧,具有
③在酶的作用下,淀粉水解为葡萄糖,葡萄糖再转化为乙醇和二氧化碳。写出葡萄糖转化为乙醇的化学方程式:
(2)材料的不断发展可以促进社会进步。
①碱式碳酸铝镁[MgaAlb(OH)c(CO3)d·xH2O]常用作塑料阻燃剂。化学式中a、b、c、d的代数关系式为
②有机玻璃属于
A 复合材料 B.合成材料 C.金属材料 D.无机非金属材料
(3)水和天然气重整可以得到合成气,其反应的微观示意图如图所示:

①在微观模型A、B、C、D中,表示水分子的是
②生成物中,C和D的质量比为
(4)农业生产中,氮肥硫酸铵不能和熟石灰混合使用的原因
更新时间:2021-10-10 15:15:16
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】工业上可以空气为原料获得氮气,氮气在一定条件条件下可与某些物质发生反应。下图是以空气和其他必要的原料合成氮肥(NH4NO3)的工业流程,请按要求回答问题:
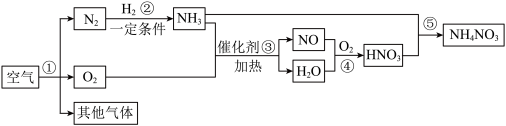
(1)步骤①中发生的是_____ 变化(填“物理”或“化学”)。
(2)写出步骤③中发生反应的符号表达式________________ 。
(3)上述化学反应中属于化合反应的有_____ 个。
(4)下图是上述流程中②发生反应的微观粒子示意图。

由图可知,反应物N2与H2的分子个数比为______ ;该反应中的最小粒子是_____ (填写化学符号)。

(1)步骤①中发生的是
(2)写出步骤③中发生反应的符号表达式
(3)上述化学反应中属于化合反应的有
(4)下图是上述流程中②发生反应的微观粒子示意图。

由图可知,反应物N2与H2的分子个数比为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】下列生活中的实例利用到的化学原理是:
(1)保温杯中,为了让茶叶与水分离,杯中通常设计了一个网状结构,其利用的原理相当于化学实验操作中的_______ 。
(2)食品包装袋常常充人氮气防腐,是因为_______ 。
(3)国六汽油是90%的普通汽油与10%的 乙醇调和而成,能有效减小对环境的污染,请 你 写出乙醇燃烧的化学方程式_______ 。
(4)春节晚会上,表演舞台的现场常有云雾的现象,通常使用物质是_______ (写化学 式)。
(1)保温杯中,为了让茶叶与水分离,杯中通常设计了一个网状结构,其利用的原理相当于化学实验操作中的
(2)食品包装袋常常充人氮气防腐,是因为
(3)国六汽油是90%的普通汽油与10%的 乙醇调和而成,能有效减小对环境的污染,请 你 写出乙醇燃烧的化学方程式
(4)春节晚会上,表演舞台的现场常有云雾的现象,通常使用物质是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】碘主要存在于海洋植物中,尤其是海带,每lkg干海带中含有816mg碘。化学兴趣小组利用灼烧法从海带中提取碘单质(I2)并验证,流程如图1:
①CCl4是一种无色、易挥发的有机溶剂,密度大于水,在水中的溶解性差,沸点为76.8℃
②I2在常温下是紫黑色固体,沸点184℃,微溶于水,易溶于CCl4呈紫红色。
(1)干海带灼烧前要剪碎并用酒精浸泡,其目的是______ 。
(2)海带灰浸出液中含有大量的碘离子(I-),利用H2O2的氧化性可将I-转化成I2,选择H2O2做氧化剂的理由是______ ,但使用时要注意在低温的原因是_______ 。(用化学方程式表示)
(3)在I2的溶液中加入CCl4,此时出现的现象是______ 。
(4)控制温度85℃对I2的CCl4溶液加热,先蒸发出来的物质是______ ,可采用的加热方式为_______ 。
(5)兴趣小组的同学又利用NaOH溶液对进行提取(图2):_______ 。
②过滤实验用到的玻璃仪器有烧杯、玻璃棒、_______ 。
③实验室用浓硫酸(溶质质量分数为98%,密度为1.84g/mL)配制196g溶质质量分数为45%的稀硫酸,需浓硫酸的体积为_______ (保留一位小数),量取浓硫酸过程中若俯视读数会导致所配溶液溶质质量分数_______ (填“偏小”,“不变”或“偏大”)。
④在I2的悬浊液中加入______ ,即可对提取出的碘进行验证。

①CCl4是一种无色、易挥发的有机溶剂,密度大于水,在水中的溶解性差,沸点为76.8℃
②I2在常温下是紫黑色固体,沸点184℃,微溶于水,易溶于CCl4呈紫红色。
(1)干海带灼烧前要剪碎并用酒精浸泡,其目的是
(2)海带灰浸出液中含有大量的碘离子(I-),利用H2O2的氧化性可将I-转化成I2,选择H2O2做氧化剂的理由是
(3)在I2的溶液中加入CCl4,此时出现的现象是
(4)控制温度85℃对I2的CCl4溶液加热,先蒸发出来的物质是
(5)兴趣小组的同学又利用NaOH溶液对进行提取(图2):
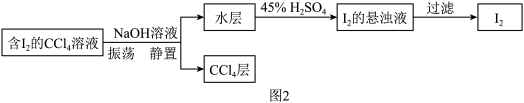
②过滤实验用到的玻璃仪器有烧杯、玻璃棒、
③实验室用浓硫酸(溶质质量分数为98%,密度为1.84g/mL)配制196g溶质质量分数为45%的稀硫酸,需浓硫酸的体积为
④在I2的悬浊液中加入
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】化学就在我们身边.

(1)土豆是我们喜爱的一种食品,上图所示是“家乡味土豆片”的主要营养成分.土豆中能为人体提供能量的营养素是________ .多食用土豆和牛奶有利于身体健康,理由是________________ .
(2)土豆等农作物的生长需要化肥.下列化肥中属于氮肥的是________ .
A.NH4Cl B. K2CO3
B. K2CO3 C. CO(NH2)2
C. CO(NH2)2 D. Ca3(PO4)2
D. Ca3(PO4)2
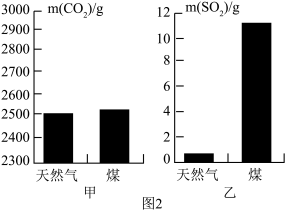
(3)贵阳市家用燃料的下列变迁,让我们认识了化学的重要价值.
充分燃烧1kg天然气和煤所产生的CO2和SO2的质量如下图所示.为此,改用天然气作燃料的优点是________ .天然气(主要成分CH4)燃烧的化学方程式为________ .
(4)氢化镁(MgH2)固体可作为氢动力汽车的能源提供剂.提供能源时MgH2与水反应生成一种碱和氢气,反应的化学方程式为________

(1)土豆是我们喜爱的一种食品,上图所示是“家乡味土豆片”的主要营养成分.土豆中能为人体提供能量的营养素是
(2)土豆等农作物的生长需要化肥.下列化肥中属于氮肥的是
A.NH4Cl
 B. K2CO3
B. K2CO3 C. CO(NH2)2
C. CO(NH2)2 D. Ca3(PO4)2
D. Ca3(PO4)2(3)贵阳市家用燃料的下列变迁,让我们认识了化学的重要价值.
煤或木柴→液化石油气或管道煤气→天然气
充分燃烧1kg天然气和煤所产生的CO2和SO2的质量如下图所示.为此,改用天然气作燃料的优点是

(4)氢化镁(MgH2)固体可作为氢动力汽车的能源提供剂.提供能源时MgH2与水反应生成一种碱和氢气,反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】如图是自然界中氮的循环图,请分析此图并回答问题。
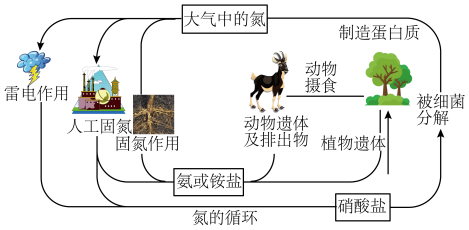
(1)大气中的氮元素主要以___________ (填化学式)存在。从空气中获取氮是人类长久以来追求的目标,图中共表示了___________ 种固氮的途径。
(2)土壤及豆科植物能进行高效固氮,该过程属于___________ (填“物理”或“化学”)变化。人工固氮是利用氮气和氢气在一定条件下合成氨气,该反应化学方程式是___________ 。
(3)氨气与硝酸化合反应生成氮肥NH4NO3,其化学方程式是___________ ,但这种肥料不适宜与___________ 性物质共用,否则会降低肥效。
(4)由图1可知,动植物体内的氮元素主要存在于___________ (填“糖类”“油脂”“蛋白质”)中,土壤中的硝酸盐会被细菌分解,有一种脱氧硫杆菌能够利用土壤中的硫化物来分解硝酸盐,其主要化学原理如下:5K2S+8KNO3+4H2O 4N2+5
4N2+5____ +8KOH ;上述过程使土壤成分发生改变,从而对农业生产造成一定不利影响,请选择任一角度进行简要说明:___________ 。

(1)大气中的氮元素主要以
(2)土壤及豆科植物能进行高效固氮,该过程属于
(3)氨气与硝酸化合反应生成氮肥NH4NO3,其化学方程式是
(4)由图1可知,动植物体内的氮元素主要存在于
 4N2+5
4N2+5
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】学习化学就是要研究物质的组成、结构、性质、变化、用途、制法等知识。
⑴判断下列物质的类别,并用相应的序号 填空
①单质②氧化物③酸④碱⑤盐
⑵按要求写化学符号:铝离子________ ;两个甲烷分子________ 。
⑶在下列横线上填写“>”、“<”、“=”。
①热稳定性:氯化钠________ 碳酸氢铵
②耐酸、耐碱性:棉纱线________ 腈纶。
⑷现有以下四种物质:A.硝酸钾B.熟石灰C.碘酒D.尼龙,根据下列要求用字母 填空:
①能用作配制波尔多液的是________ ;②可用作钓鱼线的是________ ;
⑸按要求写出方程式:
①实验室制氢气__________ ;②自然界中制取氧气的主要方法__________ 。
⑴判断下列物质的类别,并用相应的
①单质②氧化物③酸④碱⑤盐
物质化学式 | HNO3 | CuSO4 |
物质类别 |
⑶在下列横线上填写“>”、“<”、“=”。
①热稳定性:氯化钠
②耐酸、耐碱性:棉纱线
⑷现有以下四种物质:A.硝酸钾B.熟石灰C.碘酒D.尼龙,根据下列要求用
①能用作配制波尔多液的是
⑸按要求写出方程式:
①实验室制氢气
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
名校
解题方法
【推荐1】认真阅读下列材料,回答有关问题。
碘位于元素周期表的第53位,碘单质在室温下是紫黑色晶体,质软且脆,易升华,有一定的毒性和腐蚀性。碘是工业、农业、医药等行业的重要原料,也是人体不可缺少的元素之一。为了补充碘元素,在生活中我们常食用加碘食盐。超市售卖的食盐中大多添加有碘酸钾(KIO3)、碘化钾(KI)等含碘化合物。
自然界中,大部分土壤、岩石、江河湖水中的碘含量都很低,而海水中却储量丰富。此外很多海藻、海鱼和贝类等动植物体内都含有丰富的碘。某些海藻具有吸附碘的能力,如干海带中的碘的含量一般为0.3%~0.5%,比海水中碘的浓度高10万倍。
(1)碘原子的质子数(即核电荷数)是_______ 。
(2)碘酸钾(KIO3)中碘元素的化合价是_______ 价。
(3)碘是人体必需的______ 元素(填“常量”或“微量”),缺碘易引起甲状腺肿大。
碘位于元素周期表的第53位,碘单质在室温下是紫黑色晶体,质软且脆,易升华,有一定的毒性和腐蚀性。碘是工业、农业、医药等行业的重要原料,也是人体不可缺少的元素之一。为了补充碘元素,在生活中我们常食用加碘食盐。超市售卖的食盐中大多添加有碘酸钾(KIO3)、碘化钾(KI)等含碘化合物。
自然界中,大部分土壤、岩石、江河湖水中的碘含量都很低,而海水中却储量丰富。此外很多海藻、海鱼和贝类等动植物体内都含有丰富的碘。某些海藻具有吸附碘的能力,如干海带中的碘的含量一般为0.3%~0.5%,比海水中碘的浓度高10万倍。
(1)碘原子的质子数(即核电荷数)是
(2)碘酸钾(KIO3)中碘元素的化合价是
(3)碘是人体必需的
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
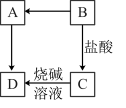
【推荐2】A、B、C、D均含有同一种金属元素,它们之间的转化关系如图(“→”表示反应可一步实现,部分物质和反应条件略去)。已知A是目前世界年产量最高的金属;B属于氧化物,其中金属元素质量分数为70%。_______ (填“常量元素”或“微量元素”)。
(2)B→A的化学方程式为_______ ;B→C的化学方程式为_______ 。
(3)A与氧气、水可以发生化合反应生成D,则D的化学式为_______ 。
(2)B→A的化学方程式为
(3)A与氧气、水可以发生化合反应生成D,则D的化学式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】日常生活、社会发展与化学密切相关。
Ⅰ.大米、番茄和牛奶是生活中常见的食品,每100 g食品中营养成分的含量如下表:
(1)表中的钙、磷、铁指的是__ (填字母序号)。
A.原子 B.单质 C.元素
(2)人体若缺少__ (填元素符号),则可能导致贫血,上表中富含该元素的食品是__ 。
(3)大米中的主要成分淀粉属于__ (填字母序号)。
A.糖类 B.油脂 C.蛋白质
(4)番茄中富含维生素C,其化学式为C6H8O6,C6H8O6中C、H、O三种元素的质量比为__ 。向维生素C溶液中滴入紫色石蕊试液,石蕊试液变红,说明维生素C溶液具有__ (填“酸性”或“碱性”)。
Ⅱ.高铁的开通不仅方便人们的出行,更助力各地经济的发展。
(5)高铁的机身采用铝合金材料,下列不属于该合金性质的是__ (填字母序号)。
A.密度大 B.耐腐蚀 C.硬度大
(6)高铁车身通过受电弓滑板与沿线架设的3万伏高压输电线相连,这是利用了受电弓滑板的______ (填“导电”或“导热”)性。
Ⅰ.大米、番茄和牛奶是生活中常见的食品,每100 g食品中营养成分的含量如下表:
| 食品 | 蛋白质/g | 脂肪/g | 糖类/g | 矿物质/mg | 维生素C/mg | ||
| 钙 | 磷 | 铁 | |||||
| 大米 | 6.7 | 0.9 | 78 | 7 | 136 | _ | 0.05 |
| 番茄 | 0.6 | 0.3 | 2 | 8 | 37 | 0.4 | 11 |
| 牛奶 | 3.1 | 3.5 | 6 | 120 | 90 | 0.1 | 1 |
A.原子 B.单质 C.元素
(2)人体若缺少
(3)大米中的主要成分淀粉属于
A.糖类 B.油脂 C.蛋白质
(4)番茄中富含维生素C,其化学式为C6H8O6,C6H8O6中C、H、O三种元素的质量比为
Ⅱ.高铁的开通不仅方便人们的出行,更助力各地经济的发展。
(5)高铁的机身采用铝合金材料,下列不属于该合金性质的是
A.密度大 B.耐腐蚀 C.硬度大
(6)高铁车身通过受电弓滑板与沿线架设的3万伏高压输电线相连,这是利用了受电弓滑板的
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】2022年2月4日,第24届冬季奥林匹克运动会在北京隆重开幕,来自世界各地的运动健儿在冰天雪地间挥洒汗水,创造奇迹。
(1)奥运会吉祥物“冰墩墩”因其外壳的设计而得名,它的硅胶外壳采用环保聚氯乙烯及聚碳酸酯制作而成,聚氯乙烯材料属于_______ (选填“合成”或“天然”)材料。
(2)在北京冬奥会期间,中国美食深受各国运动员的喜爱,例如饺子、北京烤鸭、麻婆豆腐、担担面等,其中担担面富含的营养物质是_______ 。
(3)科学家发现了一种分子结构形似奥运五环,宽度只有1.2nm,被认为是世上最小的五环标志——奥林匹克烯(C19H12),下列说法正确的是_______ 。
A.奥林匹克烯的相对分子质量为240 B.奥林匹克烯由碳、氢两种元素组成
C.每个奥林匹克烯分子中含有6个氢分子 D.奥林匹克烯中碳元素的质量分数最高
(1)奥运会吉祥物“冰墩墩”因其外壳的设计而得名,它的硅胶外壳采用环保聚氯乙烯及聚碳酸酯制作而成,聚氯乙烯材料属于
(2)在北京冬奥会期间,中国美食深受各国运动员的喜爱,例如饺子、北京烤鸭、麻婆豆腐、担担面等,其中担担面富含的营养物质是
(3)科学家发现了一种分子结构形似奥运五环,宽度只有1.2nm,被认为是世上最小的五环标志——奥林匹克烯(C19H12),下列说法正确的是
A.奥林匹克烯的相对分子质量为240 B.奥林匹克烯由碳、氢两种元素组成
C.每个奥林匹克烯分子中含有6个氢分子 D.奥林匹克烯中碳元素的质量分数最高
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】从下列选项中,选择一种适合的物质的序号填空。
①聚氯乙烯 ②碳酸钠 ③氢氧化钙 ④聚乙烯 ⑤碳酸氢钠 ⑥氢氧化钠
(1)可用作治疗胃酸过多的是______ ;
(2)可用作包装食品的是______ ;
(3)可用作改良土壤酸性的是______ 。
①聚氯乙烯 ②碳酸钠 ③氢氧化钙 ④聚乙烯 ⑤碳酸氢钠 ⑥氢氧化钠
(1)可用作治疗胃酸过多的是
(2)可用作包装食品的是
(3)可用作改良土壤酸性的是
您最近一年使用:0次
【推荐3】生活中的化学无处不在,某学生家庭晚餐菜谱:
A.米饭(200g) B.醋溜白菜(150g) C.京酱肉丝(200g) D.骨头汤(200mL)
(1)上述食物中富含多糖淀粉的是_______ (填字母)。
(2)烹调中使用了加铁酱油,酱油中加“铁”是为了防止缺铁引起的_______ 。
(3)剩菜用保鲜膜包好,保鲜膜具有_______ (填“热塑性”或“热固性”)。
(4)阅读资料卡片信息,回答①~④问题:
①“骨头汤能补钙”中的钙是指_______ (填字母);
A.钙元素 B.单质钙 C.羟基磷酸钙
②羟基磷酸钙中磷元素的化合价是_______ ;
③下列物质中不能作为人体补钙的是_______ ;(填字母);
A.牛奶 B.某品牌钙片 C.氧化钙
④若该同学只从晚餐骨头汤中获取钙,_______ (填“能、不能”)满足人体日常所需。
A.米饭(200g) B.醋溜白菜(150g) C.京酱肉丝(200g) D.骨头汤(200mL)
(1)上述食物中富含多糖淀粉的是
(2)烹调中使用了加铁酱油,酱油中加“铁”是为了防止缺铁引起的
(3)剩菜用保鲜膜包好,保鲜膜具有
(4)阅读资料卡片信息,回答①~④问题:
| 资料卡片: ①人体骨骼中的钙存在形式是羟基磷酸钙Ca10(PO4)6(OH)2,难溶于水 ②人体平均每天需要补钙约800mg ③每100mL 骨头汤约含有2mg钙 |
A.钙元素 B.单质钙 C.羟基磷酸钙
②羟基磷酸钙中磷元素的化合价是
③下列物质中不能作为人体补钙的是
A.牛奶 B.某品牌钙片 C.氧化钙
④若该同学只从晚餐骨头汤中获取钙,
您最近一年使用:0次



