用H型试管完成下列实验。
实验一:探究分子的性质

如图甲所示,将A、B管底部分别浸入盛有冷水和热水的烧杯中,同时滴入等量的浓氨水,观察到横管右侧脱脂棉上的酚酞试液先变红,请从微观角度解释这个现象:______ 。
实验二:探究燃烧的条件
已知:红磷的着火点为240℃;白磷的着火点为40℃。
(1)如图乙所示,在A、B管底部分别放置等量的红磷和白磷,塞紧橡皮塞,将A、B管底部同时浸入盛有80℃热水的水槽中,只观察到B管发生燃烧现象。原因是______ 。
(2)利用此装置探究可燃物燃烧需要空气(或氧气)。在A、B管中放置等量的白磷,在将A、B管底部同时浸入盛有80℃热水前,还需要进行的操作是______ 。
实验三:探究二氧化碳的性质
如图丙所示,B管两端开口(试纸是用石蕊溶液染过的紫色滤纸条),横管中的除杂剂可依次除去二氧化碳气体中少量氯化氢气体及水蒸气。将稀盐酸缓慢注入试管中,观察到干燥的紫色石蕊试纸均不变色、下端湿润的紫色石蕊试纸先变红。说明二氧化碳具有的性质:(1)______ ;(2)______ 。
实验四:探究物质的组成与构成
某同学根据质量守恒定律研究物质W的组成。一定条件下,W在密闭容器内发生反应,反应前后各物质的质量如下图所示:
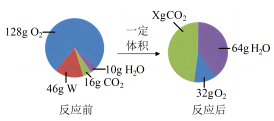
图中X=______ g。物质W由______ 种元素组成,其中碳、氢原子个数比为______ (填最简比)。
实验一:探究分子的性质

如图甲所示,将A、B管底部分别浸入盛有冷水和热水的烧杯中,同时滴入等量的浓氨水,观察到横管右侧脱脂棉上的酚酞试液先变红,请从微观角度解释这个现象:
实验二:探究燃烧的条件
已知:红磷的着火点为240℃;白磷的着火点为40℃。
(1)如图乙所示,在A、B管底部分别放置等量的红磷和白磷,塞紧橡皮塞,将A、B管底部同时浸入盛有80℃热水的水槽中,只观察到B管发生燃烧现象。原因是
(2)利用此装置探究可燃物燃烧需要空气(或氧气)。在A、B管中放置等量的白磷,在将A、B管底部同时浸入盛有80℃热水前,还需要进行的操作是
实验三:探究二氧化碳的性质
如图丙所示,B管两端开口(试纸是用石蕊溶液染过的紫色滤纸条),横管中的除杂剂可依次除去二氧化碳气体中少量氯化氢气体及水蒸气。将稀盐酸缓慢注入试管中,观察到干燥的紫色石蕊试纸均不变色、下端湿润的紫色石蕊试纸先变红。说明二氧化碳具有的性质:(1)
实验四:探究物质的组成与构成
某同学根据质量守恒定律研究物质W的组成。一定条件下,W在密闭容器内发生反应,反应前后各物质的质量如下图所示:

图中X=
更新时间:2021-11-14 23:01:08
|
相似题推荐
实验题
|
较易
(0.85)
名校
【推荐1】请根据下列装置回答问题:

(1)写出标号仪器名称:a_____ ;b _____ 。
(2)实验室用高锰酸钾制取并收集干燥的氧气时,装置应选用_____ (填字母),该发生装置不足之处是 _____ ,所发生反应的化学方程式为 _____ ,若用E装置收集,判断氧气是否收集满的方法是 _____ 。氧气收集完毕后,测得其纯度明显偏低,原因可能是: _____ (填字母,可多选);
A高锰酸钾中混入了二氧化锰B收集前,集气瓶中未注满水
C收集后,集气瓶中仍有少量水D加热前就将导管伸入集气瓶
(3)将30.9g氯酸钾(KClO3)和二氧化锰的固体混合物装入试管中,加热制取氧气,同时生成氯化钾。待反应完全后,将试管冷却,称量,可以得到21.3g固体物质。请计算原固体混合物中氯酸钾的质量。_____

(1)写出标号仪器名称:a
(2)实验室用高锰酸钾制取并收集干燥的氧气时,装置应选用
A高锰酸钾中混入了二氧化锰B收集前,集气瓶中未注满水
C收集后,集气瓶中仍有少量水D加热前就将导管伸入集气瓶
(3)将30.9g氯酸钾(KClO3)和二氧化锰的固体混合物装入试管中,加热制取氧气,同时生成氯化钾。待反应完全后,将试管冷却,称量,可以得到21.3g固体物质。请计算原固体混合物中氯酸钾的质量。
您最近一年使用:0次
实验题
|
较易
(0.85)
解题方法
【推荐2】某实验学校初三兴趣小组利用如下图所示装置(部分固定装置已略去)制备氮化钙,并探究其化学式(实验式)。

(1)按上图连接好实验装置,检查装置气密性的方法是_______ 。
(2)反应过程中末端导管必须插入试管A的水中,目的是_______ 。
(3)制备氮化钙的操作步骤是:①打开活塞K并通入N2;②点燃酒精灯,进行反应;③反应结束后,_______ ;④拆除装置,取出产物。
(4)没有U形管的可能后果是:_______ 。
(5)数据记录如下:
计算得到化学式(实验式)CaxN2,其中x=_______ 。
(6)若通入的N2中混有少量O2,则(5)中计算得到的x_______ (填“偏大”或“偏小”或“不变”)。

(1)按上图连接好实验装置,检查装置气密性的方法是
(2)反应过程中末端导管必须插入试管A的水中,目的是
(3)制备氮化钙的操作步骤是:①打开活塞K并通入N2;②点燃酒精灯,进行反应;③反应结束后,
(4)没有U形管的可能后果是:
(5)数据记录如下:
| 空硬质玻璃管质量m0/g | 硬质玻璃管与钙的质量m1/g | 硬质玻璃管与产物的质量m2/g |
| 114.8 | 120.8 | 122.2 |
(6)若通入的N2中混有少量O2,则(5)中计算得到的x
您最近一年使用:0次
实验题
|
较易
(0.85)
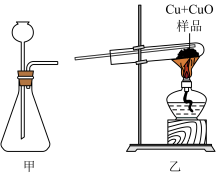
【推荐3】实验室有一瓶由铜粉和氧化铜粉末组成的固体样品。为了测定样品中各成分的质量分数,小林和小洁都利用如图甲、乙所示装置开展实验探究:从备选药品中选择所需药品在装置甲中反应,并将生成的气体通入装置乙的试管中,与所取固体样品(质量均为m)充分反应,冷却至室温后,称量试管内剩余固体质量。备选药品(足量):过氧化氢溶液、稀硫酸、二氧化锰、锌粒。
相关实验数据如表所示。
请回答下列问题:
(1)装置甲中作为反应容器的玻璃仪器的名称是______ ,小林所选药品在装置甲中发生反应的化学方程式为______ 。
(2)小林所测样品中铜粉的质量分数为______ (用含m、n的式子表示,下同),小洁所测样品中铜粉的质量分数为______ 。
(3)关于小林、小洁实验的下列说法正确的是______ (填序号)。
a.小洁实验时,必须先通入甲中生成的气体一段时间后再点燃酒精灯
b.小洁实验中,若在熄灭酒精灯后立即停止通入气体,会导致铜粉的质量分数测定值偏大
c.小林实验中,若固体样品未完全反应,会导致铜粉的质量分数测定值偏小
d.所测固体样品中铜粉和氧化铜的质量比为4:5

相关实验数据如表所示。
| 反应前固体样品质量 | 反应后剩余固体质量 | |
| 小林实验数据 | m | m+n |
| 小洁实验数据 | m | m﹣n |
(1)装置甲中作为反应容器的玻璃仪器的名称是
(2)小林所测样品中铜粉的质量分数为
(3)关于小林、小洁实验的下列说法正确的是
a.小洁实验时,必须先通入甲中生成的气体一段时间后再点燃酒精灯
b.小洁实验中,若在熄灭酒精灯后立即停止通入气体,会导致铜粉的质量分数测定值偏大
c.小林实验中,若固体样品未完全反应,会导致铜粉的质量分数测定值偏小
d.所测固体样品中铜粉和氧化铜的质量比为4:5
您最近一年使用:0次
实验题
|
较易
(0.85)
名校
解题方法
【推荐1】化学是以实验为基础的科学,根据以下实验探究回答下列问题。

(1)甲中同时向烧杯中加入等量品红,静置,发现整杯热水变红的时间比冷水短。请从微观角度分析,这是因为___________ 。
(2)根据乙中铜片上的不同现象可得出燃烧需要条件是___________ 。
(3)丙的目的是探究___________ (填物质名称)对铁生锈有无影响。
(4)丁实验的现象是___________ ,可得到的结论是___________ 。

(1)甲中同时向烧杯中加入等量品红,静置,发现整杯热水变红的时间比冷水短。请从微观角度分析,这是因为
(2)根据乙中铜片上的不同现象可得出燃烧需要条件是
(3)丙的目的是探究
(4)丁实验的现象是
您最近一年使用:0次
实验题
|
较易
(0.85)
解题方法
【推荐2】某兴趣小组做以下实验探究分子的运动,如下图所示。请回答实验中的有关问题:

查阅资料:浓氨水是一种无色、有刺激性气味、易挥发的液体,它能使无色的酚酞试液变红。
(1)实验1:在盛有少量蒸馏水的小烧杯中滴入2~3滴酚酞试液,现象是__________ ;
(2)实验2(如图甲所示):烧杯B的现象是________ ;
(3)为使实验结论准确可靠,该兴趣小组设计实验3(如图乙所示)作为对比实验,你认为有无必要?________ 。
(4)该实验的结论是__________ 。

查阅资料:浓氨水是一种无色、有刺激性气味、易挥发的液体,它能使无色的酚酞试液变红。
(1)实验1:在盛有少量蒸馏水的小烧杯中滴入2~3滴酚酞试液,现象是
(2)实验2(如图甲所示):烧杯B的现象是
(3)为使实验结论准确可靠,该兴趣小组设计实验3(如图乙所示)作为对比实验,你认为有无必要?
(4)该实验的结论是
您最近一年使用:0次
【推荐1】根据下列实验装置图回答问题。

(1)仪器a的名称是_______ 。
(2)实验室用A、F组合制取并收集氧气,发生反应的化学方程式为_______ 。实验结束后,应先将导管移出水面,再熄灭酒精灯,原因是_______ 。
(3)实验室用块状大理石和稀盐酸制取二氧化碳,若想控制反应的发生与停止,应选择的发生与收集装置分别是_______ (填字母)。
(4)装置G可观察到湿润纸花变红,使其变红的物质是________ (填化学式)。

(1)仪器a的名称是
(2)实验室用A、F组合制取并收集氧气,发生反应的化学方程式为
(3)实验室用块状大理石和稀盐酸制取二氧化碳,若想控制反应的发生与停止,应选择的发生与收集装置分别是
(4)装置G可观察到湿润纸花变红,使其变红的物质是
您最近一年使用:0次
实验题
|
较易
(0.85)
解题方法
【推荐2】请根据图1实验装置图回答问题:

(1)写出仪器a,b的名称:a是_______ ,b是_______ 。
(2)用A装置制取氧气的化学方程式是_______ ,可选用的收集装置是_______ (填序号)。
(3)实验室制取二氧化碳气体应选用的发生装置是___ (填序号),有关的化学方程式是___ 。
(4)将一瓶二氧化碳气体正立于烧杯中(装置见图2),敞口一会儿,集气瓶外壁上湿润的蓝色石蕊试纸自上面而下变_______ 色,该现象说明二氧化碳气体_______ ,_______ 。

(1)写出仪器a,b的名称:a是
(2)用A装置制取氧气的化学方程式是
(3)实验室制取二氧化碳气体应选用的发生装置是
(4)将一瓶二氧化碳气体正立于烧杯中(装置见图2),敞口一会儿,集气瓶外壁上湿润的蓝色石蕊试纸自上面而下变
您最近一年使用:0次
实验题
|
较易
(0.85)
解题方法
【推荐3】化学是一门以实验为基础的科学。根据如图回答问题。

(1)写出图中标字母的仪器名称:a___________ ;b___________ ;
(2)实验室用过氧化氢溶液和二氧化锰混合物制取氧气,反应的化学方程式为___________ ,若要控制液体滴加速率获得平稳气流,应选择的发生装置是___________ ;实验室用C装置制氧气的化学方程式为___________ ;
(3)如果用G收集二氧化碳,二氧化碳气体从___________ (填m或n)通入;
(4)如图装置H,将二氧化碳气体通入紫色石蕊中观察到的现象是___________ ,反应的化学方程式是___________ 。

(1)写出图中标字母的仪器名称:a
(2)实验室用过氧化氢溶液和二氧化锰混合物制取氧气,反应的化学方程式为
(3)如果用G收集二氧化碳,二氧化碳气体从
(4)如图装置H,将二氧化碳气体通入紫色石蕊中观察到的现象是
您最近一年使用:0次
实验题
|
较易
(0.85)
解题方法
【推荐1】用图装置验证可燃物燃烧的条件。

已知:白磷着火点为40℃,红磷着火点为240℃。
(1)实验中,利用了铜片的物理性质是___________ 。
(2)实验中的现象___________ 。
(3)该实验能证明可燃物燃烧的一个条件是___________ 。
(4)用该装置验证可燃物燃烧的另一个条件,应补充的操作是___________ 。

已知:白磷着火点为40℃,红磷着火点为240℃。
(1)实验中,利用了铜片的物理性质是
(2)实验中的现象
(3)该实验能证明可燃物燃烧的一个条件是
(4)用该装置验证可燃物燃烧的另一个条件,应补充的操作是
您最近一年使用:0次
【推荐2】如图是初中化学一些重要实验,请回答下列问题:

(1)实验A:实验结束后进入集气瓶中水的体积多于瓶内原气体体积的 ,造成该现象的原因是
,造成该现象的原因是_______ (答一条)。
(2)实验B:从下面进水,上面出水的优点_______ (答一条)。
(3)实验C:该操作的不良后果_______ 。
(4)实验D:通过实验现象可知,物质的溶解性与_______ 有关。

(1)实验A:实验结束后进入集气瓶中水的体积多于瓶内原气体体积的
 ,造成该现象的原因是
,造成该现象的原因是(2)实验B:从下面进水,上面出水的优点
(3)实验C:该操作的不良后果
(4)实验D:通过实验现象可知,物质的溶解性与
您最近一年使用:0次
实验题
|
较易
(0.85)
解题方法
【推荐3】碳酸铈广泛应用于汽车发动机尾气净化剂、化工催化剂等。人们对稀土产品的质量指标要求越来越高,某客户对高纯度碳酸铈中氯离子的含量提出了小于 50ppm 的要求。为此,某课题组以氯化铈液为原料,浓度为 150g/L 的碳酸氢铵溶液为沉淀剂,研究条件对氯离子含量的影响。相关数据如下:
(1)本实验研究了哪些因素对氯离子含量的影响_____ 。
(2)实验 1、2 的目的是_____ 。
(3)为符合客户要求,应选用的的工艺方法为_____ (填编号)。
| 编号 | pH | 料液浓度(g/L) | 沉淀时间 (min) | 碳酸氢铵溶液浓度配制时间 | C1-(ppm) |
| 1 | 1.0-1.5 | 30 | 120 | 一天 | 246 |
| 2 | 3.5-4.0 | 30 | 120 | 一天 | 37 |
| 3 | 3.5-4.0 | 65 | 120 | 一天 | 65 |
| 4 | 3.5-4.0 | 100 | 120 | 一天 | 80 |
| 5 | 3.5-4.0 | 30 | 90 | 一天 | 80 |
| 6 | 3.5-4.0 | 30 | 150 | 一天 | 75 |
(1)本实验研究了哪些因素对氯离子含量的影响
(2)实验 1、2 的目的是
(3)为符合客户要求,应选用的的工艺方法为
您最近一年使用:0次




