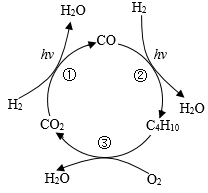
24.8g过氧化银(Ag2O2)在真空条件下加热至固体质量不再发生变化,产生3.2gO2。固体质量随温度的变化如图所示。下列说法不正确的是


| A.X→W过程中,固体中银元素的质量分数保持不变 |
B.X→Y过程中,发生的反应为 |
| C.Z→W过程中产生的氧气质量为1.6g |
| D.W点对应的固体为Ag |
更新时间:2021-12-05 13:09:02
|
相似题推荐
选择题-单选题
|
较难
(0.4)
【推荐1】有化学反应 3A+B+2C=D,将 A、B、C 各15g 混合均匀后加热,生成了30gD。向残留物中加入10g A 后,反应又继续开始,待反应再次停止后反应物中只剩余 C。以下说法中正确的是( )
| A.第一次反应停止时 B 剩余了9g | B.第一次反应停止时 C 剩余了6g |
| C.反应中 A 和 C 的质量比为 5:3 | D.第二次反应后 C 剩余了5g |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
解题方法
【推荐2】某物质6.0g完全燃烧后,生成17.6g二氧化碳和10.8g水,则关于该物质的说法正确的是( )
| A.只含有碳、氢元素 | B.一定含有碳、氢、氧三种元素 |
| C.条件不足、无法判断 | D.一定含有碳、氢元素,可能含有氧元素 |
您最近一年使用:0次
选择题-选择题组
|
较难
(0.4)
【推荐1】阅读下列材料,完成下面小题。
中国古代四大发明之一的黑火药是由木炭、硫磺和硝酸钾按一定比例混合而成的。黑火药爆炸时发生的主要反应是:S+2KNO3+3C K2S+X↑+3CO2↑
K2S+X↑+3CO2↑
古代曾以硝土[含硝酸钙、少量氯化钠、不溶于水的一些杂质等]和草木灰(含碳酸钾)为原料制取硝酸钾。某化学兴趣小组设计了如下实验流程:
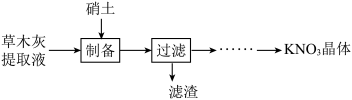

1.黑火药爆炸时产生的物质X是
2.下列化学用语中的数字“0”或“3”可以表示分子个数的是
3.能正确表示“制备”过程中发生反应的化学方程式为
4.将滤液加热蒸发浓缩后,再冷却至低温结晶,可得到纯度较高的硝酸钾晶体。下列说法不正确的是
中国古代四大发明之一的黑火药是由木炭、硫磺和硝酸钾按一定比例混合而成的。黑火药爆炸时发生的主要反应是:S+2KNO3+3C
 K2S+X↑+3CO2↑
K2S+X↑+3CO2↑古代曾以硝土[含硝酸钙、少量氯化钠、不溶于水的一些杂质等]和草木灰(含碳酸钾)为原料制取硝酸钾。某化学兴趣小组设计了如下实验流程:


1.黑火药爆炸时产生的物质X是
| A.N2 | B.N2O | C.NO | D.N2O4 |
A.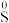 | B.KNO3 | C.3C | D.3CO2 |
| A.Ca(NO3)2+KCO3=CaCO3↓+KNO3 | B.Ca(NO3)2+K2CO3=CaCO3↓+KNO3 |
| C.Ca(NO3)2+K2CO3=CaCO3↓+2KNO3 | D.Ca(NO3)2+K2CO3=CaCO3+KNO3 |
| A.滤液中一定含硝酸钾和氯化钠 |
| B.加热蒸发浓缩的目的是为了形成硝酸钾的热饱和溶液 |
| C.冷却至低温时,硝酸钾会大量结晶析出 |
| D.冷却至低温时,氯化钠较难析出的原因是氯化钠的溶解度受温度影响不明显 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
解题方法
【推荐2】天然气因含有少量H2S等气体开采应用受限。T.F菌在酸性溶液中可实现天然气的催化脱硫,其原理如图所示。下列说法正确的是

| A.该脱硫过程需要不断添加Fe2(SO4)3溶液 |
| B.脱硫过程中,理论上每生成32g硫,需要消耗32g氧气 |
| C.反应过程i,属于置换反应 |
| D.整个过程中有三种元素化合价发生了变化 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
解题方法
【推荐1】将乙酸(CH3COOH)和葡萄糖(C6H12O6)溶于水得到混合溶液,测得溶液中氢元素的质量分数为8%,则溶液中碳元素的质量分数为
| A.8% | B.28% | C.38% | D.48% |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
解题方法
【推荐2】现有120g碳酸钙和氧化钙的混合物,高温煅烧充分反应后得到固体剩余物84g,则原混合物中钙元素的质量分数是
| A.20% | B.50% | C.60% | D.75% |
您最近一年使用:0次