以高纯度的二氧化锰为原料制备高锰酸钾的主要流程如下
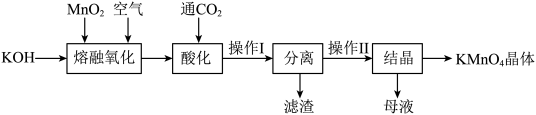
(1)融化氧化时,也可以用氯酸钾代替空气,原因是______ 。
(2)操作I中玻璃棒的作用是______ ;
(3)“酸化”时反应的化学方程式为: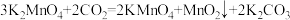 ,该反应中锰元素的转化率(所得高锰酸钾中锰元素与反应物中锰元素的质量百分比)为
,该反应中锰元素的转化率(所得高锰酸钾中锰元素与反应物中锰元素的质量百分比)为______ (精确到小数点后一位)。
(4)操作Ⅱ是根据KMnO4和K2CO3两种物质在溶解性上的差异将两者分离。具体操作步骤为:蒸发浓缩、降温结晶,过滤,洗涤干燥,得KMnO4晶体。则两者中______ (填化学式)的溶解度受温度影响变化更大,母液是高锰酸钾的______ 溶液(填“饱和”或“不饱和”)。蒸发过程中温度不宜过高,原因是______ (用方程式表示)。
(5)本流程中可以循环利用的物质是______ 。
(6)电解法也可以实现由K2MnO4向KMnO4的转化,与“通CO2”相比,其优点是______ (填字母,该反应的化学方程式为: )。
)。
a.节约能源b.锰元素转化率高c.得到的KOH可以循环利用d.可以同时获得氢气

(1)融化氧化时,也可以用氯酸钾代替空气,原因是
(2)操作I中玻璃棒的作用是
(3)“酸化”时反应的化学方程式为:
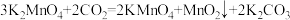 ,该反应中锰元素的转化率(所得高锰酸钾中锰元素与反应物中锰元素的质量百分比)为
,该反应中锰元素的转化率(所得高锰酸钾中锰元素与反应物中锰元素的质量百分比)为(4)操作Ⅱ是根据KMnO4和K2CO3两种物质在溶解性上的差异将两者分离。具体操作步骤为:蒸发浓缩、降温结晶,过滤,洗涤干燥,得KMnO4晶体。则两者中
(5)本流程中可以循环利用的物质是
(6)电解法也可以实现由K2MnO4向KMnO4的转化,与“通CO2”相比,其优点是
 )。
)。a.节约能源b.锰元素转化率高c.得到的KOH可以循环利用d.可以同时获得氢气
更新时间:2021-12-22 23:44:21
|
相似题推荐
填空与简答-科普阅读题
|
适中
(0.65)
名校
【推荐1】在能源需求庞大的今天,科学家都在尽可能开发新能源。其中太阳能因其可再生、对环境无污染、分布广等优点而备受科学家的青睐。太阳能电池也因此应运而生。制作太阳能电池主要是以半导体材料为基础,其工作原理是利用光电材料吸收光能后发生光电转换反应。太阳能电池有多种,硅太阳能电池就是其中的一种。晶体硅为灰黑色,金属光泽。熔点高,硬度大,质地脆。工业上用石英(主要成分为SiO2)制备粗硅的反应为:SiO2+2C==Si+2X↑,实验室里可用镁粉在赤热下还原粉状二氧化硅发生置换反应,用稀酸洗去生成的氧化镁和镁粉,再用氢氟酸洗去未作用的二氧化硅,即得单质硅。
请依据上文回答下列问题:
(1)硅太阳能电池是将______ 能转化为______ 能。
(2)硅的物理性质______ (请描述1点)。
(3)文章中x的化学式为______ 。
(4)请写出实验室制取硅单质的化学方程式______ 。
请依据上文回答下列问题:
(1)硅太阳能电池是将
(2)硅的物理性质
(3)文章中x的化学式为
(4)请写出实验室制取硅单质的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
【推荐2】煤是重要的化石燃料之一,下图是煤的精炼和综合利用的流程图。
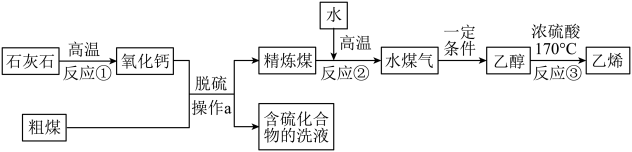
(1)反应①的化学方程式为__________ 。
(2)“脱硫”的目的是减少二氧化硫的排放,二氧化硫对环境的影响主要是________ 。
A 臭氧层空洞
B 沙尘暴
C 雾霾
D 酸雨
(3)脱硫时可以得到石膏(CaSO4﹒2H2O),发生的总反应为: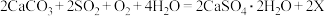 ,则X的化学式为
,则X的化学式为 _________ 。操作a的名称是 _____________ 。

(1)反应①的化学方程式为
(2)“脱硫”的目的是减少二氧化硫的排放,二氧化硫对环境的影响主要是
A 臭氧层空洞
B 沙尘暴
C 雾霾
D 酸雨
(3)脱硫时可以得到石膏(CaSO4﹒2H2O),发生的总反应为:
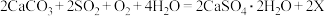 ,则X的化学式为
,则X的化学式为
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐3】阅读下面科普短文,回答问题。
石墨烯是一种单层碳原子晶体,石墨烯的厚度只有0.335nm, 是目前为止最薄的二维 纳米碳材料。石墨烯具有优良的性能,在纺织、电子等领域具有广泛应用。纺织领域是石 墨烯应用的新兴领域,纺织面料中掺入石墨烯后,在低温情况下,石墨烯可将来自远红外线 的热量传送给人体,改善人体微循环系统,促进新陈代谢。石墨烯晶体管的传输速度远远 超过目前的硅晶体管,因此有希望应用于全新超级计算机的研发。科学家用一种非常简单 易行的机械剥离法得到石墨烯之后,制备石墨烯的新方法层出不穷,工业上可采用甲烷气 体(CH4)在高温和Cu-Pd 催化下分解制取石墨烯,同时产生氢气。随着科技水平的提升,石墨烯的应用前景会十分广阔。
(1)石墨和金刚石都是由碳元素组成的单质,但它们的物理性质存在明显差异,原因是_______ (从微观角度分析)。
(2)从材料可知,石墨烯在纺织面料中的作用是_______ 。
(3)下列有关说法中正确的是 (填字母)。
(4)请写出工业上制取石墨烯的化学方程式_____ 。
石墨烯是一种单层碳原子晶体,石墨烯的厚度只有0.335nm, 是目前为止最薄的二维 纳米碳材料。石墨烯具有优良的性能,在纺织、电子等领域具有广泛应用。纺织领域是石 墨烯应用的新兴领域,纺织面料中掺入石墨烯后,在低温情况下,石墨烯可将来自远红外线 的热量传送给人体,改善人体微循环系统,促进新陈代谢。石墨烯晶体管的传输速度远远 超过目前的硅晶体管,因此有希望应用于全新超级计算机的研发。科学家用一种非常简单 易行的机械剥离法得到石墨烯之后,制备石墨烯的新方法层出不穷,工业上可采用甲烷气 体(CH4)在高温和Cu-Pd 催化下分解制取石墨烯,同时产生氢气。随着科技水平的提升,石墨烯的应用前景会十分广阔。
(1)石墨和金刚石都是由碳元素组成的单质,但它们的物理性质存在明显差异,原因是
(2)从材料可知,石墨烯在纺织面料中的作用是
(3)下列有关说法中正确的是 (填字母)。
| A.石墨烯是由碳原子构成的 |
| B.石墨烯材料在常温下化学性质稳定 |
| C.石墨烯与氧气反应只会生成 CO2 |
| D.石墨烯有希望应用于全新超级计算机的研发 |
(4)请写出工业上制取石墨烯的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】A-E是初中化学常见的物质,它们之间的转化关系如下图所示(“—”表示相邻的两物质可以发生反应,“→”表示箭头前面的物质可以转化为箭头后面的物质;部分反应的反应物、生成物和反应条件没有标出)。其中A为白色固体,B、C的物质状态相同,A、B、D、E含有一种相同的元素,请回答下列问题:

(1)写出物质A的化学式:______ ;
(2)A→B属于_____ 反应(填基本反应类型);
(3)写出E→B的符号表达式:_______ ;
(4)写出C→D反应的符号表达式:______ 。

(1)写出物质A的化学式:
(2)A→B属于
(3)写出E→B的符号表达式:
(4)写出C→D反应的符号表达式:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】以化合价为纵坐标,以物质的类别为横坐标所绘制的图像叫价类图。如图为氯元素的价图,请分析该图后填写:

(1)请依次写出A、B两点所代表的物质的化学式:_______ 、_______ ;
(2)C常用于实验室制取氧气,同时生成D,请写出C→D的化学方程式_______ ;
(3)已知构成D物质的微粒和构成NaCl的微粒种类相同。所以D物质是由K+和_______ 构成的(用化学符号表示)。

(1)请依次写出A、B两点所代表的物质的化学式:
(2)C常用于实验室制取氧气,同时生成D,请写出C→D的化学方程式
(3)已知构成D物质的微粒和构成NaCl的微粒种类相同。所以D物质是由K+和
您最近一年使用:0次
【推荐1】溶液在日常生活、工农业生产和科学研究中具有广泛用途。

(1)KNO3属于复合肥,所含的营养元素有_________ ;溶质质量分数为3%的KNO3溶液常用作无土栽培的营养液,配制100g该营养液需要KNO3的质量为_________ g,配制时常用玻璃棒搅拌,目的是___________ 。
(2)如图1,60℃时KNO3的溶解度为________ g:某KNO3固体(混有少量NaCl),可采用___________ (填“降温结晶”或“蒸发结晶”)的方法提纯该固体中的KNO3:
(3)如图2是探究温度对溶解度的影响。固体X是NH4NO3或NaOH,固体Y是KNO3或Ca(OH)2,烧杯中盛放20℃Y的饱和溶液(有少量Y的固体剩余),往试管中滴入适量水,烧杯中固体逐渐消失,写出X与Y可能的1种组合_________ 。

(1)KNO3属于复合肥,所含的营养元素有
(2)如图1,60℃时KNO3的溶解度为
(3)如图2是探究温度对溶解度的影响。固体X是NH4NO3或NaOH,固体Y是KNO3或Ca(OH)2,烧杯中盛放20℃Y的饱和溶液(有少量Y的固体剩余),往试管中滴入适量水,烧杯中固体逐渐消失,写出X与Y可能的1种组合
您最近一年使用:0次
【推荐2】海洋是一个巨大的资源宝库。
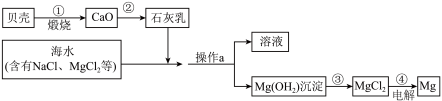
(1)金属镁广泛应用于火箭、导弹和飞机制造业,目前世界上60%的镁是从海水(主要含NaCl和MgCl2)中提取的。主要步骤如下图所示,试回答以下问题:

写出过程步骤②反应的化学方程式________ ,该反应属于_____ (填“化合”“分解”“置换”“复分解”之一)反应。海水或卤水中本来就含有氯化镁,为什么还要经过①②两个步骤,重新制得氯化镁?原因是____________ 。
(2)海水中除了蕴含大量的钠元素和镁元素外,还含有大量的钾元素。KCl和KNO3的溶解度曲线如图所示,试回答下列问题:
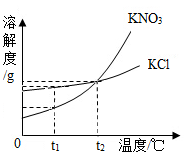
①在____________ ℃时,KCl和KNO3的溶解度相等。
②已知30℃时,KNO3的溶解度为46g。30℃时,向50g水中加入28g KNO3固体,形成的溶液是此温度下KNO3的__________ (填“饱和”或“不饱和”之一)溶液。此时溶液中溶质质量分数为___________ (计算结果精确至0.1%)。
③当KNO3固体中含有少量KCl时,可采用__________ 的方法提纯KNO3(填“降温结晶”、“蒸发结晶”之一)。
(3)海底不仅蕴藏着大量的煤、石油、天然气等常规化石燃料,人们还在海底发现了一种新型矿产资源——“可燃冰”。请写出“可燃冰”充分燃烧的反应的化学方程式_________ ;下列有关“可燃冰”的说法正确的是___________ 。

A.“可燃冰”是可再生能源
B.“可燃冰”燃烧产物只有水,无污染
C.“可燃冰”热值高,燃烧后几乎不产生任何残渣和废气,被誉为“未来能源”
(4)从浩瀚的海洋中获取淡水,对解决淡水危机具有重要意义。下列方法中能淡化海水的是_______(填字母)。
(1)金属镁广泛应用于火箭、导弹和飞机制造业,目前世界上60%的镁是从海水(主要含NaCl和MgCl2)中提取的。主要步骤如下图所示,试回答以下问题:

写出过程步骤②反应的化学方程式
(2)海水中除了蕴含大量的钠元素和镁元素外,还含有大量的钾元素。KCl和KNO3的溶解度曲线如图所示,试回答下列问题:

①在
②已知30℃时,KNO3的溶解度为46g。30℃时,向50g水中加入28g KNO3固体,形成的溶液是此温度下KNO3的
③当KNO3固体中含有少量KCl时,可采用
(3)海底不仅蕴藏着大量的煤、石油、天然气等常规化石燃料,人们还在海底发现了一种新型矿产资源——“可燃冰”。请写出“可燃冰”充分燃烧的反应的化学方程式

A.“可燃冰”是可再生能源
B.“可燃冰”燃烧产物只有水,无污染
C.“可燃冰”热值高,燃烧后几乎不产生任何残渣和废气,被誉为“未来能源”
(4)从浩瀚的海洋中获取淡水,对解决淡水危机具有重要意义。下列方法中能淡化海水的是_______(填字母)。
| A.过滤法 | B.多级闪急蒸馏法 | C.沉淀法 | D.分解法 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】下图为甲、乙、丙三种不含结晶水的固体物质溶解度曲线,据图回答:

①图中___________ 物质的溶解度曲线与气体物质溶解度曲线受温度影响变化相似。
②t1℃时,25g甲物质的饱和溶液中,含甲物质________ 克。
③t3℃时,取等质量甲、乙、丙三种物质分别配制成饱和溶液,所得溶液质量最小的是_________ 物质。
④现有甲、乙、丙三种物质的浓溶液,可用海水晒盐原理进行结晶提纯的是__________ 物质。
⑤下列叙述中错误的是__________ 。

①图中
②t1℃时,25g甲物质的饱和溶液中,含甲物质
③t3℃时,取等质量甲、乙、丙三种物质分别配制成饱和溶液,所得溶液质量最小的是
④现有甲、乙、丙三种物质的浓溶液,可用海水晒盐原理进行结晶提纯的是
⑤下列叙述中错误的是
| A.t1℃时,甲、乙、丙三种物质溶液的溶质质量分数可能相等 |
| B.t2℃时,甲、乙物质溶解度相等,则两种溶液的溶质质量分数也相等 |
| C.t1℃时,甲、乙、丙三种物质的溶液分别升温(溶剂不蒸发),丙物质溶液浓度可能发生改变 |
| D.t3℃时,甲、乙、丙三种物质的饱和溶液降温到t1℃时,析出晶体最多是甲物质 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
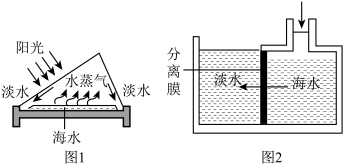
【推荐1】海水淡化常用太阳能蒸馏和膜分离等方法,根据图示回答问题。_____ (物理/化学)变化。太阳能蒸馏淡化的优点是_____ 。
(2)膜分离的原理上图如图2所示。将海水加压,水分子能透过分离膜, 和
和 却不能透过,一段时间后,右侧海水中氯化钠的质量分数
却不能透过,一段时间后,右侧海水中氯化钠的质量分数_____ (变大/变小/不变)。膜分离的原理与化学实验中物质分离的_____ (操作方法)相似。
(2)膜分离的原理上图如图2所示。将海水加压,水分子能透过分离膜,
 和
和 却不能透过,一段时间后,右侧海水中氯化钠的质量分数
却不能透过,一段时间后,右侧海水中氯化钠的质量分数
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】锂电池在新能源产业链中,有着不可替代的价值。如图是从钴酸锂(LiCoO2)废电极片中回收得到Co2O3和Li2 CO3的工艺流程。
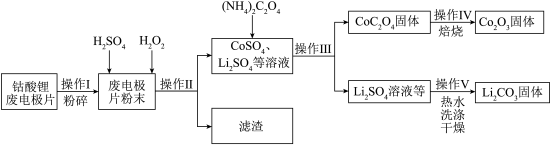
(1)操作I中,粉碎废电极片的目的是______ 。
(2)操作Ⅱ和操作Ⅲ的名称是______ 。
(3)操作IV中,在高温条件下,CoC2O4在空气中反应生成Co2O3和CO2,反应的化学方程式为______ 。
(4)操作V中,加入沉淀剂得到Li2CO3固体,用热水洗涤Li2CO3固体表面的杂质,比用冷水洗涤损耗更少,说明Li2CO3的溶解度随温度升高而______ 。
(5)若20g钴酸锂废电极片经过上述回收过程,最终得到16.6gCo2O3和7.4 g Li2CO3固体,不考虑物质损失的情况下,原废电极片中钴元素和锂元素质量的最简整数比为______ 。

(1)操作I中,粉碎废电极片的目的是
(2)操作Ⅱ和操作Ⅲ的名称是
(3)操作IV中,在高温条件下,CoC2O4在空气中反应生成Co2O3和CO2,反应的化学方程式为
(4)操作V中,加入沉淀剂得到Li2CO3固体,用热水洗涤Li2CO3固体表面的杂质,比用冷水洗涤损耗更少,说明Li2CO3的溶解度随温度升高而
(5)若20g钴酸锂废电极片经过上述回收过程,最终得到16.6gCo2O3和7.4 g Li2CO3固体,不考虑物质损失的情况下,原废电极片中钴元素和锂元素质量的最简整数比为
您最近一年使用:0次