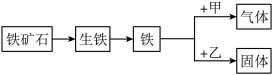
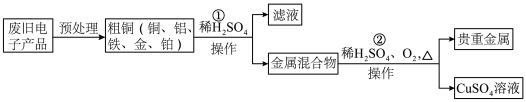
某兴趣小组的同学从实验室收集到一桶含有FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体(FeSO4·7H2O),设计了如下实验方案,请回答下列问题:
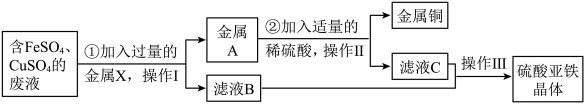
(1)操作Ⅰ、Ⅱ都为________ ;
(2)步骤①中,金属X是________ ,该反应的化学方程式为__________ ;
(3)步骤②中,加稀硫酸的目的是__________ ,该反应的化学方程式为_________ ;
(4)滤液B、C中的溶质是_________ ;
(5)操作Ⅲ中,玻璃棒的作用是________ 。

(1)操作Ⅰ、Ⅱ都为
(2)步骤①中,金属X是
(3)步骤②中,加稀硫酸的目的是
(4)滤液B、C中的溶质是
(5)操作Ⅲ中,玻璃棒的作用是
更新时间:2021-12-23 07:03:49
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】化学兴趣小组在一定质量的AgNO3、Cu(NO3)2和Fe(NO3)2的混合溶液中加入锌粉,溶液质量变化如图所示:

(1)写出a点发生反应的化学方程式________ 。
(2)m1~m2之间溶液质量增重的原因________ 。
(3)b点溶液中的溶质有哪些_______ 。

(1)写出a点发生反应的化学方程式
(2)m1~m2之间溶液质量增重的原因
(3)b点溶液中的溶质有哪些
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐2】氧化锌广泛地应用于塑料、合成橡胶、药膏等产品的制作中。
Ⅰ.氧化锌的制备利用氧化锌矿(含少量CuO、NiO)为原料制备高纯氧化锌的流程如下:

已知:①金属活动性Fe>Ni>H;
②碳酸氢铵1000元/吨,碳酸钠2650元/吨。
(1)为提高锌浸出率,可以采取的生产条件是_______ 。
(2)“酸溶”后溶液中含有的阳离子有Zn2+、Ni2+、_______ 。
(3)“过滤I”所得滤渣中所含的金属有_______ (填化学式)。
(4)“反应”可加入碳酸钠制备碱式碳酸锌,反应原理为:3Na2CO3+3ZnSO4+3H2O=ZnCO3·2Zn(OH)2·H2O↓+3Na2SO4+2CO2↑。亦可采用新工艺,即选用碳酸氢铵来代替碳酸钠制备碱式碳酸锌,反应原理为6NH4HCO3+3ZnSO4=ZnCO3·2Zn(OH)2·H2O↓+3(NH4)2SO4+5CO2↑。
①选用碳酸氢铵来代替碳酸钠制备碱式碳酸锌的优点是_______ 。
②新工艺常控制在40°C条件下进行,其目的是________ 。
Ⅱ.氧化锌的应用炉甘石始栽于《外丹本草》,主要成分为碳酸锌(ZnCO3)和碱式碳酸锌,炮制后主要成分为氧化锋(ZnO),可添加至药膏用作外用药。
(5)氧化锌、碳酸锌、碱式碳酸锌都有一定的抑菌活性,说明起抑菌作用的有效成分可能是锌_______ (选填“单质”或“元素”)。
(6)药效高低与有效成分的含量相关。碳酸锌的抑菌活性低于相同质量的氧化锌,可能的原因是_______ 。
Ⅰ.氧化锌的制备利用氧化锌矿(含少量CuO、NiO)为原料制备高纯氧化锌的流程如下:

已知:①金属活动性Fe>Ni>H;
②碳酸氢铵1000元/吨,碳酸钠2650元/吨。
(1)为提高锌浸出率,可以采取的生产条件是
(2)“酸溶”后溶液中含有的阳离子有Zn2+、Ni2+、
(3)“过滤I”所得滤渣中所含的金属有
(4)“反应”可加入碳酸钠制备碱式碳酸锌,反应原理为:3Na2CO3+3ZnSO4+3H2O=ZnCO3·2Zn(OH)2·H2O↓+3Na2SO4+2CO2↑。亦可采用新工艺,即选用碳酸氢铵来代替碳酸钠制备碱式碳酸锌,反应原理为6NH4HCO3+3ZnSO4=ZnCO3·2Zn(OH)2·H2O↓+3(NH4)2SO4+5CO2↑。
①选用碳酸氢铵来代替碳酸钠制备碱式碳酸锌的优点是
②新工艺常控制在40°C条件下进行,其目的是
Ⅱ.氧化锌的应用炉甘石始栽于《外丹本草》,主要成分为碳酸锌(ZnCO3)和碱式碳酸锌,炮制后主要成分为氧化锋(ZnO),可添加至药膏用作外用药。
(5)氧化锌、碳酸锌、碱式碳酸锌都有一定的抑菌活性,说明起抑菌作用的有效成分可能是锌
(6)药效高低与有效成分的含量相关。碳酸锌的抑菌活性低于相同质量的氧化锌,可能的原因是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】向Cu(NO3)2、Al(NO3)3和AgNO3的混合溶液中加入一定量的锌粉,反应过程中溶液质量的变化如图所示。充分反应后过滤,向所得固体上滴加稀盐酸。

(1)写出AB段发生反应的化学方程式____ 。
(2)写出 点溶液中溶质的化学式
点溶液中溶质的化学式____ 。
(3)证明锌粉过量的实验现象是什么?_____ 。

(1)写出AB段发生反应的化学方程式
(2)写出
 点溶液中溶质的化学式
点溶液中溶质的化学式(3)证明锌粉过量的实验现象是什么?
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】复印机的墨粉中含有Fe3O4粉末。其制备的主要流程如下:

(1)①中反应的化学方程式为_______ ;
(2)试剂X为_______ ;
(3)操作Y为_______ ;
(4)现有168kg铁粉,假设该过程没有铁损失,理论上可制得Fe3O4的质量为_______ kg。

(1)①中反应的化学方程式为
(2)试剂X为
(3)操作Y为
(4)现有168kg铁粉,假设该过程没有铁损失,理论上可制得Fe3O4的质量为
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】水是生命之源,也是人类宝贵的资源,请回答下列问题:
(1)下列“水”属于纯净物的是______(填序号)。
(2)生活中为降低水的硬度并杀灭水中病原生物,可采用的方法是_______ 。
(3)实验室中常通过______ 的操作来除去水中不溶性的杂质,该操作需要用到的玻璃仪器有烧杯、________ 、玻璃棒,其中玻璃棒的作用是________ 。
(1)下列“水”属于纯净物的是______(填序号)。
| A.蒸馏水 | B.河水 | C.自来水 | D.海水 |
(3)实验室中常通过
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】某合金主要成分为Zn、Fe、Cu及这三种金属的少量氧化物。利用该合金制成的机械零件废弃物制取高纯度ZnO,其部分工艺流程如图所示。请回答:
已知:Zn(OH)2溶于强碱形成可溶性盐。_____________ ,滤渣Ⅰ中一定有______ 。
(2)加酸溶解废弃物时,需要通风并远离火源,其原因是______ 。写出较活泼金属生成该气体的化学方程式:______ (写一个),此反应属于______ (填基本反应类型)。
已知:Zn(OH)2溶于强碱形成可溶性盐。

(2)加酸溶解废弃物时,需要通风并远离火源,其原因是
您最近一年使用:0次
【推荐3】化学实验技能是学习化学和进行探究活动的进程和保证。某化学实验小组进行了一系列实验。主要操作过程下图所示:

请回答下列问题:
(1)实验甲中烧杯内的现象是______________________________________ ;所需的硫酸铜溶液,在配制前应先将硫酸铜晶体放于__________________ 内将其研碎。
(2)实验乙中的一处明显错误的是______________________________________ ;
(3)实验乙、丙中均使用到了玻璃棒,下列实验中必须使用玻璃棒的是________________ (填写字母序号)。
A.稀释浓硫酸
B.硫在氧气中燃烧
C.用pH试纸测肥皂水的pH
D.实验室制取二氧化碳
(4)实验丁中将氧化铜和木炭粉混合物加入试管中的正确操作是_______________ ;
为进一步提高实验的温度,应采取的措施是_________________________ 。

请回答下列问题:
(1)实验甲中烧杯内的现象是
(2)实验乙中的一处明显错误的是
(3)实验乙、丙中均使用到了玻璃棒,下列实验中必须使用玻璃棒的是
A.稀释浓硫酸
B.硫在氧气中燃烧
C.用pH试纸测肥皂水的pH
D.实验室制取二氧化碳
(4)实验丁中将氧化铜和木炭粉混合物加入试管中的正确操作是
为进一步提高实验的温度,应采取的措施是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】水是生命之源。
(1)1 滴水(以 20 滴水为 1mL 计)中大约有 1.67×10 21个水______ (用“分子”、“原子”或“离子”填空)
(2)如图为电解水的实验装置图。

①通电一段时间后,试管 a 中收集到的气体为______ (填化学式), 其体积与试管 b 中气体体积比为______ 。
②电解水的化学方程式为______ 。
(3)自然界的水循环如图所示。

①自然界的水属于______ (填“纯净物”或“混合物”)。
②从分子、原子角度分析,水变为水蒸气时,发生变化的是______ 。
③小颖在海边取了一瓶海水回家,她希望将海水中的泥沙除去。查阅九上化学课本,小颖发现实验室过滤实验需要用到漏斗、玻璃棒、滤纸等用品,小颖走进厨房灵机一动,她用纱布代替滤纸,用剪开的矿泉水塑料瓶代替漏斗,用筷子代替______ ,用杯子承接滤液,最终成功将泥沙除去。
(4)一定量水中加入适量氯化钠,充分溶解后通电,在电源负极会得到氢氧化钠和氢气,在正极会得到氯气(Cl2)。此反应的化学方程式为______ 。
(1)1 滴水(以 20 滴水为 1mL 计)中大约有 1.67×10 21个水
(2)如图为电解水的实验装置图。

①通电一段时间后,试管 a 中收集到的气体为
②电解水的化学方程式为
(3)自然界的水循环如图所示。

①自然界的水属于
②从分子、原子角度分析,水变为水蒸气时,发生变化的是
③小颖在海边取了一瓶海水回家,她希望将海水中的泥沙除去。查阅九上化学课本,小颖发现实验室过滤实验需要用到漏斗、玻璃棒、滤纸等用品,小颖走进厨房灵机一动,她用纱布代替滤纸,用剪开的矿泉水塑料瓶代替漏斗,用筷子代替
(4)一定量水中加入适量氯化钠,充分溶解后通电,在电源负极会得到氢氧化钠和氢气,在正极会得到氯气(Cl2)。此反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】《天工开物》“乃服”卷称:“凡棉布寸土皆有”,“织机十室必有”。我国棉纺织业在明代就非常发达,古代纺织业常用氢氧化钾作洗涤剂,对天然纤维进行脱脂、除杂等处理。生产氢氧化钾的一种工艺流程如图所示:

(1)操作X是________ 。
(2)上述工艺中,贝壳的主要成分煅烧分解的化学方程式为____________ ;可以循环利用的物质是_______________ 。
(3)受工艺条件限制,产品中的溶质除了KOH,还可能含有________ (写一种物质的化学式)。

(1)操作X是
(2)上述工艺中,贝壳的主要成分煅烧分解的化学方程式为
(3)受工艺条件限制,产品中的溶质除了KOH,还可能含有
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】某生铁粉末中含铁粉、碳粉和氧化铁。为测定所含碳粉的质量,化学小组取ag该样品,分别设计了如下实验方案,并对方案进行实验与分析,从而获取相关数据。
【方案甲】_______ 。
(2)操作I用到的玻璃仪器有烧杯、玻璃棒和_______ 。
(3)所得固体表面会残留少量溶液,在操作Ⅱ中需用蒸馏水多次洗涤并烘干,证明已洗涤干净的方法是_______ 。
【方案乙】装置如下图(夹持仪器省略,空气中CO2和H2O对实验的影响忽略不计)。_______ 。
(5)将反应后装置B中的物质全部加入足量水中搅拌、过滤:经检验滤渣的成分是碳酸钙,则滤液中一定含有的溶质是_______ 。
【反思】
(6)最终所得碳粉的质量:甲方案为m1g,乙方案为m2g,且m1>m2.请结合实验分析造成此差异的可能原因是_______ 。
【方案甲】

(2)操作I用到的玻璃仪器有烧杯、玻璃棒和
(3)所得固体表面会残留少量溶液,在操作Ⅱ中需用蒸馏水多次洗涤并烘干,证明已洗涤干净的方法是
【方案乙】装置如下图(夹持仪器省略,空气中CO2和H2O对实验的影响忽略不计)。

(5)将反应后装置B中的物质全部加入足量水中搅拌、过滤:经检验滤渣的成分是碳酸钙,则滤液中一定含有的溶质是
【反思】
(6)最终所得碳粉的质量:甲方案为m1g,乙方案为m2g,且m1>m2.请结合实验分析造成此差异的可能原因是
您最近一年使用:0次