某学习小组对铜丝在空气中灼烧后的产物进行探究。
实验1:甲同学将螺旋状铜丝灼烧至红热,冷却后观察到铜丝表面变为黑色,再伸入质量分数为25%的稀硫酸中,黑色固体消失,溶液出现蓝色,将铜丝取出洗净;重复上述实验2~3次,溶液蓝色逐渐加深。
【实验分析】灼烧铜丝生成黑色固体,该反应属于基本反应类型中的________ 反应,溶液变为蓝色的原因是黑色固体溶于稀硫酸变成硫酸铜溶液,写出生成硫酸铜的化学方程式_______ 。
实验2:乙同学将螺旋状铜丝灼烧至红热,迅速伸入质量分数为25%的稀硫酸中,观察到溶液中有红色固体产生,将铜丝取出洗净;重复上述实验2~3次,红色固体逐渐增多,沉淀后滤出红色固体,滤液呈浅蓝色。
【提出问题】红色固体是什么?
【查阅资料1】①Cu与O2在高于900℃时会反应生成红色的Cu2O。
②Cu2O能与H2SO4发生反应: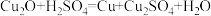 。
。
③加热条件下,Cu2O能与H2反应生成Cu和H2O。
【提出猜想】丙同学认为红色固体全部是Cu,不含Cu2O。
【实验验证1】学习小组取经过干燥的红色固体,采用如图装置验证猜想。
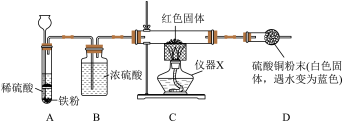
(1)仪器X的名称为_________ 。
(2)装置B中浓硫酸的作用是_________ 。
(3)实验时,应先将产生的氢气通入装置C中,待________ ,再开始加热。
(4)实验中观察到_______ (填实验现象),说明红色固体中含有Cu2O,丙同学猜想错误。
【提出问题2】实验2中有稀硫酸存在的情况下,为什么红色固体中仍含有Cu2O?
【查阅资料2】Cu2O与H2SO4反应的快慢与稀硫酸的浓度有关。稀硫酸的浓度越大,Cu2O与H2SO4反应越快。
【实验验证2】请设计实验验证“稀硫酸的浓度越大,Cu2O与H2SO4的反应越快”这一结论。简述实验过程(包括操作和现象):_______ 。
(实验中须使用的试剂:Cu2O、质量分数为5%和40%的稀硫酸)
【问题解决】因实验2中稀硫酸浓度变小,Cu2O与H2SO4反应变慢,Cu2O没有反应完全,故红色固体中仍含有Cu2O。
实验1:甲同学将螺旋状铜丝灼烧至红热,冷却后观察到铜丝表面变为黑色,再伸入质量分数为25%的稀硫酸中,黑色固体消失,溶液出现蓝色,将铜丝取出洗净;重复上述实验2~3次,溶液蓝色逐渐加深。
【实验分析】灼烧铜丝生成黑色固体,该反应属于基本反应类型中的
实验2:乙同学将螺旋状铜丝灼烧至红热,迅速伸入质量分数为25%的稀硫酸中,观察到溶液中有红色固体产生,将铜丝取出洗净;重复上述实验2~3次,红色固体逐渐增多,沉淀后滤出红色固体,滤液呈浅蓝色。
【提出问题】红色固体是什么?
【查阅资料1】①Cu与O2在高于900℃时会反应生成红色的Cu2O。
②Cu2O能与H2SO4发生反应:
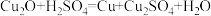 。
。③加热条件下,Cu2O能与H2反应生成Cu和H2O。
【提出猜想】丙同学认为红色固体全部是Cu,不含Cu2O。
【实验验证1】学习小组取经过干燥的红色固体,采用如图装置验证猜想。

(1)仪器X的名称为
(2)装置B中浓硫酸的作用是
(3)实验时,应先将产生的氢气通入装置C中,待
(4)实验中观察到
【提出问题2】实验2中有稀硫酸存在的情况下,为什么红色固体中仍含有Cu2O?
【查阅资料2】Cu2O与H2SO4反应的快慢与稀硫酸的浓度有关。稀硫酸的浓度越大,Cu2O与H2SO4反应越快。
【实验验证2】请设计实验验证“稀硫酸的浓度越大,Cu2O与H2SO4的反应越快”这一结论。简述实验过程(包括操作和现象):
(实验中须使用的试剂:Cu2O、质量分数为5%和40%的稀硫酸)
【问题解决】因实验2中稀硫酸浓度变小,Cu2O与H2SO4反应变慢,Cu2O没有反应完全,故红色固体中仍含有Cu2O。
更新时间:2021-12-23 07:03:49
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】在初中化学“金属的性质”中有如下实验。___________ 。
研究性学习小组对其展开了进一步探究。
【提出问题】
Al和CuSO4溶液也能发生化学反应吗?
(2)预测Al能和CuSO4溶液反应,理由是___________ 。
【进行实验】
将一端缠绕的铝丝浸入CuSO4溶液(如图),观察现象。
(3)铝丝表面未出现红色物质,原因是___________ 。
【实验改进】
用砂纸将铝丝表面打磨光亮,将其浸入CuSO4溶液,观察现象。
(4)填写实验报告单:
【深入探究】为研究上述异常现象,同学们查阅了相关资料,继续开展探究。
资料:①Cu2(OH)2SO4呈蓝绿色,不溶于水;
②Cl-可加快铝丝和其他物质的反应速率。
(5)取出铝丝,将试管中的混合物分离得到蓝绿色固体。加入稀硫酸,固体溶解形成蓝色溶液,使溶液呈现蓝色的离子是___________ (填写离子符号)。
(6)欲加快Al和CuSO4溶液的反应,可加入的物质是___________ (填一种即可)。
【拓展应用】通过探究,同学们提出了铝制品使用的注意事项。
(7)下列食品不能长时间用铝制炊具盛放的是___________(填序号)。

研究性学习小组对其展开了进一步探究。
【提出问题】
Al和CuSO4溶液也能发生化学反应吗?
(2)预测Al能和CuSO4溶液反应,理由是
【进行实验】
将一端缠绕的铝丝浸入CuSO4溶液(如图),观察现象。
(3)铝丝表面未出现红色物质,原因是
【实验改进】
用砂纸将铝丝表面打磨光亮,将其浸入CuSO4溶液,观察现象。
| 序号 | 实验现象 | 结论与解释 |
| a | 铝丝表面有少量气泡; 铝丝周围出现蓝绿色物质 | CuSO4溶液呈弱酸性,与Al反应产生的气体是 |
| b | 24h后,铝丝仍光亮;48h后,铝丝表面出现少量红色物质 | 红色物质是 |
| c | 铝丝周围溶液逐渐变成无色,铝丝以下溶液仍为蓝色;两层溶液界面清晰 | 反应生成的Al2(SO4)3为无色;Al2(SO4)3溶液的密度 |
(4)填写实验报告单:
【深入探究】为研究上述异常现象,同学们查阅了相关资料,继续开展探究。
资料:①Cu2(OH)2SO4呈蓝绿色,不溶于水;
②Cl-可加快铝丝和其他物质的反应速率。
(5)取出铝丝,将试管中的混合物分离得到蓝绿色固体。加入稀硫酸,固体溶解形成蓝色溶液,使溶液呈现蓝色的离子是
(6)欲加快Al和CuSO4溶液的反应,可加入的物质是
【拓展应用】通过探究,同学们提出了铝制品使用的注意事项。
(7)下列食品不能长时间用铝制炊具盛放的是___________(填序号)。
| A.食醋 | B.食用油 | C.面粉 | D.咸菜 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
【推荐2】同学们发现新鲜的苹果汁在空气中放置一段时间后会变色,仿佛铁生锈一样。于是,研究性小组同学设计并进行实验,探究苹果汁变色的原因。
【查阅资料】苹果汁中含有0.001%的二价铁物质,同时也含有多酚类物质,多酚可与空气中的氧气反应变为褐色。二价铁在空气中或与浓硝酸反应都能变为三价铁,且三价铁的溶液为黄色。硫氰化钾(KSCN)溶液变色规律如下:
【猜想与假设】Ⅰ.苹果汁变色与苹果中的铁元素有关
Ⅱ.苹果汁变色是苹果汁中的多酚物质与空气中的氧气反应的结果
【进行实验】
【解释与结论】
(1)实验1验证了苹果汁中含有二价铁物质。在该实验中③的现象是_______ 。
(2)实验2的②中FeSO4溶液溶质的质量分数为_______ %。该实验中,试管②③实验对比得出的结论是_______ 。由实验2得出:猜想Ⅰ_______ (填“成立”或“不成立”)。
(3)为验证猜想II成立,实验3应进行的操作_______ 。
【反思与评价】
(4)写出一种防止苹果汁变色的方法_______ 。
【查阅资料】苹果汁中含有0.001%的二价铁物质,同时也含有多酚类物质,多酚可与空气中的氧气反应变为褐色。二价铁在空气中或与浓硝酸反应都能变为三价铁,且三价铁的溶液为黄色。硫氰化钾(KSCN)溶液变色规律如下:
| 药品 | 二价铁溶液 | 三价铁溶液 |
| KSCN溶液 | 不变色 | 变红色 |
Ⅱ.苹果汁变色是苹果汁中的多酚物质与空气中的氧气反应的结果
【进行实验】
| 编号 | 实验操作 | 实验现象 | |||
| 实验1 |  | 试管②中未出现明显变化 试管③中 | |||
| 实验2 | 分别放置于空气中一段时间 (如下图所示)  | 试管编号 | 1min | 10min | 24 小时 |
| ① | 黄褐色 | 褐色 | 深褐色 | ||
| ② | 无明显变化 | 无明显变化 | 无明显变化 | ||
| ③ | 略有些黄色 | 浅黄 | 黄色 | ||
| 实验3 | 苹果汁不变色 | ||||
(1)实验1验证了苹果汁中含有二价铁物质。在该实验中③的现象是
(2)实验2的②中FeSO4溶液溶质的质量分数为
(3)为验证猜想II成立,实验3应进行的操作
【反思与评价】
(4)写出一种防止苹果汁变色的方法
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某学习小组将“从空气中制取氮气”作为研究课题,以下是他们的实验方案:

(提示:NaOH溶液能吸收二氧化碳,浓硫酸能吸收水分)
(1)方案一:将空气通过图1进行实验,此法得到的氮气不纯,请你分析可能的原因(写出2点)_____ ;_____
(2)方案二:将空气通过图1中A、B装置后,收集于图2的广口瓶中,用图2装置代替装置C进行实验。实验中红磷燃烧的现象是_____ 。该反应的化学方程式是_____ ;实验中用红磷而不用木炭的原因是_____ ;
(3)在工业上,分离空气中的氮气和氧气是利用它们_____ 的不同。

(提示:NaOH溶液能吸收二氧化碳,浓硫酸能吸收水分)
(1)方案一:将空气通过图1进行实验,此法得到的氮气不纯,请你分析可能的原因(写出2点)
(2)方案二:将空气通过图1中A、B装置后,收集于图2的广口瓶中,用图2装置代替装置C进行实验。实验中红磷燃烧的现象是
(3)在工业上,分离空气中的氮气和氧气是利用它们
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐1】定性和定量结合既是化学的重要思想,也是研究物质组成的重要方法。某研究性学习小组为检测实验室用H2还原CuO所得红色固体Cu中是否含有Cu2O(红色),进行了认真的研究。请你一起踏上探究之路,回答下列问题。
【查阅资料】①无水CuSO4遇水变蓝 ②高温灼烧CuO生成Cu2O和O2③Cu2O与稀H2SO4反应:Cu2O+H2SO4=Cu+CuSO4+H2O
【设计实验方案】
方案1 取该红色固体加入适量稀H2SO4,实验现象为_______ ,结论为红色固体中含有Cu2O.
方案2 装置如图所示,拟通过干燥管中CuSO4变蓝来判断红色固体是否含有Cu2O.
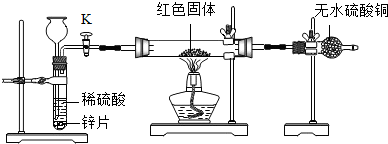
(1)为确保探究的科学、合理、安全.实验中还应采取的措施有_____ ;(填序号)
①加热前先排尽装置中的空气
②在氢气发生器与硬质玻璃管之间加一个干燥装置
③在盛有CuSO4的干燥管后再连接一个装有浓H2SO4的洗气瓶
(2)由方案2实验后得出结论:红色固体中含有Cu2O.写出红色固体Cu2O与H2反应的化学方程式_______________
方案3 称得干燥坩埚(常用于固体加热的容器)的质量为ag,取红色固体置于坩埚中称得总质量为bg,在空气中高温灼烧至质量恒定,称得最后坩埚与固体总质量为cg.
(1)该实验方案最少得进行_____ 次称量;
(2)若确认红色固体中含有Cu2O,则c与a,b应符合的数学关系式为_____ .
【查阅资料】①无水CuSO4遇水变蓝 ②高温灼烧CuO生成Cu2O和O2③Cu2O与稀H2SO4反应:Cu2O+H2SO4=Cu+CuSO4+H2O
【设计实验方案】
方案1 取该红色固体加入适量稀H2SO4,实验现象为
方案2 装置如图所示,拟通过干燥管中CuSO4变蓝来判断红色固体是否含有Cu2O.

(1)为确保探究的科学、合理、安全.实验中还应采取的措施有
①加热前先排尽装置中的空气
②在氢气发生器与硬质玻璃管之间加一个干燥装置
③在盛有CuSO4的干燥管后再连接一个装有浓H2SO4的洗气瓶
(2)由方案2实验后得出结论:红色固体中含有Cu2O.写出红色固体Cu2O与H2反应的化学方程式
方案3 称得干燥坩埚(常用于固体加热的容器)的质量为ag,取红色固体置于坩埚中称得总质量为bg,在空气中高温灼烧至质量恒定,称得最后坩埚与固体总质量为cg.
(1)该实验方案最少得进行
(2)若确认红色固体中含有Cu2O,则c与a,b应符合的数学关系式为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】纳米零价铁在环保领域应用广泛。
I、制备纳米铁粉
(1)已知氢气与菱铁矿(主要成分为 )在高温条件下反应能得到铁、水及二氧化碳,请写出化学反应方程式
)在高温条件下反应能得到铁、水及二氧化碳,请写出化学反应方程式______ 。
Ⅱ、探究制备纳米铁粉后所得固体的成分
【提出问题】氢气与碳酸亚铁反应后剩余固体的成分是什么?
【做出猜想】猜想一:Fe 猜想二: 猜想三:Fe和
猜想三:Fe和
【查阅资料】①氢气具有还原性,能够冶炼金属。
②无水硫酸铜是一种白色固体,遇水会变为蓝色。
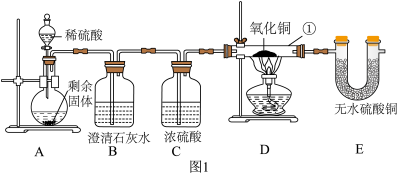
【实验探究】某学习小组利用如图1所示装置,对剩余固体成分(杂质不与稀硫酸反应)进行探究,实验操作及现象如下、回答下列问题。______ 。
(3)向装置A中加入稀硫酸后,A中产生气泡且溶液变为浅绿色,甲同学判断猜想一正确,乙同学认为甲的判断不合理,理由是______ 。
(4)观察到装置B中澄清石灰水变浑浊,D中______ (填实验现象),E中固体变蓝。
【实验结论】综上所述,猜想三正确。
【反思交流】
(5)若去掉装置E,______ (填“能”或“不能”)证明固体中含有Fe。
(6)若实验中先点燃D处的酒精灯,再向A中加稀硫酸,可能造成的后果是______ 。
Ⅲ、处理水体中的氮、磷______ 时、______ (填“酸性”或“碱性”)条件下处理效果更好。
(8)纳米铁粉能处理水体中的硝态氮。
①在酸性条件下,纳米铁粉能与 反应,该反应的化学方程式为:
反应,该反应的化学方程式为: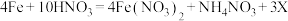 ,X的化学式为
,X的化学式为______ 。
②研究发现,废水中的溶解氧会对 去除产生一定影响。在其他条件相同时,有氧与无氧条件下
去除产生一定影响。在其他条件相同时,有氧与无氧条件下 的去除率随反应时间的变化如图3所示,分析1~3h时,有氧条件下
的去除率随反应时间的变化如图3所示,分析1~3h时,有氧条件下 的去除率低于无氧条件下的可能原因是
的去除率低于无氧条件下的可能原因是______ 。
I、制备纳米铁粉
(1)已知氢气与菱铁矿(主要成分为
 )在高温条件下反应能得到铁、水及二氧化碳,请写出化学反应方程式
)在高温条件下反应能得到铁、水及二氧化碳,请写出化学反应方程式Ⅱ、探究制备纳米铁粉后所得固体的成分
【提出问题】氢气与碳酸亚铁反应后剩余固体的成分是什么?
【做出猜想】猜想一:Fe 猜想二:
 猜想三:Fe和
猜想三:Fe和
【查阅资料】①氢气具有还原性,能够冶炼金属。
②无水硫酸铜是一种白色固体,遇水会变为蓝色。
【实验探究】某学习小组利用如图1所示装置,对剩余固体成分(杂质不与稀硫酸反应)进行探究,实验操作及现象如下、回答下列问题。
(3)向装置A中加入稀硫酸后,A中产生气泡且溶液变为浅绿色,甲同学判断猜想一正确,乙同学认为甲的判断不合理,理由是
(4)观察到装置B中澄清石灰水变浑浊,D中
【实验结论】综上所述,猜想三正确。
【反思交流】
(5)若去掉装置E,
(6)若实验中先点燃D处的酒精灯,再向A中加稀硫酸,可能造成的后果是
Ⅲ、处理水体中的氮、磷

(8)纳米铁粉能处理水体中的硝态氮。
①在酸性条件下,纳米铁粉能与
 反应,该反应的化学方程式为:
反应,该反应的化学方程式为: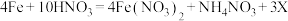 ,X的化学式为
,X的化学式为②研究发现,废水中的溶解氧会对
 去除产生一定影响。在其他条件相同时,有氧与无氧条件下
去除产生一定影响。在其他条件相同时,有氧与无氧条件下 的去除率随反应时间的变化如图3所示,分析1~3h时,有氧条件下
的去除率随反应时间的变化如图3所示,分析1~3h时,有氧条件下 的去除率低于无氧条件下的可能原因是
的去除率低于无氧条件下的可能原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】小丽同学在刚买来的袋装薯片中发现还有一个小袋,上面标有“成分: CaO、Fe;作用:防潮、防氧化;警告:禁止食用”等字样,撕开小袋,发现里面的固体粉末有少许是棕红色,大多数是灰白色的。经过分析,她认为棕红色粉末是Fe2O3,灰白色粉末应该含有CaCO3和Fe,为验证自己的判断,小丽同学打算进行实验探究,请你一同参与。
[实验目的]证实灰白色粉末中含有CaCO3和Fe。
[实验设计]装置如图所示:

[实验预测与分析]
(1)若要证实样品中含有CaCO3,观察到的实验现象是____ ,B中发生反应的化学方程式为____ 。
(2)若要证实样品中含有Fe, D中应该观察到的现象是____ ,E中的现象是____ ,此时C装置的作用是_____ 。
(3)看了小丽同学的分析结论,有同学认为小袋内灰白色粉末中还应该有别的物质,请你写出其中一种物质的化学式:_____ 。
[实验目的]证实灰白色粉末中含有CaCO3和Fe。
[实验设计]装置如图所示:

[实验预测与分析]
(1)若要证实样品中含有CaCO3,观察到的实验现象是
(2)若要证实样品中含有Fe, D中应该观察到的现象是
(3)看了小丽同学的分析结论,有同学认为小袋内灰白色粉末中还应该有别的物质,请你写出其中一种物质的化学式:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
【推荐1】实验室有一瓶敞放着的氢氧化钠固体,同学们想探究这瓶固体的成分,请你一同参与探究并回答有关问题.
【查阅资料】
碳酸钠水溶液显碱性,氯化钠、氯化钙水溶液显中性.
请你写出氢氧化钠在空气中变质的化学方程式__________ .
【提出猜想】
猜想1:这瓶固体的成分是NaOH; 猜想2:这瓶固体的成分是______ (填化学式);
猜想3:这瓶固体的成分是NaOH和Na2CO3的混合物;
【实验与结论】
(1)取少量样品于试管中,加入适量蒸馏水,振荡,样品全部溶于水,向其中加入无色酚酞溶液,溶液由无色变成红色.甲同学认为这瓶固体含有NaOH,乙同学认为甲同学的结论不正确,其理由是________ .
(2)向(1)溶液中加入过量的CaCl2溶液,生成白色沉淀,沉淀后静置,溶液由红色变成无色.同学们认为猜想______ 是正确的.
【问题讨论】(1)丙同学认为实验时也可以先加入过量的CaCl2溶液,振荡、静置,然后在上层清液中加入无色酚酞溶液,你认为丙同学的说法____ (填“正确”或“不正确”).
(2)丁同学认为CaCl2溶液也可以改为Ca(OH)2溶液,你认为丁同学的说法(填“正确”或“不正确”)______ ,理由是__________ .
【查阅资料】
碳酸钠水溶液显碱性,氯化钠、氯化钙水溶液显中性.
请你写出氢氧化钠在空气中变质的化学方程式
【提出猜想】
猜想1:这瓶固体的成分是NaOH; 猜想2:这瓶固体的成分是
猜想3:这瓶固体的成分是NaOH和Na2CO3的混合物;
【实验与结论】
(1)取少量样品于试管中,加入适量蒸馏水,振荡,样品全部溶于水,向其中加入无色酚酞溶液,溶液由无色变成红色.甲同学认为这瓶固体含有NaOH,乙同学认为甲同学的结论不正确,其理由是
(2)向(1)溶液中加入过量的CaCl2溶液,生成白色沉淀,沉淀后静置,溶液由红色变成无色.同学们认为猜想
【问题讨论】(1)丙同学认为实验时也可以先加入过量的CaCl2溶液,振荡、静置,然后在上层清液中加入无色酚酞溶液,你认为丙同学的说法
(2)丁同学认为CaCl2溶液也可以改为Ca(OH)2溶液,你认为丁同学的说法(填“正确”或“不正确”)
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】小玲的爸爸是化学教授,她对爸爸的一项研究成果产生了兴趣:CO2与Na在高温高压,催化剂的作用下,可以制得纳米级别的金刚石和一种白色固体。为了探究该白色固体的成分,小玲和同学一起来到爸爸的实验室,请你和她们一起完成如下探究:
【提出问题】白色固体的成分是什么?
【查阅资料】a.碳酸钠(Na2CO3)、氧化钠(Na2O)均为白色固体;
b.氧化钠与水常温下反应生成氢氧化钠,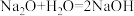
【猜想与假设】根据资料,小玲与两位同学提出以下猜想
甲同学:“白色固体是氧化钠(Na2O)”;
乙同学:“白色固体是碳酸钠(Na2CO3)”;
【实验与结论】①甲同学为验证猜想,取白色固体样品于试管中,加适量水,滴加无色酚酞溶液,通过酚酞溶液变红就判断自己的猜想正确,但遭到其他同学反对,原因是:______ 。
②为了验证自己的猜想,小玲设计了以下方案进行验证:
③通过上述实验可证明乙同学猜想正确,请写出Na与CO2反应的化学方程式______ 。
【提出问题】白色固体的成分是什么?
【查阅资料】a.碳酸钠(Na2CO3)、氧化钠(Na2O)均为白色固体;
b.氧化钠与水常温下反应生成氢氧化钠,
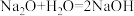
【猜想与假设】根据资料,小玲与两位同学提出以下猜想
甲同学:“白色固体是氧化钠(Na2O)”;
乙同学:“白色固体是碳酸钠(Na2CO3)”;
【实验与结论】①甲同学为验证猜想,取白色固体样品于试管中,加适量水,滴加无色酚酞溶液,通过酚酞溶液变红就判断自己的猜想正确,但遭到其他同学反对,原因是:
②为了验证自己的猜想,小玲设计了以下方案进行验证:
| 实验步骤 | 实验现象 | 实验结论 |
| Ⅰ、取少量白色固体样品于试管中,加入足量水使之溶解,并加入过量的 | 试管中产生白色沉淀 | 白色固体中有碳酸钠 |
| Ⅱ、往实验Ⅰ反应后的试管中滴加酚酞溶液,观察现象 | 白色固体中没有氧化钠 |
③通过上述实验可证明乙同学猜想正确,请写出Na与CO2反应的化学方程式
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】小林同学在体育课上腿部擦伤,医务室的大夫在她伤口上涂了医用过氧化氢溶液,小林看到伤口处产生了小气泡,很好奇。为什么瓶中的过氧化氢溶液涂到伤口上,分解就加快了呢?

I、小林准备用如下图所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧气。记录2分钟收集的气体体积。

(1)请写出过氧化氢分解的文字(或化学式)表达式:______ 。
(2)若要检验生成的气体是否为氧气,可将导气管从水中取出,取带火星的木条放在导气管口处,观察到______ ,说明生成的气体是氧气。
II、小林查阅了相关资料,并进行了探究实验
【查阅资料】
1、过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以催化过氧化氢分解。
2、温度对化学反应的快慢有影响,人体正常体温是37℃。
【提出猜想】
猜想1:过氧化氢分解加快是因为体温比瓶中的温度高。
猜想2:过氧化氢分解加快是因为伤口中有过氧化氢酶。
【进行实验】
(3)实验①得出的结论是______ 。
(4)实验②中横线部分应进行的操作是______ 。
【实验反思】
小林反思了实验过程,认为人体中过氧化氢酶是在体温条件下发挥作用的,实验得出的结论可能存在不足。因此又补充进行了几组实验,数据记录如下表所示。
(5)通过这些数据,你能得出的新结论是______ 。

I、小林准备用如下图所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧气。记录2分钟收集的气体体积。

(1)请写出过氧化氢分解的文字(或化学式)表达式:
(2)若要检验生成的气体是否为氧气,可将导气管从水中取出,取带火星的木条放在导气管口处,观察到
II、小林查阅了相关资料,并进行了探究实验
【查阅资料】
1、过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以催化过氧化氢分解。
2、温度对化学反应的快慢有影响,人体正常体温是37℃。
【提出猜想】
猜想1:过氧化氢分解加快是因为体温比瓶中的温度高。
猜想2:过氧化氢分解加快是因为伤口中有过氧化氢酶。
【进行实验】
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 分两次进行实验,均注入5 mL过氧化氢溶液 第一次在常温下进行 第二次将试管浸在37℃的温水中 | 量筒中2分钟收集到的气体体积均为5 mL | ______ |
| ② | 分两次进行实验 第一次将装有一小粒过氧化氢酶的试管浸在37℃的温水中,注入5 mL过氧化氢溶液 第二次______ | 第一次,量筒中2分钟收集到的气体体积为56 mL 第二次,量筒中2分钟收集到的气体体积为5 mL | 过氧化氢分解加快是因为过氧化氢酶的作用 |
(4)实验②中横线部分应进行的操作是
【实验反思】
小林反思了实验过程,认为人体中过氧化氢酶是在体温条件下发挥作用的,实验得出的结论可能存在不足。因此又补充进行了几组实验,数据记录如下表所示。
加入过氧化氢酶 | 不加过氧化氢酶 | |||||
| 反应温度/ ℃ | 25 | 37 | 42 | 25 | 37 | 42 |
| 收集到气体体积/ mL | 39 | 56 | 34 | 5 | 5 | 5 |
您最近一年使用:0次



