稀氢氧化钠溶液与稀盐酸反应时,溶液的pH与加入的稀氢氧化钠溶液的质量关系如图所示。
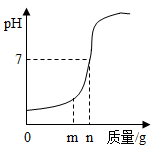
(1)稀氢氧化钠溶液的pH______ 7(填“>”“<”或“=”)。
(2)请将氢氧化钠与盐酸反应的化学方程式补充完整: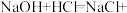
______ 。
(3)当加入稀氢氧化钠溶液质量为mg时,溶液中的溶质是______ ,此时在溶液中滴入紫色石蕊试液,溶液呈______ 色。
(4)在如图中用A表示出氢氧化钠与盐酸恰好完全反应时的点。

(1)稀氢氧化钠溶液的pH
(2)请将氢氧化钠与盐酸反应的化学方程式补充完整:
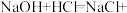
(3)当加入稀氢氧化钠溶液质量为mg时,溶液中的溶质是
(4)在如图中用A表示出氢氧化钠与盐酸恰好完全反应时的点。
2022·上海杨浦·一模 查看更多[3]
更新时间:2022-01-14 21:23:54
|
相似题推荐
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐1】酸碱指示剂的发现与应用
很多重大的发现源于科学家善于观察、思考的品质。石蕊这种酸碱指示剂就是英国化学家波义耳偶然发现的。有一天,波义耳看到溅了几滴盐酸的紫罗兰花朵变成了红色,紫罗兰为什么会变红?波义耳用其他物质进行了反复实验,终于认定紫罗兰花的浸出液可用于检验溶液是否呈酸性,他又努力寻找用来检验碱性的物质,后来发现了从石蕊地衣中提取出的紫色石蕊溶液可以用来检验溶液的酸碱性。
后来人们测出了石蕊较准确的变色范围:在pH<5.0的溶液里呈红色,在pH>8.0的溶液里呈蓝色,pH在两者之间呈紫色。酚酞是另一种酸碱指示剂,在pH<8.2的溶液里呈无色,在pH>8.2的溶液里呈红色,但如遇到较浓的碱液,又会立即变成无色。除以上两种指示剂外,生活中我们也可以用红萝卜皮、紫卷心菜等植物自制酸碱指示剂。
分析短文,回答问题:
(1)文中提到当波义耳发现紫罗兰花朵变红时,他又用其他物质进行了反复实验,他可能用到了下列物质中的___________ (填字母)。
a稀硫酸 b氯化钠溶液 c碳酸钠溶液 d柠檬酸溶液
(2)下列说法正确的是___________ 。(填字母)
a某些溶液的酸碱性无法用石蕊溶液和酚酞溶液检测出来
b某溶液的pH=6,在该溶液中滴加紫色石蕊溶液,溶液变红
c红萝卜皮、紫卷心菜的提取液遇酸性溶液和碱性溶液时呈现不同的颜色
(3)老师在做“中和反应”的实验时,先向氢氧化钠溶液中滴加了几滴无色酚酞溶液,观察到酚酞刚滴入时为红色,但瞬间变成无色,加入少量稀盐酸后又变为红色。实验中酚酞瞬间变成无色时,溶液呈___________ (填“酸性”“中性”或“碱性”)。分析上述实验中酚酞无色后又变红色原因是:___________ ;向此溶液中逐滴滴加盐酸,溶液刚好变成无色时,溶液的pH___________ 7。(填“一定等于”或“不一定等于”)
很多重大的发现源于科学家善于观察、思考的品质。石蕊这种酸碱指示剂就是英国化学家波义耳偶然发现的。有一天,波义耳看到溅了几滴盐酸的紫罗兰花朵变成了红色,紫罗兰为什么会变红?波义耳用其他物质进行了反复实验,终于认定紫罗兰花的浸出液可用于检验溶液是否呈酸性,他又努力寻找用来检验碱性的物质,后来发现了从石蕊地衣中提取出的紫色石蕊溶液可以用来检验溶液的酸碱性。
后来人们测出了石蕊较准确的变色范围:在pH<5.0的溶液里呈红色,在pH>8.0的溶液里呈蓝色,pH在两者之间呈紫色。酚酞是另一种酸碱指示剂,在pH<8.2的溶液里呈无色,在pH>8.2的溶液里呈红色,但如遇到较浓的碱液,又会立即变成无色。除以上两种指示剂外,生活中我们也可以用红萝卜皮、紫卷心菜等植物自制酸碱指示剂。
分析短文,回答问题:
(1)文中提到当波义耳发现紫罗兰花朵变红时,他又用其他物质进行了反复实验,他可能用到了下列物质中的
a稀硫酸 b氯化钠溶液 c碳酸钠溶液 d柠檬酸溶液
(2)下列说法正确的是
a某些溶液的酸碱性无法用石蕊溶液和酚酞溶液检测出来
b某溶液的pH=6,在该溶液中滴加紫色石蕊溶液,溶液变红
c红萝卜皮、紫卷心菜的提取液遇酸性溶液和碱性溶液时呈现不同的颜色
(3)老师在做“中和反应”的实验时,先向氢氧化钠溶液中滴加了几滴无色酚酞溶液,观察到酚酞刚滴入时为红色,但瞬间变成无色,加入少量稀盐酸后又变为红色。实验中酚酞瞬间变成无色时,溶液呈
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】A、B两班同学分别做常见酸和碱反应中和的实验,使用的试剂有:盐酸、氢氧化钠溶液、酚酞试液.实验后废液倒入废液缸中,研究小组对两个班的废液进行检测,结果如下:
(1)A班:观察废液呈无色,则废液显_________ 性,再向废液中加Fe若看到_________ 说明显酸性.废液中含__________ .(酚酞与水除外,下同)
(2)B班:观察废液呈红色推断:废液中没有_________ ,含有_________ .发生的化学反应是________ .
(1)A班:观察废液呈无色,则废液显
(2)B班:观察废液呈红色推断:废液中没有
您最近一年使用:0次
【推荐3】张雅轩同学在学习酸、碱性质时,利用以下装置对酸、碱的化学性质进行探究。

(1)浓盐酸、浓硫酸敞口放置在空气中一段时间、溶质的质量分数都会
(2)酸有相似的化学性质,因为它们的溶液中都含有
(3)实验 I 中在点滴板中完成实验,点滴板完成实验的优点是
溶液 | 稀盐酸 | 氢氧化钙溶液 |
实验现象 | 溶液变红色 | 溶液变 |
(4)实验Ⅱ中,为了验证石灰石与稀盐酸发生反应,试剂X 为澄清石灰水,写出澄清石灰水变浑浊的化学方程式
(5)在实验的烧杯②中滴加2滴酚酞溶液后,扣上大烧杯,一段时间后看到的现象是烧杯②中红色溶液变成无色,得出的结论是:分子在
您最近一年使用:0次
【推荐1】“宏观辨识与微观探析”是化学学科特有的学习方法之一。下面是四个与NaCl有关的化学反应的微观示意图。



(1)由图1可看出,元素的化学性质与___________ 有关。氯化钠是由________ 构成的。
(2)图2中A、B表示的粒子符号依次是____________ 。
(3)图3表示的化学反应中,氯元素的化合价共有______ 种。
(4)图4是一种家用环保型消毒液发生器,其中发生的主要反应是: ,其中物质X的化学式为
,其中物质X的化学式为_______ 。



(1)由图1可看出,元素的化学性质与
(2)图2中A、B表示的粒子符号依次是
(3)图3表示的化学反应中,氯元素的化合价共有
(4)图4是一种家用环保型消毒液发生器,其中发生的主要反应是:
 ,其中物质X的化学式为
,其中物质X的化学式为
您最近一年使用:0次
【推荐2】归纳总结是学习化学的重要方法,小明同学用图l总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应)。结合你所学过的知识,简要回答问题:
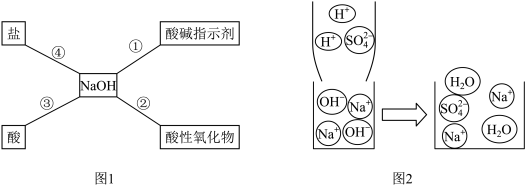
(1)为了验证反应①,小明将无色酚酞试液滴入NaOH溶液中,溶液变成_________ 色。
依据反应②说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为:__________________ 。
(2)“用微观的眼光看世界”,是我们学习化学的重要思想方法。小明用微观示意图(图2)来说明反应③的发生,用化学反应方程式表示为:_____________________ ;反应类型为 ______________ 。从该图可以看出,反应前后没有发生变化的微观粒子有 _________ 和 _______ ;该反应中复分解反应能发生的本质原因 ___________ 。
(3)在图2所示的反应过程中,小明对反应溶液的pH进行了三次测定,当溶液pH=7时,溶液中溶质为______ (填化学式);
(4)为了验证反应④能够发生,请你选择一种物质,写出其对应的化学反应方程式:_____________ 。

(1)为了验证反应①,小明将无色酚酞试液滴入NaOH溶液中,溶液变成
依据反应②说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为:
(2)“用微观的眼光看世界”,是我们学习化学的重要思想方法。小明用微观示意图(图2)来说明反应③的发生,用化学反应方程式表示为:
(3)在图2所示的反应过程中,小明对反应溶液的pH进行了三次测定,当溶液pH=7时,溶液中溶质为
(4)为了验证反应④能够发生,请你选择一种物质,写出其对应的化学反应方程式:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】“见著知微,见微知著”是化学思维方法,也是认识物质结构与性质的重要方法。
(1)表中为三种元素原子的结构示意图。
①x=___________ 。
②已知这三种原子的核外电子层数越多,原子半径越大;核外电子层数相等时,核电荷数越多,原子半径越小。这三种原子中半径最小的___________ 。(填原子符号)
(2)氮及其化合物的“化合价—物质类别”关系如图。

①物质X的化学式是___________ 。
②请写出和HNO3通过中和反应生成Ca(NO3)2的化学方程式为___________ 。
③爆炸性的高能 阳离子(氮元素的原子序数为7)被美国加州爱得华空军基地研究高能材料的化学家合成。关于
阳离子(氮元素的原子序数为7)被美国加州爱得华空军基地研究高能材料的化学家合成。关于 的说法正确的是
的说法正确的是___________ 。(填序号)
A 该粒子的电子数为34 B.该粒子的质子数为34
C.该粒子由5个氮分子构成 D.它是一种由5个氮原子构成的单质分子
(3)①如图所示,微粒A、B、C、D、E中,对应单质化学性质最稳定的是_____ 。(填化学式)
②微粒A、E形成的化合物的化学式为___________ 。

(1)表中为三种元素原子的结构示意图。
①x=
②已知这三种原子的核外电子层数越多,原子半径越大;核外电子层数相等时,核电荷数越多,原子半径越小。这三种原子中半径最小的
| 元素名称 | 氮 | 氟 | 镁 |
| 原子结构示意图 |  |  |  |

①物质X的化学式是
②请写出和HNO3通过中和反应生成Ca(NO3)2的化学方程式为
③爆炸性的高能
 阳离子(氮元素的原子序数为7)被美国加州爱得华空军基地研究高能材料的化学家合成。关于
阳离子(氮元素的原子序数为7)被美国加州爱得华空军基地研究高能材料的化学家合成。关于 的说法正确的是
的说法正确的是A 该粒子的电子数为34 B.该粒子的质子数为34
C.该粒子由5个氮分子构成 D.它是一种由5个氮原子构成的单质分子
(3)①如图所示,微粒A、B、C、D、E中,对应单质化学性质最稳定的是
②微粒A、E形成的化合物的化学式为

您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是向滴有酚酞的氢氧化钠溶液中缓慢滴加稀盐酸的实验操作图。请回答下列问题:

(1)实验中观察到什么现象时,能证明氢氧化钠和稀盐酸发生了化学反应?
(2)从微观角度看,该化学反应的实质是什么?

(1)实验中观察到什么现象时,能证明氢氧化钠和稀盐酸发生了化学反应?
(2)从微观角度看,该化学反应的实质是什么?
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐2】根据图片回答下列问题:
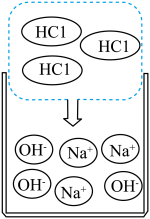
(1)从微观角度看,该化学反应的实质是什么?______ 。
(2)已知图中所示的两种溶液恰好完全反应,若保持氢氧化钠溶液不变,将稀盐酸改为相同质量且相同溶质质量分数的稀硫酸,则反应过后溶液中溶质的成分是什么?_____ 。

(1)从微观角度看,该化学反应的实质是什么?
(2)已知图中所示的两种溶液恰好完全反应,若保持氢氧化钠溶液不变,将稀盐酸改为相同质量且相同溶质质量分数的稀硫酸,则反应过后溶液中溶质的成分是什么?
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】传感器探究氢氧化钠溶液与稀硫酸发生酸碱中和过程中温度和 pH的变化,实验测定结果如图甲、乙图所示。请回答:

(1)图甲表明酸和碱的反应_____ (填吸热或放热)。
(2)图乙表明实验时将_____ (填 酸溶液滴入碱溶液或碱溶液滴入酸溶液)中。
(3)写出氢氧化钠溶液和稀硫酸反应的化学方程式:_____ 。
(4)在反应50 s时的溶液中滴加酚酞溶液,可观察到实验现象是_____ 。
(5)请从微观的角度分析图丙中甲、乙处分别应填入的微粒符号为_____ 、 _ 。

(1)图甲表明酸和碱的反应
(2)图乙表明实验时将
(3)写出氢氧化钠溶液和稀硫酸反应的化学方程式:
(4)在反应50 s时的溶液中滴加酚酞溶液,可观察到实验现象是
(5)请从微观的角度分析图丙中甲、乙处分别应填入的微粒符号为
您最近一年使用:0次
【推荐1】依据文章内容,回答相关问题:
炒菜时放点食醋能软化植物纤维素,改善食物的色、香、味,并可保护食物中的维生素C(维生素C在酸性条件下稳定),能溶解骨质,促进人体对钙、磷的吸收。
回答相关问题:
(1)山西老陈醋属于______ (填“混合物”或“纯净物”),使老陈醋显酸性的离子是______ (填离子符号)。
(2)新醋通过“夏伏晒、冬捞冰”的陈放过程得到老陈醋,此时老陈醋的pH值比新醋______ (填“大”或“小”),请写出pH试纸的使用操作______ 。
(3)请用化学方程式解释酿造时注意防火的原因______ 。
(4)家中炒菜时放入适量食醋的目的是______ 。
天下第一醋——老陈醋
山西老陈醋历史渊远、驰名中外,素有“天下第一醋”的盛誉。食醋中含3%~5%的醋酸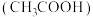 ,醋酸又称乙酸,常温下是一种有强烈刺激性气味的无色液体,易溶于水和乙醇,水溶液呈酸性。
,醋酸又称乙酸,常温下是一种有强烈刺激性气味的无色液体,易溶于水和乙醇,水溶液呈酸性。
老陈醋是将高粱、大麦、豌豆等粉碎后进行发酵,发酵时先生成乙醇 和二氧化碳(乙醇遇明火会发生燃烧生成二氧化碳和水),乙醇在空气中醋酸菌的催化下变成醋酸和水,经过磨、淋、薰、蒸等复杂的手工酿造过程之后得到新醋,再输之以“夏伏晒、冬捞冰”的陈放过程,使醋中的杂质沉淀,水分通过蒸发或结冰析出后得到老陈醋。
和二氧化碳(乙醇遇明火会发生燃烧生成二氧化碳和水),乙醇在空气中醋酸菌的催化下变成醋酸和水,经过磨、淋、薰、蒸等复杂的手工酿造过程之后得到新醋,再输之以“夏伏晒、冬捞冰”的陈放过程,使醋中的杂质沉淀,水分通过蒸发或结冰析出后得到老陈醋。
炒菜时放点食醋能软化植物纤维素,改善食物的色、香、味,并可保护食物中的维生素C(维生素C在酸性条件下稳定),能溶解骨质,促进人体对钙、磷的吸收。
回答相关问题:
(1)山西老陈醋属于
(2)新醋通过“夏伏晒、冬捞冰”的陈放过程得到老陈醋,此时老陈醋的pH值比新醋
(3)请用化学方程式解释酿造时注意防火的原因
(4)家中炒菜时放入适量食醋的目的是
您最近一年使用:0次
【推荐2】常见的碱有氢氧化钠和氢氧化钙。请回答下列有关问题:
(1)向盛有氢氧化钠溶液的锥形瓶里滴入几滴酚酞溶液,溶液变成_____ 色,pH_____ 7(填“>”“<”或“=”),逐滴向锥形瓶中滴入盐酸并振荡,观察到的现象是_____ ,溶液的pH_____ (填“增大”或“减小”)。
(2)氢氧化钙俗称熟石灰,在生产和生活中有广泛的用途。
①熟石灰可由生石灰溶于水制得,反应的化学方程式是:_____ 。
②用石灰浆粉刷墙壁,干燥后墙面变硬,反应的化学方程式是:_____ 。
③用熟石灰来改良酸性土壤(以土壤中含有硫酸为例),反应的化学方程式是:_____ 。
④用熟石灰粉与草木灰(主要成分是K2CO3)按一定比例混合可制得高效环保农药“黑白粉”。使用时,选择在有露水的早晨,把“黑白粉”撒在植物茎叶上,可消除忌碱虫体。“黑白粉”比熟石灰更高效,是由于生成了碱性更强的KOH,反应的化学方程式是:_____ 。
(1)向盛有氢氧化钠溶液的锥形瓶里滴入几滴酚酞溶液,溶液变成
(2)氢氧化钙俗称熟石灰,在生产和生活中有广泛的用途。
①熟石灰可由生石灰溶于水制得,反应的化学方程式是:
②用石灰浆粉刷墙壁,干燥后墙面变硬,反应的化学方程式是:
③用熟石灰来改良酸性土壤(以土壤中含有硫酸为例),反应的化学方程式是:
④用熟石灰粉与草木灰(主要成分是K2CO3)按一定比例混合可制得高效环保农药“黑白粉”。使用时,选择在有露水的早晨,把“黑白粉”撒在植物茎叶上,可消除忌碱虫体。“黑白粉”比熟石灰更高效,是由于生成了碱性更强的KOH,反应的化学方程式是:
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐3】氧化镁在医药、建筑等行业应用广泛。以菱镁矿(主要成分为MgCO3,含少量FeCO3和不溶性杂质)为原料制备高纯氧化镁的实验流程图如下:

(1)FeCO3的名称是________ ;MgSO4固体与木炭反应的化学方程式为_____________ 。
(2)在实验室里完成操作I,需要用到的玻璃仪器除漏斗、玻璃棒外,还有________ ;滤液I里,主要的金属阳离子是_________ (填离子符号)。
(3)通过加入氨水使溶液的pH______________ (填“增大”或“减小”或“不变”),将杂质离子沉淀除去。
(4)若直接煅烧100t含碳酸镁84%的菱镁矿,理论上可制得氧化镁的质量为______ t。
(5)为了探究最佳实验条件,提升硫酸镁固体的转化率,实验小组进行了以下实验,并得到如下数据:
请分析数据,选出在此工业生产中采取的最佳实验条件:
温度_____________ ℃、 m(MgSO4):m(C)______________ 、时间_____________ h。

(1)FeCO3的名称是
(2)在实验室里完成操作I,需要用到的玻璃仪器除漏斗、玻璃棒外,还有
(3)通过加入氨水使溶液的pH
(4)若直接煅烧100t含碳酸镁84%的菱镁矿,理论上可制得氧化镁的质量为
(5)为了探究最佳实验条件,提升硫酸镁固体的转化率,实验小组进行了以下实验,并得到如下数据:
| 编号 | 矿石质量(g) | 温度(℃) | m(MgSO4):m(C) | 时间(h) | 硫酸镁的转化率(%) |
| 1 | 85.71 | 600 | 1:1 | 0.5 | 49.98 |
| 2 | 85.71 | 650 | 2:1 | 0.5 | 65.34 |
| 3 | 85.71 | 600 | 2:1 | 0.5 | 56.39 |
| 4 | 85.71 | 650 | 2:1 | 1 | 80.76 |
| 5 | 85.71 | 800 | 8:1 | 2 | 98.12 |
| 6 | 85.71 | 850 | 8:1 | 3 | 98.48 |
请分析数据,选出在此工业生产中采取的最佳实验条件:
温度
您最近一年使用:0次



