元素周期表是学习和研究化学的重要工具。溴元素的相关信息如图甲所示,请回答下列问题。
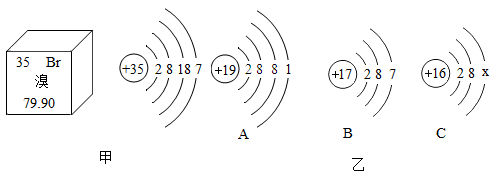
(1)溴的相对原子质量是___________ ,溴属于___________ (填“金属”或“非金属”)元素。
(2)溴元素的化学性质与图乙中___________ (填元素符号)元素的化学性质相似。
(3)溴元素与图乙中A元素,形成化合物的化学式为___________ 。
(4)若图乙中C表示离子,则x的值是___________ 。
(5)在单质中元素的化合价为___________ 。

(1)溴的相对原子质量是
(2)溴元素的化学性质与图乙中
(3)溴元素与图乙中A元素,形成化合物的化学式为
(4)若图乙中C表示离子,则x的值是
(5)在单质中元素的化合价为
更新时间:2022-02-07 18:12:32
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】元素周期表是学习和研究化学的重要工具。
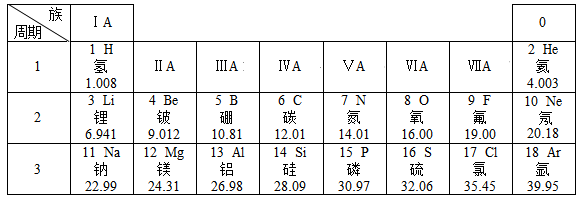
请分析图中信息回答相关问题:
(1)硫原子在化学反应中容易___________ (填“得到”或“失去”)电子成为硫离子,硫离子与硫原子的化学性质___________ (填“相同”或“不同”)。
(2)在元素周期表中,同一族的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是___________。(填序号)
(3)同一周期,从左到右,原子半径减小,元素的原子得电子能力增强。原子非金属性增强;同一族,从上到下,原子半径增大,元素的原子得电子能力减弱,原子非金属性减弱,O、F、Cl元素的原子非金属性最强的是___________ (填符号)。

请分析图中信息回答相关问题:
(1)硫原子在化学反应中容易
(2)在元素周期表中,同一族的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是___________。(填序号)
| A.C和Ne | B.Be和Mg | C.Al和Si | D.F和Cl |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】元素周期表是学习和研究化学的重要工具。
(1)原子序数为1~18的元素在元素周期表中的位置如下表所示。
① Na属于________ (填“金属”或“非金属”)元素,其原子的核电荷数为________ 。
② Mg原子的结构示意图为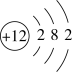 ,则镁离子的核外电子数为
,则镁离子的核外电子数为__________ 。
③ 周期表中氯元素的有关信息如图所示,图中“35.45”所表示的含义是______ 。

④ 由镁和氯构成的盐的化学式为________________ 。
(2)根据周期表体现的结构与性质之间的关系,某同学构建了铜及其化合物的“化合价—物质类别”关系图。
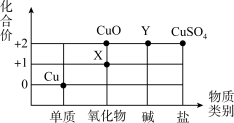
① 写出物质X的化学式:______________ 。
② 写出由物质Y转化为CuSO4的化学反应方程式:_____________ 。
(1)原子序数为1~18的元素在元素周期表中的位置如下表所示。
| 第1周期 | H | He | ||||||
| 第2周期 | Li | Be | B | C | N | O | F | Ne |
| 第3周期 | Na | Mg | Al | Si | P | S | Cl | Ar |
② Mg原子的结构示意图为
 ,则镁离子的核外电子数为
,则镁离子的核外电子数为③ 周期表中氯元素的有关信息如图所示,图中“35.45”所表示的含义是

④ 由镁和氯构成的盐的化学式为
(2)根据周期表体现的结构与性质之间的关系,某同学构建了铜及其化合物的“化合价—物质类别”关系图。

① 写出物质X的化学式:
② 写出由物质Y转化为CuSO4的化学反应方程式:
您最近一年使用:0次
【推荐3】在全球半导体产业的剧烈竞争中,中国的芯片技术正逐渐崭露头角。华为发布的新款手机中搭载的麒麟9000S芯片已经有世界展示了中国芯片的实力和潜力。
芯片的主要材料由高纯度单晶硅(化学式为Si)制作,工正上用粗硅经两步反应制得单品硅。第一步:粗硅和氯化氢在300℃发生反应,生成三氯硅烷(化学式为SiHCl3)和氢气。第二步:三氯硅烷和氢气在1000℃时发生反应,生成单品硅和氯化氢。
石墨烯最有潜力成为硅的替代品,它是目前已知材料中电子传导速率最快的。石墨烯是将石墨逐层剥离,直到最后形成一个单层,厚度只有一个碳原子的单层石墨。
阅读分析,解决问题:
(1)硅元素在地壳里含量较高。写出地壳里含量最高金属元素的元素符号_______________ 。
(2)从原子结构来分析,单晶硅和石墨烯化学性质都很稳定的原因是_______________ 。
(3)石墨烯由_______________ 微粒构成。石墨烯在空气中完全燃烧,反应的符号表达式为_______________ 。
(4)三氯硅烷中氢元素化合价为+1价,氯元素显负价,则硅元素的化合价为_______________ 。
(5)石墨烯代替硅制作电子产品的重要意义是_______________ 。
芯片的主要材料由高纯度单晶硅(化学式为Si)制作,工正上用粗硅经两步反应制得单品硅。第一步:粗硅和氯化氢在300℃发生反应,生成三氯硅烷(化学式为SiHCl3)和氢气。第二步:三氯硅烷和氢气在1000℃时发生反应,生成单品硅和氯化氢。
石墨烯最有潜力成为硅的替代品,它是目前已知材料中电子传导速率最快的。石墨烯是将石墨逐层剥离,直到最后形成一个单层,厚度只有一个碳原子的单层石墨。
阅读分析,解决问题:
(1)硅元素在地壳里含量较高。写出地壳里含量最高金属元素的元素符号
(2)从原子结构来分析,单晶硅和石墨烯化学性质都很稳定的原因是
(3)石墨烯由
(4)三氯硅烷中氢元素化合价为+1价,氯元素显负价,则硅元素的化合价为
(5)石墨烯代替硅制作电子产品的重要意义是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】如图为某反应的微观反应示意图。
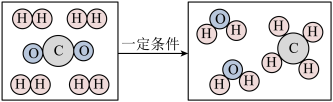
(1)图中的物质均有______________ (填“粒子、原子或分子”)构成。
(2)图中属于单质的是_________ (写化学式,后同),属于化合物的是________ 。
(3)该反应的化学方程式为___________________ 。

(1)图中的物质均有
(2)图中属于单质的是
(3)该反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】在宏观、微观和符号之间建立联系是化学学科的特点。
(1)构成氧气的粒子是_______ (填“氧原子”或“氧分子”)。
(2)下图是钠、镁、氯、溴四种原子的结构示意图。

①镁原子的结构示意图中x的数值为_______ 。
②以上图中共有_______ 种元素。
③溴(Br)原子在化学反应中容易_______ 电子(填“得到”或“失去”),钠原子在化学反应中容易____ 电子(填“得到”或“失去”);溴化钠是由钠元素和溴元素组成的化合物,溴化钠的化学式为_______ 。
(3)汽车尾气净化装置中装有铂催化剂,尾气在催化剂表面反应的微观过程如图所示。试回答:
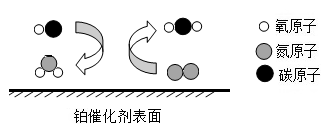
①应前后铂催化剂的质量_______ (填:改变或不变)
②反应中属于单质的物质化学式为_______ 。
③写出该反应的符号表达式_______ 。
(1)构成氧气的粒子是
(2)下图是钠、镁、氯、溴四种原子的结构示意图。

①镁原子的结构示意图中x的数值为
②以上图中共有
③溴(Br)原子在化学反应中容易
(3)汽车尾气净化装置中装有铂催化剂,尾气在催化剂表面反应的微观过程如图所示。试回答:

①应前后铂催化剂的质量
②反应中属于单质的物质化学式为
③写出该反应的符号表达式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】已知如图A、B、C三种元素的粒子结构示意图依次为:
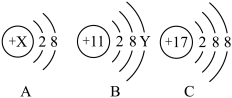
(1)当A、B为原子结构示意图时,X=_____ ;Y=_____ ;
(2)当A为离子结构示意图时,若该离子带2个单位正电荷时,则其离子符号为_____ ,若该离子带一个单位负电荷时,则其离子符号为_____ 。
(3)C表示的是离子结构示意图,为_____ (填“阳离子”、“阴离子”或“原子”);该元素与B元素形成的化合物的化学式为_____ ;该化合物是由_____ (填“分子”、“原子”或“离子”)构成。

(1)当A、B为原子结构示意图时,X=
(2)当A为离子结构示意图时,若该离子带2个单位正电荷时,则其离子符号为
(3)C表示的是离子结构示意图,为
您最近一年使用:0次
【推荐1】在宏观、微观和符号之间建立联系是学习化学的重要思维方式。
(1)元素周期表是学习化学的重要工具,根据如图信息回答问题。
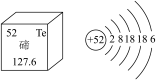
①碲属于_______ (填“金属”或“非金属”)元素,其相对原子质量为_______ 。
②碲元素化学性质与图中_______ 元素化学性质相似,碲元素与13号元素形成的化合物化学式为_______ 。
(2)氢气与乙烯在催化剂金属镍表面反应生成乙烷,微观过程如图所示:
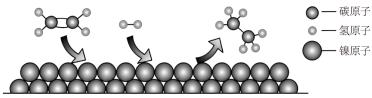
①金属镍在化学反应前后_______ 不变。
②反应的化学方程式为_______ 。
(1)元素周期表是学习化学的重要工具,根据如图信息回答问题。
| l H | 2 He | ||||||
| 3 Li | 4Be | 5 B | 6C | 7 N | 80 | 9F | 10 Ne |
| 11 Na | 12 Mg | 13 Al | l4 Si | 15 P | 16 S | l7 Cl | l8 Ar |

①碲属于
②碲元素化学性质与图中
(2)氢气与乙烯在催化剂金属镍表面反应生成乙烷,微观过程如图所示:

①金属镍在化学反应前后
②反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】“嫦娥五号”月球采样返回,“天问一号”成功抵达火星,标志着我国航天事业取得突破性进展。
(1)月壤含CaAl2Si2O8以及可作为核聚变燃料的氦-3等物质。
①CaAl2Si2O8中,Si、O两种元素的质量比为____________ 。
②如图为氦在元素周期表中的部分信息。氦-3原子的质子数与中子数之和为3则其中子数为_______ 、核外电子数为_______ 。

(2)着陆器上的仪器可探测水。若月球上存在大量的水,可利用光催化分解水技术得到氧气,对人类在月球上活动意义重大,该反应的化学方程式为__________________ 。
(3)火星拥有丰富的金属矿物和二氧化碳等资源。火星低层大气的主要成分如下表。
①为鉴别一瓶模拟“火星低层大气”组成的气体和一瓶空气,可采用的化学方法是___________ 。
②若为满足人类未来在火星上生活,下列研究设想不合理的是___________ (填标号)。
a.将CO2转化为O2,提高O2含量
b.将CO2分解转化为N2,提高N2含量
c.寻找水的存在和开发水循环技术
d.利用火星上的金属矿物冶炼金属
(1)月壤含CaAl2Si2O8以及可作为核聚变燃料的氦-3等物质。
①CaAl2Si2O8中,Si、O两种元素的质量比为
②如图为氦在元素周期表中的部分信息。氦-3原子的质子数与中子数之和为3则其中子数为

(2)着陆器上的仪器可探测水。若月球上存在大量的水,可利用光催化分解水技术得到氧气,对人类在月球上活动意义重大,该反应的化学方程式为
(3)火星拥有丰富的金属矿物和二氧化碳等资源。火星低层大气的主要成分如下表。
| 气体成分 | CO2 | N2 | Ar | O2 | 其他 |
| 体积分数/% | 95.32 | 2.7 | 1.6 | 0.13 | 0.25 |
②若为满足人类未来在火星上生活,下列研究设想不合理的是
a.将CO2转化为O2,提高O2含量
b.将CO2分解转化为N2,提高N2含量
c.寻找水的存在和开发水循环技术
d.利用火星上的金属矿物冶炼金属
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】在“宏观—微观—符号”之间建立联系,是学习化学的一种重要思维方式。下列是元素周期表中部分元素的原子结构示意图,根据所学知识回答下列问题:

(1)以上四种元素中,属于非金属元素的是______ (填元素符号)。
(2)2个镁离子的符号为______ ,硅的氧化物的化学式为______ 。
(3)相对原子质量与原子真实质量之间存在紧密的关系(见下表),根据下表判断 个钠原子的质量y为
个钠原子的质量y为______ 。请归纳下表中的规律:_____ 。

(1)以上四种元素中,属于非金属元素的是
(2)2个镁离子的符号为
(3)相对原子质量与原子真实质量之间存在紧密的关系(见下表),根据下表判断
 个钠原子的质量y为
个钠原子的质量y为| 碳 | 氧 | 钠 | |
| 相对原子质量 | 12 | 16 | 23 |
 个原子的质量 个原子的质量 | 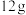 |  | y |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】用恰当的化学符号表示:
(1)2个氧原子______ (2)3个二氧化碳分子 _______ (3)3个亚铁离子______
(4)3个氯离子______
(5)地壳中含量最多的非金属元素和含量最多的金属元素组成的化合物______
(6)2个碳酸根离子__________
(7)氧化铁中铁元素显+3价_______
(8)与KClO3中Cl元素化合价相同的氯的氧化物_______
(1)2个氧原子
(4)3个氯离子
(5)地壳中含量最多的非金属元素和含量最多的金属元素组成的化合物
(6)2个碳酸根离子
(7)氧化铁中铁元素显+3价
(8)与KClO3中Cl元素化合价相同的氯的氧化物
您最近一年使用:0次

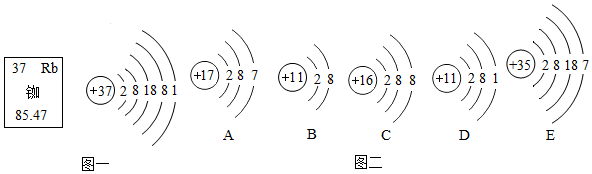
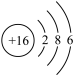 表示的微粒所形成的离子
表示的微粒所形成的离子

